Уравнения, применяемые к неидеальным (реальным) растворам. Термодинамическая константа ионизации.
Понятие “активность”введено в науку для того, чтобы законы, сформулированные для идеальных систем, были применимы к (неидеальным) реальным системам. Подстановка величин активности вместо молярных концентраций в уравнение закона действия масс делает эти уравнения применимыми к нёидеальным (реальным) системам. Закон действующих масс - скорость химической реакции пропорциональна произведению концентраций реагирующих веществ. Например, для обратимой реакции А + В↔С + D после замены молярных концентраций их активностями получим;
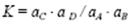
или, заменив активности их значениями а = с f, будем иметь: 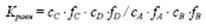
Точно так же при замене в уравнениях констант ионизации равновесных концентраций активностями ионов получаются уравнения, справедливые в отношении растворов сильных электролитов, концентрированных растворов слабых электролитов и растворов слабых электролитов в присутствии сильных электролитов.
Константы электролитической ионизации, определяемые с помощью активностей, называются истинными или термодинамическими константами электролитической ионизации. Величины термодинамических констант не зависят от концентрации растворов и потому подчиняются закону действия масс.
Пользуясь величинами термодинамических констант, можно находить активности ионов в растворе и решать ряд других задач, например находить рН и рОН растворов и т. д.
10. Основные типы равновесий в растворах. Константы химического равновесия (истинная, термодинамическая, концентрационная). Действие одноименного иона.
Типы химических реакций (равновесий):
1) с переносом протона – кислотно-основные реакции;
2) с переносом электрона – окислительно-восстановительные реакции;
3) с переносом электронных пар с образованием донорно-акцепторных связей – реакции комплексообразования.
Химическое равновесие - это такое состояние обратимого процесса, в котором скорость прямой и обратной реакций равны между собой.
Концентрации веществ в состоянии химического равновесия называются равновесными: [Ā], моль/л.
Кинетические кривые обратимой реакции аА↔bВ
Кинетическое описание химического равновесия основано на законе действующих масс: скорость реакции прямо пропорциональна концентрации реагирующих веществ.
Отношение констант скорости является постоянной величиной, обозначаемой Kc:
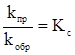
где Kс – концентрационная константа равновесия.
Таким образом, закон действующих масс для обратимой реакции записывается так:
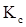
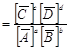
Величина константы равновесия, выраженная через активности реагирующих веществ, называется термодинамической константой равновесия.
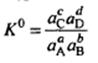
Запишем выражения, используя вместо активностей частиц их равновесные концентрации.
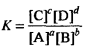
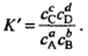
Эти величины называются концентрационными константами равновесия. При этом К – реальная, а К’ – условная константа равновесия.
Действие одноименного иона.
Степень диссоциации слабых электролитов можно искусственно понижать.
СН3СООН  СН3СОО– + H+
СН3СОО– + H+
Если в раствор добавить CH3COONa, то, являясь сильным электролитом, эта соль дает большое количество ионов CH3COO- => их концентрация увеличивается. Равновесие при этом сместится влево и степень диссоциации кислоты уменьшится, концентрация H+ понизится.
11. II аналитическая группа катионов (Аg+, Pb2+, Hg22+) и их специфические реакции.
Общая характеристика группы
 Из солей этих катионов хорошо растворимыми в воде являются лишь нитраты. Оксиды и гидроксиды трудно растворимы. Cеребра (I) гидроксид неустойчив: в момент образования большая часть молекул разлагается по схеме: 2 AgOH ↔ Ag2O↓ + H2O
Из солей этих катионов хорошо растворимыми в воде являются лишь нитраты. Оксиды и гидроксиды трудно растворимы. Cеребра (I) гидроксид неустойчив: в момент образования большая часть молекул разлагается по схеме: 2 AgOH ↔ Ag2O↓ + H2O
Соляная кислота с ионами серебра, свинца, ртути (I) образует трудно растворимые осадки хлоридов. Так как остальные катионы, изучаемые нами, не дают нерастворимых хлоридов, соляная кислота может быть использована в качестве группового реактива на катионы II группы.
Химический анализ катионов II группы имеет большое значение в определении качества изделий из стекла, пищевых продуктов.
Реакции обнаружения катионов свинца (Pb2+)
Действие группового реактива HCl: Pb(NO3)2 + 2 HCl → PbCl2↓ + 2 HNO3
Pb2+ + 2Cl‾ → PbCl2↓
Работа с осадками: осадок свинца (II) хлорида растворим в горячей воде. При охлаждении кристаллы свинца (II) хлорида снова выпадают.
Едкие щелочи:ионы свинца – белый осадок свинца (II) гидроксида:
Pb(NO3)2 + 2 NaOH → Pb(OH)2↓ + 2 NaNO3
Pb2+ + 2 OH‾ → Pb(OH)2↓
Свинца (II) гидроксид обладает амфотерными свойствами и поэтому в избытке щелочи растворяется с образованием гидроксокомплекса свинца:
Pb(OH)2 + 2 NaOH → Na2[Pb(OH)4]
Pb(OH)2 + 2 OH‾ → [Pb(OH)4]2‾
1. Калия иодид KI – дает с ионами свинца осадок ярко-желтого цвета:
Pb(NO3)2 + 2 KI → PbI2↓ + 2 KNO3
Pb2+ + 2 I‾ → PbI2↓
Осадок растворим в горячей воде в уксусной среде. После охлаждения выпадают красивые золотистые кристаллы свинца (II) иодида.
2. Серная кислота и растворимые сульфаты образуют с ионами свинца белый кристаллический осадок свинца (II) сульфата. Осадок растворим при нагревании в едких щелочах с образованием натрия тетрагидроксоплюмбата (II):
Pb(NO3)2 + H2SO4 → PbSO4↓ + 2 HNO3
Pb2+ + SO42‾ → PbSO4↓
PbSO4 + 4 NaOH → Na2[Pb(OH)4] + Na2SO4
PbSO4 + 4 OH‾ → [Pb(OH)4]2‾ + SO42‾
Осадок растворим также в растворе аммония ацетата при нагревании.
3. При добавлении калия дихромата (K2Cr2O7) или калия хромата (К2CrO4) к нейтральному или уксуснокислому раствору соли свинца образуется осадок ярко-желтого цвета PbCrO4:
2 Pb(NO3)2 + K2Cr2O7 + 2 CH3COONa + H2O → 2 PbCrO4↓ + 2 CH3COOH + 2 KNO3 + 2 NaNO3
2 Pb2++ Cr2O72‾ + 2 CH3COO‾ + H2O → 2 PbCrO4↓ + 2 CH3COOH
Осадок PbCrO4 малорастворим в разбавленных HNO3 или HCl; практически нерастворим в аммиаке, уксусной кислоте, аммония ацетате. Растворяется в NaOH и концентрированной HNO3.
PbCrO4↓ + 4 NaOH → Na2[Pb(OH)4] + Na2CrO4
PbCrO4↓ + 4 OH‾ → [Pb(OH)4]2‾ + CrO42‾
Эта реакция позволяет отличить PbCrO4 от BaCrO4, который не растворяется в NaOH.
Реакции обнаружения катионов ртути (I) (Hg22+)
Действие группового реактива HCl: Hg2(NO3)2 + 2 HCl → Hg2Cl2↓ + 2 HNO3
Hg22+ + 2Cl‾ → Hg2Cl2↓
Работа с осадками: Hg2Cl2 + 2 NH4OH → [NH2Hg2]Cl↓ + NH4Cl + 2 H2O
[NH2Hg2]Cl → [NH2Hg]Cl↓ + Hg↓
Едкие щелочи:ионы ртути (I) – черный осадок оксида ртути (I):
Hg2(NO3)2 + 2 KOH → 2 HgOH↓ + 2 KNO3
 |  |
Hg2O↓ H2O
Hg22+ + 2 OH‾ → Hg2O↓ + H2O
2. Характерной реакцией для катиона Hg22+ является также взаимодействие их с калия иодидом, при которой образуется темно-зеленый осадок Hg2I2.
Hg2(NO3)2 + 2 KI → Hg2I2↓ + 2 KNO3
Hg22+ + 2 I‾ → Hg2I2↓
Hg2I2 + 2 KI → K2[HgI4] + Hg↓
Hg2I2 + 2 I‾ → [HgI4]2‾ + Hg↓
Таким образом, если в растворе отсутствуют катионы Ag+, Pb2+, Cu2+ и в значительных концентрациях Bi3+ и Fe3+, то калия иодид будет специфическим реактивом на катионы одновалентной ртути, так как все остальные катионы не будут мешать открытию Hg22+ этим реактивом.
3. Металлическая медь восстанавливает ртуть из ее солей в виде металлической ртути (осадок черного цвета). Эту реакцию рекомендуют проводить капельным методом. Открытию ртути мешают только катионы Hg22+ и больших концентраций Ag+.
Cu + Hg2(NO3)2 → 2 Hg↓ + Cu(NO3)2
Cu + Hg22+ → 2 Hg↓ + Cu2+
Опыт: Каплю раствора, содержащего ионы одновалентной ртути, помещают на хорошо очищенную медную пластинку. Через несколько минут на поверхности пластинки (под каплей) образуется темно-серое пятно металлической ртути. Если полученное при этом пятно протереть тканью или бумагой, то оно обретает вид зеркала.
4. Калия хромат (или калия дихромат (K2Cr2O7)) дает при нагревании с солями ртути (I) кирпично-красный осадок Hg2CrO4, растворимый в азотной кислоте.
Hg2(NO3)2 + K2CrO4 → Hg2CrO4↓ + 2 KNO3
Hg22+ + CrO42‾ → Hg2CrO4↓
Реакции обнаружения катионов серебра (Ag+)
Действие группового реактива HCl: AgNO3 + HCl → AgCl↓ + HNO3
Ag+ + Cl‾ → AgCl↓
Работа с осадками: осадок серебра хлорида нерастворим в разбавленных кислотах (HNO3, H2SO4), но растворим в растворе NH4OH с образованием комплексной соли
AgCl + 2 NH4OH → [Ag(NH3)2]Cl + 2 H2O
AgCl + 2 NH4OH → [Ag(NH3)2]+ + Cl‾ + 2 H2O
Комплексную соль серебра (аммиакат серебра) можно разрушить:
1) действием азотной кислоты:
[Ag(NН3)2]Cl + 2 HNO3 → AgCl↓ + 2 NH4NO3
[Ag(NН3)2]+ + Cl‾ + 2H+ → AgCl↓ + 2 NH4+
2) действием калия иодида (избытком):
[Ag(NН3)2]Cl + KI + 2 H2O → AgI↓ + KCl + 2 NH4OH
[Ag(NН3)2]+ + I‾ + 2 H2O → AgI↓ + 2 NH4OH
В первом случае выпадает осадок белого цвета, во втором случае – осадок бледно-желтого цвета.
Едкие щелочи:ионы серебра – бурый осадок оксида серебра:
2 AgNO3 + 2 NaOH → Ag2O↓ + 2 NaNO3 + H2O
2 Ag+ + 2 OH‾ → Ag2O↓ + H2O
Осадок в избытке щелочи не растворяется.
1. Калия иодид KI – дает с ионами серебра осадок бледно-желтого цвета:
AgNO3 + KI → AgI↓ + KNO3
Ag+ + I‾ → AgI↓
Осадок нерастворим в растворе аммиака, кислотах. Открытию катиона Ag+ данной реакцией мешают катионы Hg22+, Pb2+, Cu2+, Fe3+.
2. Калия хромат (или калия дихромат (K2Cr2O7)) при взаимодействии с солями серебра образует кирпично-красный осадок Ag2CrO4, растворимый в азотной кислоте и NH4OH, но нерастворимый в уксусной кислоте:
2 AgNO3 + K2CrO4 → Ag2CrO4↓ + 2 KNO3
2 Ag+ + CrO42‾ → Ag2CrO4↓
12. Систематический анализ смеси катионов II аналитической группы.5
| Анализируемый раствор: обработка HCl и фильтрование |  | Фильтрат отбрасывают |
 Осадок: AgCl, PbCl2, Hg2Cl2; обработка горячей водой Осадок: AgCl, PbCl2, Hg2Cl2; обработка горячей водой |
| Фильтрат: открывают Pb2+ калия иодидом или K2Cr2O7 |
| Фильтрат: открывают Ag+ при помощи KI или K2CrO4 |
Осадок: AgCl, Hg2Cl2;  обработка раствором аммиака и открытие ртути Hg22+; растворение AgCl обработка раствором аммиака и открытие ртути Hg22+; растворение AgCl |
