Описание экспериментальной установки
Установка для изучения технологических параметров процессов реагентного осаждения представлена на рисунке 2. Через трансформатор 1, проводится регулирование напряжение, подаваемого на нагревательную плитку 2. На плитку устанавливается колба 3, в которую помещается раствор для осаждения. В раствор погружен термометр 4 для контроля за температурой осаждения. Раствор перемешивается с помощью мешалки 5. Мешалка приводится в движение двигателем 6. Частота оборотов мешалки изменяется при помощи лабораторного автотрансформатора 7. Раствор осаждающего реагента приливается из бюретки 8.
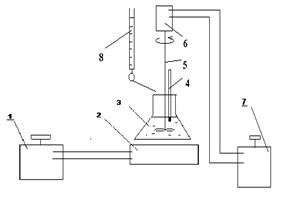
Рисунок 2 Экспериментальная установка для изучения технологических параметров процессов реагентного осаждения
Порядок выполнения работы.
- Приготовить 100 мл раствора сульфата меди с различной концентрацией 1, 5, 10, 20, 50, 100, 200, 250, 300, 350, 400, грамм соли на литр. Поместить раствор в колбу
Учитывать, что растворимость сульфата меди сильно зависит от температуры. Данные о растворимости представлены в таблице 2.
Таблица 2
Растворимость сульфата меди при различных температурах
| Растворимость, г/л | ||||||||||
| Температура, 0С |
- Рассчитать какой объем насыщенного раствора NaOH потребуется для осаждения всей меди из раствора в виде гидрооксида меди. Приготовить насыщенный раствор NaOH и залить его в бюретку. К раствору сульфата меди по каплям прибавлять из бюретки насыщенный раствор гидрооксида натрия. Включить мешалку, поддерживать температуру, указанную преподавателем.
- К раствору сульфата прилить не сразу весь объем щелочи, а некоторую его часть, по указанию преподавателя.
- После того как сформировался осадок, отфильтровать пульпу через вакуумный фильтр. Оставшийся в колбе осадок смыть на фильтр маточным раствором.
- Высушить, взвесить осадок и сдать его для анализа на содержание меди. Полученный результат занести в таблицу 3.
- Повторить опыт при различном расходе осаждающего реагента (раствора щелочи), различной концентрации NaOH в осаждающем растворе, различной температуре, при добавке примесных солей, влияющих на ионную силу раствора и степень извлечения меди в осадок, при различной исходной концентрации сульфата меди в растворе. Результаты опытов записывать в таблицу 3.
- Повторить опыт используя нитрат, хлорид и ацетат меди
Таблица 3
Результаты опытов по изучению технологических показателей процесса реагентного осаждения меди из раствора сульфата меди.
| С Н2SO4, % | Объем раствора NaOH | Масса | Т, 0С | Активность | m | ПР | Степень извлечения Cu в осадок | ||||
| Стехиом. | Факт. | осадка | Cu в осадке | Cu2+ | ОН- | факт. | теор. | ||||
4. Обработка экспериментальных данных, содержание отчета
- Рассчитать согласно стехиометрии реакции расход гидрооксида натрия на осаждение ионов меди из раствора сульфата меди.
CuSO4 + 2 NaOH = Cu(OH)2 + Na2SO4
NaOH = 2 * MCuSO4 * MrNaOH / MrCuSO4
- Рассчитать объем раствора щелочи по формуле:
V NaOH = NaOH / CNaOH, (9)
где: V NaOH - объем раствора щелочи
CNaOH - концентрация раствора щелочи (задается преподавателем или принимается как для насыщенного раствора при данной температуре – 1000-1100 грамм / литр)
- Рассчитать фактическую степень извлечения меди в осадок по формуле:
Хфакт = Мосадка * [Cu, %]осадка * MrCuSO4 / МCuSO4 * ArCu (10)
- Рассчитать концентрацию ионов меди в маточном растворе как корень квадратный из произведения растворимости. ПР Cu(OH)2 = 2,2*10-20
- Рассчитать теоретическую степень извлечения меди, без учета ионной силы раствора, как описано в примере 3.
- Найти отношение объема фактически прилитого раствора щелочи к стехиометрическому объему.
- Построить график зависимости фактической степени извлечения меди в осадок от, найденного выше, отношения для различных температур, исходных концентраций сульфата меди и щелочи в осадителе, и различных исходных солей меди – нитрата, хлорида, ацетата и т.д.
- Используя математический пакет корреляционно-регрессионного анализа построить математическую модель процесса реагентного осаждения ионов меди как зависимость вида Х CuSO4 = f (Vфакт / Vстехиометр, С Н2SO4, температура, CNaOH)
- Дополнительно рассчитайте ионную силу раствора, коэффициенты активности Cu2+ , ОН- и ПР с учетом коэффициентов активности по формулам 6, 7, 8 и данным таблицы 1. С учетом изменившегося ПР рассчитать теоретическую степень извлечения меди в осадок. Расчет вести исходя из стехиометрического расхода щелочи на связывание ионов меди.
- Сделать выводы по проведенной работе и предложить технологические параметры процесса осаждения меди из раствора
Контрольные вопросы:
- Опишите общую схему процессов осаждения – выщелачивания
- Объясните природу процессов, сопровождающих явления растворения – осаждения
- Как описывается скорость процессов растворения – осаждения ?
- Что такое произведение растворимости (ПР) ? Как выводится формула для расчета ПР ?
- Как рассчитать концентрацию насыщенного раствора соли, зная произведение растворимости ?
- Как опытным путем определить ПР ?
- Как рассчитать теоретическое значение степени извлечения иона в осадок, зная ПР ?
- Как рассчитать концентрацию насыщенного раствора соли, зная ПР ?
- Что такое ионная сила раствора ? Закон Льюиса ?
- Закон Дебая-Хюккеля ?
- Что такое цементация ?
- Какие были сделаны выводы по работе и предложены технологические параметры процесса осаждения ?
