Г) всех перечисленных факторов
71. Степень диссоциации слабого основания в растворе:
а) не зависит от природы слабого основания и растворителя;
б) уменьшится при увеличении температуры;
в) уменьшится при увеличении концентрации основания;
г) увеличится при добавлении в раствор гидроксида натрия.
72. Степень диссоциации синильной кислоты (К = 7·10 – 10) в растворе с концентрацией 0,05 моль/л равна:
а) 0,0108%; б) 0,0118 %; в) 1,1800%; г) 0,1800%.
73. При степени диссоциации 21% из каждых 200 внесенных в раствор молекул на ионы распадается:
а) 21; б) 42;в) 79; г) 179.
74. При диссоциации одной молекулы какого электролита образуются три различных по составу иона:
а) КОН; б) NaHCO3;в) Al2(SO4)3; г) Н3РО4.
75. Отметьте формулу сильного электролита в водном растворе:
а) CH3COOH; б) NH4OH; в) K2SO4;г) С2Н5ОН
76. Укажите суммарное количество (моль) ионов Н+ и F- в растворе HF, если α=8%, а общее количество растворенных молекул составляет 0,1 моль:
а) 0,008; б) 0,100; в) 0,016;г) 0,080.
77. При полной диссоциации 0,1 моль Ва(ОН)2 общее количество (моль) ионов Ва2+ и ОН- в растворе равно:
а) 0,1; б) 0,2; в) 0,3;г) 0,4
78. Определите, какое количество CaCl2 (моль) было растворено, если при полной диссоциации общее количество ионов Са2+ и Cl- в растворе составляет 0,6 моль:
а) 0,6; б) 0,3; в) 0,2;г) 0,4
79. На каждые 20 распавшихся молекул НХ приходится 140 не распавшихся. Степень электролитической диссоциации НХ равна (%):
а) 14,3; б) 12,5;в) 20,0; г) 10,0
80. Уравнение, которое наглядно показывает связь между концентрацией слабого электролита и степенью его диссоциации и дает возможность вычислять степень диссоциации при различных концентрациях электролита, если известна его константа диссоциации:
а) К~α2С;б) α~ КС2; в) К~α2(1-α); г) К~α2 +С
81. Кажущаяся степень диссоциации (%) раствора хлорида натрия (М=58,5 г/моль), замерзающего при минус 0,6170С и содержащего в 200 г воды 2,5 г соли (криоскопическая константа воды 1,86) равна (ответ дать с точность до целого):
а) 55%; б) 5%; в) 35%; г) 45%
82. Ионная сила раствора Na2SO4 c концентрацией 0,02 моль/л равна:
а) 0,12; б) 0,06; в) 0,08; г) 0,10
83. Ионная сила раствора Fe2(SO4)3 c концентрацией 0,02 моль/л равна:
а) 0,3; б) 0,15; в) 0,35; г) 0,45
84. Удельная электрическая проводимость растворов сильных электролитов при уменьшении их концентрации:
а) возрастает, достигая максимального значения, затем не изменяется;
б) возрастает, достигая максимума, затем уменьшается;
в) уменьшается, достигая минимума, затем увеличивается;
г) не изменяется
85. Эквивалентная электрическая проводимость растворов сильных электролитов при уменьшении их концентрации:
а) возрастает, достигая максимального значения, затем не изменяется;
б) возрастает, достигая максимума, затем уменьшается;
в) уменьшается, достигая минимума, затем увеличивается;
г) не изменяется
86. Эквивалентнаяэлектрическая проводимость исследуемого раствора уксусной кислоты равна 4,815 См·м2·кг-экв-1. Эквивалентная электрическая проводимость раствора уксусной кислоты при бесконечном разведении 39,060 См·м2·кг-экв-1. Степень диссоциации (%) исследуемого раствора равна (ответ дать с точностью до целых):
а) 13%; б) 1%; в) 12%; г) 10%
87. Единицами измерения удельной и эквивалентной электрической проводимости являются соответственно:
а) Ом · м – 1 и Ом · м 2 · моль; в) См · м – 1 и См · м2 · моль– 1;
б) См · м и См · м 2 · моль– 1; г) См – 1 · м и См – 1 · м2 · моль
88. Удельная и эквивалентная электропроводность связаны между собой в единицах СИ соотношением:
а) 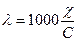 ; б)
; б) 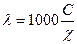 ; в)
; в) 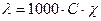 ; г)
; г) 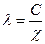 .
.
89. В бесконечно разбавленном растворе слабого электролита:
а) λ → 1; α → 1; б) λ → 1; α → 0; в) λ → λ ∞; α → 0; г) α → 1; λ → λ ∞
90. Числом переноса называется величина, характеризующая:
а) долю общего электричества, переносимую ионами данного вида;
б) долю участия катионов и анионов в переносе электричества;
в) долю тока, переносимую данным ионом;
г) правильными являются все ответы
91. Метод прямой кондуктометрии основан на измерении:
а) электродного потенциала; в) плотности тока;
б) электропроводности; г) потенциала полуволны
92. Укажите формулу, выражающую закон Кольрауша о независимом движении ионов:
а) 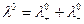 ;б)
;б) 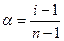 ; в)
; в) 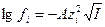 ; г)
; г) 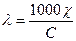
93. Фазой называется:
а) система в определенном агрегатном состоянии;
б) гетерогенная система;
в) равновесная система;
