Обработка результатов исследования
Исследования проводятся с использованием дериватографа Паулик-Паулик и Эрдей. Объект исследования (CuS, Cu2S, ZnS, PbS, FeS) выбирается преподавателем.
Тепловыделение в процессе эксперимента описывается формулой:
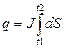
(6)
где: dS- элементарная площадка, зафиксированная самопишущим прибором за время dt; q- тепловыделение, t1 и t2 - время начала и конца процесса; J - постоянная эксперимента.
На рисунке 3 приведена типичная дифференциальная кривая. Площадь термограммы, заштрихованная на рисунке, пропорциональна количеству выделившегося тепла.
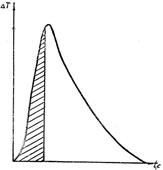
Рисунок 3-Дифференциальная термограмма окисления
Степень протекания процесса (α) за определенный интервал времени пропорциональна отношению площади термограммы к максимальной площади, соответствующей полному протеканию процесса.
Данные эксперимента сводятся в таблицу 1.
Таблица 1- Результаты эксперимента
| Температура, К | Т1 | Т2 | Т3 |
| Интервал времени, сек. | α - степень протекания процесса | ||
| 0-30 | |||
| 0-60 | |||
| 0-90 | |||
| 0-120 | |||
| 0-150 | |||
| 0-180 |
Константу скорости реакции окисления сульфида К при данной температуре находят как тангенс угла наклона, образованного кривой построенной в координатах τ (ось абсцисс) и ln 1/(1-α). (ось ординат), где α - степень протекания процесса, соответствующая времени τ.
Порядок реакции по кислороду определяют из формулы:
lgV=nlgCO2+lgK (7)
где: V- скорость реакции, определяется как тангенс угла наклона кинетической кривой в координатах; α- ось абсцисс; τ- ось ординат; n- порядок реакции по кислороду, определяется как тангенс угла наклона кривой в координатах; lgV-ось абцисс; lgCO2-ось ординат; CO2-концентрация кислорода в газовой фазе.
Кажущаяся энергия активации Е вычисляется но уравнению:
Е=2,3R(lgK2-lgK1)/(1/T1-1/T2), (8)
где: K1 и K2- константы скорости реакции при температурах T1 и T2.
По величине Е оценивают лимитирующую стадию процесса при данной температуре. Значения кажущейся энергии активации- до 1216 кДж/моль соответствуют протеканию реакции в диффузионной области. Протеканию реакции в кинетической области соответствует значение кажущейся энергии активации больше 50-60 кДж/моль. Промежуточное значение E соответствует протеканию реакции в переходной области.
Кроме того лимитирующая стадия оценивается по уравнению Ерофеева. После двойного логарифмирования это уравнение принимает вид:
lg[-lg(1-α)]=nlgt+lg(K·lge), (9)
где n- определяется как тангенс угла наклона в координатах; lg[-lg(1α)]- ось ординат; lgt- ось абсцисс.
Содержание отчета
Отчет должен содержать:
- краткое изложение теоретических основ процесса окисления;
- методику проведения эксперимента;
- эскиз установки;
- результаты обработки опытных данных и выводы.
Контрольное вопросы:
1. Какие методики исследования кинетики окисления сульфидов нашли широкое применение?
2. В чем достоинство используемой методики?
3. Принцип работы дифференциальной термопары. Ее устройство.
4. Чем можно объяснить тот факт, что пирит воспламеняется при более низких температурах, чем пирротин?
5. Пользуясь данными диаграмм зависимости ΔGTo образования сульфидов и окислов от температуры, определить, какой из каждой пары металлов переходит в шлак, а какой - в штейн: Cu-Pb, Fe-Ni, Zn-Ca?
6. На основании данных по зависимости ΔGTo образования сульфидов и сульфатов от температуры определить, какое соединение цинка; сульфид или сульфат - более устойчивое при температуре 673 К?
7. Каким образом можно рассчитать термодинамическую вероятность осуществления реакции взаимодействия сульфида металла и его окисла при заданной температуре?
8. Почему в условиях обычного окислительного обжига сульфидов образуется, как правило, пористая окалина?
Лабораторная работа №5. Измерения поверхностного натяжения и плотности расплавов методом максимального давления в пузырьке газа.
