Определение массовой процентной доли ионов железа в железо-аммонийных квасцах методом фотоколориметрии
Определение основано на измерении оптической плотности раствора железа (III) моносульфосалицилата, образованного при рН=2-3 по реакции:
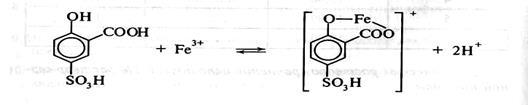
РЕАКТИВЫ:
Железо-аммонийные квасцы, х. ч.; стандартный раствор с концентрацией ионов Fe3+ 100 мкг/см3 (Навеску 0,8633 г NH4Fe(S04)2·12H20 с помощью 25 мл 0.5М раствора H2S04 переносят в мерную колбу на 1 дм3 и доводят объем водой до метки); кислота сульфосалициловая 0,01 М раствор; кислота серная 0,5M раствор.
МЕТОДИКА ВЫПОЛНЕНИЯ РАБОТЫ
1. Приготовление эталонных растворов железа (III) моносульфосалицилата.
Серию эталонных растворов готовят в мерных колбах в соответствии с таблицей. Раствор железо-аммонийных квасцов отбирают пипеткой, а растворы кислот цилиндром. Растворы доводят до метки по нижнему мениску и тщательно перемешивают.
| № эталонного раст-вора | Объемы растворов, см3 | Воды до общего раствора, см3 | Содержание ионов Fe3+ мг/50 см3 | ||
| Стандартный раствор железо-аммонийных квасцов | кислота серная 0,5M раствор | кислота сульфосалициловая 0,01 М раствор | |||
| 0,1 | |||||
| 0,2 | |||||
| 0,3 | |||||
| 0,4 | |||||
| 0,5 | |||||
| - | - |
2. Выбор светофильтра, позволяющего фотометрировать анализируемый раствор в оптимальном диапазоне длин волн, проводят следующим образом. В кювету с толщиной слоя 1 см наливают эталонный раствор средней концентрации (№3) и измеряют его оптическую плотность со всеми светофильтрами. В кювету сравнения наливают холостой раствор (№6). Результаты определений А записывают. Светофильтр, при котором оптическая плотность имеет максимальное значение, выбирают в качестве рабочего для последующих измерений А анализируемого раствора.
2. Измерение оптической плотности эталонных растворов.
Для измерения оптической плотности растворов используют выбранный сфетофильтр и кювету на 1 см. Оптическую плотность каждого раствора измеряют 2-3 раза и вычисляют среднее арифметическое значений А для каждого раствора.
3. Построение градуировочного графика.
Полученные значения оптической плотности эталонных растворов используют для построения градуировочного графика. В координатах А=f (V стандартного раствора) или А=f (mFe).
4. Измерение оптической плотности контрольного раствора.
В колбу с контрольным раствором железо-аммонийных квасцов приливают цилиндром растворы кислот такие же объемы как и для серии стандартных растворов и доводят до метки водой.
5. Определение содержания Fe3+ в контрольной задаче.
По градуировочному графику определяют содержание Fe3+ в мг в контрольной задаче.
ЛАБОРАТОРНАЯ РАБОТА
ОПРЕДЕЛЕНИЕ ХЛОРОВОДОРОДНОЙ И УКСУСНОЙ КИСЛОТ
МЕТОДОМ КОНДУКТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
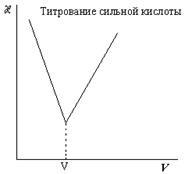
Краткое теоретическое вступление: Определение основано на последовательном взаимодействии с раствором сильного основания NaOH кислот, отличающихся друг от друга степенью ионизации. В первую очередь взаимодействует сильная кислота, что вызывает резкое понижение электролитической проводимости раствора вследствие связывания высокоподвижных ионов водорода: Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
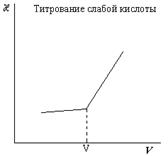
При титровании слабой кислоты проводимость обычно возрастает, так как вместо слабого электролита образуется хорошо диссоциирующая соль: Na+ + OH- + СН3СООН = Na+ СН3СОО- + H2O.
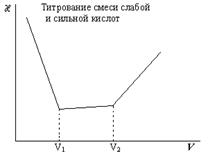
И, наконец, после точки эквивалентности проводимость резко возрастает благодаря появлению в растворе гидроксильных ионов, обладающих высокой подвижностью. V1 – объем щелочи, пошедший на титрование соляной кислоты; V2 – объем щелочи, пошедший на титрование суммы соляной и уксусной кислот.
Цель работы: ознакомление с принципом работы кондуктометра;
определение содержания в исследуемом растворе уксусной и хлороводородной кислот
Ход выполнения:
1.Стандартизация раствора NaOH по HCl. В стакан помещают 10 мл стандартного раствора соляной кислоты, добавляют дистиллированную воду до полного погружения ячейки (электродное отверстие должно быть полностью погружено в раствор); включают магнитную мешалку. При титровании приливают раствор NaOH порциями по 0,5 мл и каждый раз записывают значение удельной электропроводности и объем титранта, пока не обнаружат точку эквивалентности (излом на кривой титрования), соответствующую данной реакции. После этого снимают показания еще в 4 – 5 точках. По полученным данным строят кривую титрования в координатах удельной электропроводности – объем титранта, мл. Находят объем титранта в точке эквивалентности, Vэкв, и рассчитывают концентрацию раствора NaOH.
2. Анализ исследуемого раствора. Исследуемый раствор, содержащий смесь HCl и СН3СООН, доводят до метки, отбирают 10 мл, полученного раствора и переносят в стакан, добавляют воду до полного погружения ячейки и включают мешалку. Титруют раствором NaOH, приливая его порциями по 0,5 мл и в каждой точке записывая сопротивление раствора. Титрование прекращают после того, как будут обнаружены два излома на кривой титрования. Строят кривую титрования, по которым находят V1 и V2.
Обработка результатов:
Таблица 1. Значения удельной электропроводности при стандартизации гидроксида натрия
| Объем NaOH, V, мл | Показание прибора, χ |
| 0,5 | |
| ... |
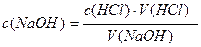
Таблица 2. Значения удельной электропроводности при титровании смеси кислот
| Объем NaOH, V, мл | Показание прибора, χ |
| 0.5 | |
| … |
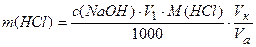
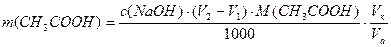
Выводы:
ЛАБОРАТОРНАЯ РАБОТА
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СОЛИ (CuSO4, NiSO4, KCl, NaCl) В РАСТВОРЕ С ПРИМЕНЕНИЕМ КАТИОНИТА
Определение основано на том, что при пропускании раствора соли через колонку с катионитом в Н-форме катионы соли обмениваются на ионы водорода, при этом выделяется кислота в количестве, эквивалентном содержанию соли в растворе. Количество выделившейся кислоты определяют титрованием щелочи.
Процесс катионного обмена можно представить следующим уравнением:
2R-H + CuSO4 → R2-Cu + H2SO4
В большинстве случаев ионный обмен проводят в водной среде, при этом можно определить содержание в растворе любой соли, если соль и соответствующая кислота хорошо растворимы в воде.
Для определения гидролизующихся солей применяют ионный обмен в неводных средах. В качестве сильнокислотных катионитов в этом случае можно использовать катиониты марки СДВ-3, КУ-2 и др. в Н-форме.
Методика определения. Отбирают пипеткой 10 мл анализируемого (~0,1н) раствора соли из мерной колбы и помещают в колонку (диаметр 20 мм, высота 300 мм), содержащую 15 г сильнокислотного катионита в Н-форме. Раствор пропускают через катионит со скоростью 10 мл/мин (примерно 2 капли в 1 с). Вытекающий из колонки раствор собирают в коническую колбу емкостью 300 мл. Затем через катионит пропускают 60 – 100 мл дистиллированной воды, наливая, её из промывалки отдельными порциями по 10 – 15 мл. Новую порцию воды наливают тогда, когда уровень жидкости в колонке достигнет поверхности катионита.
Полноту вымывания выделившейся кислоты проверяют по метиловому оранжевому; для этого отбирают на часовое стекло каплю вытекающего из колонки раствора и прибавляют индикатор. Если при этом окраска раствора станет желтой, то считают, что кислота полностью вымыта из катионита. Промывные воды тщательно собирают в ту же коническую колбу. Всё содержимое конической колбы оттитровывают стандартным 0,1 н раствором NaOH в присутствии метилового оранжевого. Определение проводят 2 – 3 раза, пропуская раствор соли через ту же колонку.
Расчет. Содержание соли (m) вычисляют (в мг) по формуле:
m = MЭсолиVNaOH CNaOH(VK/VA)
где VK – общий объем исследуемого раствора,мл;
VA – объем анализируемого раствора,мл
После окончания определения катионит регенерируют, т.е. снова переводят в Н-форму. Для этого через колонку с катионитом пропускают 200 мл 2 н раствора HCl для извлечения поглощенных катионитов, затем отмывают катионит от кислоты дистиллированной водой и до следующего определения катионит сохраняют в колонке, заполненной водой.
ЛАБОРАТОРНАЯ РАБОТА
