Титрационные кулонометры
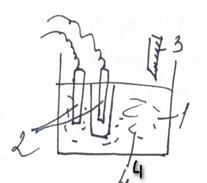
Тетрационные кулонометры представляют собой электролитическую ячейку 1 в которую опушены два платиновых электрода, отрицательно заряженный электрод помещается в пористый стаканчик представляющий собой полупроницаемую мембрану и заполненный раствором KCl, для титрования предусмотрена бюретка 3.
Кулонометры этого типа используются тогда, когда при прохождении электрического тока через раствор образуется какое либо в-во которое м.б. оттитровано (прим. J) в этом титрантом является тиосульфат натрия.
Газовые кулонометры
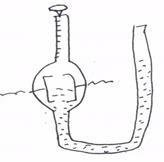
Газовые колонометры представляют собой U образную бюретку с расширением.
В это расширение монтируются круглые платиновые электроды.
Газовый кулонометр заполняется раствором который при электролизе дает газ(прим. Н2О).
Вода при электролизе выделяет Н2 и О2 которая собирается в верхней части бюретки, которая в свою очередь отградуирована. Вполне возможно сразу в (Кл) единицах количества электричества. Ячейку заполняют до верху, закрываю кран и начинают электролиз.
Различают два вида кулонометрического анализа: прямую и косвенную кулонометрию.
В методах прямой кулонометрии анализируемое вещество подвергается электрохимическому превращения в самой ячейке.
В косвенной кулонометрии определяемое в-во реагирует с титрантом.
Титрант получается в кулонометрической ячейке при электролизе специально подобранного раствора. Прямая кулонометрия проводится при контролированном потенциале.
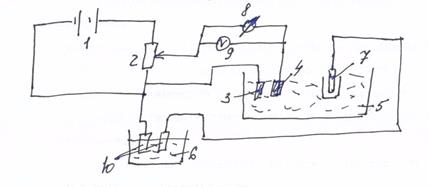
Напряжение от аккумуляторной батареи 1 через регулируемое сопротивление 2 подается в кулонометр 6 куда опущены медные или серебряные электоды. Анализируемый рас-р в кулонометрической ячейке 5 куда опущены 3 электрода, побочный электрод и электрод сравнения 3 (ХС) и вспомогательный электрод 7 опущены в пористый стакан.
Потенциал определяется мили вольтметром 9 , а сила током гальванометром 8. Т.к. данный метод проводится при контролированном, т.е. постоянном потенциале, то необходимо следит за ее величиной и регулировать сопротивление 2.
В данном методе изменение силы тока по мере протекания р-ции в электролитической ячейке зависимость lnJ=f(τ) представляет собой прямую линию
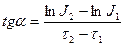
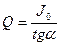
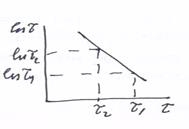
Точка эквивалентности определяется отдельными методами:
1.фотометрическим
2.потенциометрическим
3.амперометрическим
Кулонометрический анализ при контролируемой силе тока
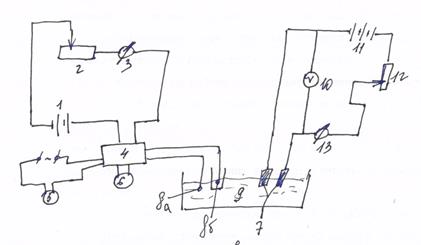
Переключатель 4 питается стабилизирующим напряжением от аккумулятора 1, в сеть включено сопротивлении 2 и гальванометр 3. Гальванометр 3 контролирует силу тока при анализе,(должен показывать постоянное значение). Переключатель соединен с с потенциометром 6 и секундомером 5, по которому определяется время реакции.
При включение генераторной цепи начинается электрохим-я реакция. Генераторная цепь содержит 2 генераторных электрода.
Назначение генераторных электродов состоит в генерирование титранта, при прохождение электрического тока через ячейку. Один из электродов 8а называют рабочим, а8б вспомогательным.
Кроте того в эту же ячейку опущены 2 индикаторных электрода 7, которые представляют собой металлические электроды Pt→Pt либо сис-мы Pt→ХС электрод или Pt→КЭ электрод. Вспомогательный электрод 8б помещен в пористый стаканчик заполненный р-ром KCl.
В измерительной схеме находится аккумулятор 11, гольванометр 13 и вольтметр 10,а так же регулятор сопротивления 12.
Приборы показания которого отвечают за ход хим. р-ции, это гальванометр 13. По мере того как протекает хим. реакция изменяется сила тока. По результатам анализа строят графики J=F(τ)
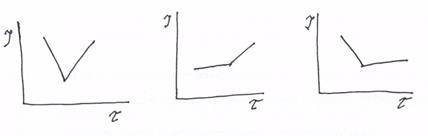
Вид графика зависит от природы пары титруемое вещество- титрант:
1 график: оба в-ва явл. электрохимически активными, т.е. сопряженные пары есть и у титранта и у титруемого в-ва.
2 график: титруется в-во которое явл. электорхимически не активным, после достижения точки эквивалентности появляется сопряженная пара у титранта.
3 график: электролитически активным явл. титруемое в-во, а титрант явл. электролитически не активным.
Характеристика
Кулонометрическое титрование при контролируемой силе тока имеет ряд, преимуществ по сравнению с кулонометрией при контролированном потенциале.
1. Нет необходимости готовить р-р титранта, стандартизировать его т.к. титрант генерирует в кулонометрической ячейке в количестве необходимом для анализа.
2. Легко анализируется , многие легко летучие в-ва, а так же множество органических соединений.
3. Это метод малых концентраций ± 0,05моль/л
4. Высокая чувствительность 10-6 моль/л
5. Высокая селективность
6. Возможность автоматизации
7. Метод явл. универсальным
