Молекулярная физика. Основные положения молекулярно-кинетической теории газов. Идеальный газ. Законы Бойля-Мариотта, Гей-Люссака, Шарля
Молекулярно-кинетическая теория утверждает, чтовсе тела состоят из молекул, атомов или ионов (если речь идет о чистых элементах или ионных кристаллах), находящихся в непрерывном хаотическом движении (тепловое движение). Молекулярно-кинетическая теория экспериментально подтверждается броуновским движением, диффузией (в газах, жидкостях и твердых телах) и прямыми методами визуализации структуры в ионном проекторе и электронном микроскопе.
Идеальный газ — математическая модельгаза, в которой предполагается, что: 1) потенциальной энергией взаимодействия молекулможно пренебречь по сравнению с их кинетической энергией; 2) суммарный объём молекул газа пренебрежимо мал; 3) между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги; 4) время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями. В расширенной модели идеального газа частицы, из которого он состоит, имеют форму упругих сфер или эллипсоидов, что позволяет учитывать энергию не только поступательного, но и вращательно-колебательного движения, а также не только центральные, но и нецентральные столкновения частиц[1].
Закон Бо́йля — Марио́тта — один из основных газовыхзаконов,
Утверждение закона Бойля — Мариотта состоит в следующем[3][4][5]:
При постоянных температуре и массе газа произведение давления газа на его объём постоянно.
В математической форме это утверждение записывается в виде формулы
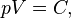
где 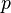 — давление газа;
— давление газа; 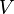 — объём газа, а
— объём газа, а 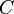 — постоянная в оговоренных условиях величина. В общем случае значение
— постоянная в оговоренных условиях величина. В общем случае значение 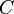 определяется химической природой, массой и температурой газа.
определяется химической природой, массой и температурой газа.
Очевидно, что если индексом 1 обозначить величины, относящиеся к начальному состоянию газа, а индексом 2 — к конечному, то приведённую формулу можно записать в виде
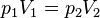 .
.
Из сказанного и приведённых формул следует вид зависимости давления газа от его объёма в изотермическом процессе:
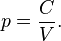
Эта зависимость представляет собой другое, эквивалентное первому, выражение содержания закона Бойля — Мариотта[4][5] . Она означает, что
Давление некоторой массы газа, находящегося при постоянной температуре, обратно пропорционально его объёму.
Тогда связь начального и конечного состояний газа, участвовавшего в изотермическом процессе, можно выразить в виде:
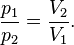
Следует отметить, что применимость этой и приведённой выше формулы, связывающей начальные и конечные давления и объёмы газа друг с другом, не ограничивается случаем изотермических процессов. Формулы остаются справедливыми и в тех случаях, когда в ходе процесса температура изменяется, но в результате процесса конечная температура оказывается равной начальной.
Важно уточнить, что данный закон справедлив только в тех случаях, когда рассматриваемый газ можно считать идеальным. В частности, с высокой точностью закон Бойля — Мариотта выполняется применительно к разреженным газам. Если же газ сильно сжат, то наблюдаются существенные отступления от этого закона.
Закон Гей-Люссака — закон пропорциональной зависимости объёма газа от абсолютной температуры при постоянном давлении
Изобарический закон, открытый Гей-Люссаком в 1802 году утверждает, что при постоянном давлении, объём постоянной массы газа пропорционален абсолютной температуре. Математически закон выражается следующим образом:
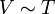
или
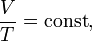
где 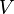 — объём газа,
— объём газа, 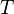 — температура.
— температура.
Если известно состояние газа при неизменном давлении и двух разных температурах, закон может быть записан в следующей форме:
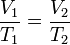
или
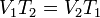 .
.
Зако́н Ша́рля или второй закон Гей-Люссака — один из основных газовых законов, описывающий соотношение давления и температуры для идеального газа.
Формулировка закона Шарля следующая:
Давление газа фиксированной массы и фиксированного объёма прямо пропорционально абсолютной температуре газа.
Проще говоря, если температура газа увеличивается, то и его давление тоже увеличивается, если при этом масса и объём газа остаются неизменными.Закон имеет особенно простой математический вид, если температура измеряется по абсолютной шкале, например, в градусах Кельвина. Математически закон записывают так:
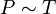
или
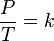
где:
P — давление газа,
T — температура газа (в градусах Кельвина),
k — константа.
Этот закон справедлив, поскольку температура является мерой средней кинетической энергии вещества. Если кинетическая энергия газа увеличивается, его частицы сталкиваются со стенками сосуда быстрее, тем самым создавая более высокое давление.
Для сравнения того же вещества при двух различных условиях, закон можно записать в виде: