Теоретическое обоснование. Кислотно-основное титрование (протолитометрия) относится к классическим методам
Кислотно-основное титрование (протолитометрия) относится к классическим методам химического анализа и основано на протекании в растворе реакции нейтрализации между определяемым веществом и раствором реагента (рабочий раствор). В процессе титрования происходит изменение кислотности среды, что фиксируется по изменению цвета специальных веществ – индикаторов или же путем непосредственного измерения рН среды. В момент резкого изменения кислотности среды (область скачка на кривой титрования) фиксируется расход объема титранта, дальнейшие расчеты проводятся по закону эквивалентов.
Так как расчет основан на законе эквивалентов, то необходимо правильно готовить и определять концентрации применяемых растворов реагентов. В протолитометрии это растворы кислот, щелочей, солей слабых кислот и солей слабых оснований. Любой раствор, концентрация которого точно известна, называют стандартным титрованнымраствором или просто титрованным.
Исходя из способа приготовления, различают растворы с приготовленным титром или первичные стандарты и растворы с установленным титром или стандартизированные.
Первичные стандарты, например, буру, готовят по точно взятой на аналитических весах навеске или из фиксаналов.
Способов приготовления стандартизированных растворов несколько: по приближенной навеске, методом разбавления из концентрированного раствора, ионным обменом. Концентрация таких растворов подлежит установлению, то есть стандартизации по другим растворам. В зависимости от устойчивости при хранении различают растворы вторичного стандарта и титрованные. Раствор вторичного стандарта, например 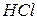 , устойчив и может длительно храниться, тогда как просто титрованный, например
, устойчив и может длительно храниться, тогда как просто титрованный, например 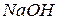 , стандартизируют перед его применением.
, стандартизируют перед его применением.
Рабочие растворы – это растворы, которые используют непосредственно в ходе анализа. Такие растворы не обязательно должны обладать свойствами стандартов.
При приготовлении растворов с установленным титром используют мерную посуду приближенной точности: мензурки, цилиндры, стаканы, колбы с делениями. Взятие навесок выполняют на технических весах с точностью до 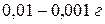 .
.
Наиболее нестойки при хранении растворы щелочей, так как гидроксиды натрия и калия легко вступают в реакцию карбонизации с диоксидом углерода с образованием гидрокарбонатов. Такие растворы необходимо защищать от воздействия воздуха с помощью затворов, содержащих натронную известь, а стандартизировать желательно в тот же день, что и выполнение анализа с их участием. Щелочи растворяют в свежеперегнанной дистиллированной воде, которую дополнительно кипятят в течение 2 – 3-х часов для удаления содержащихся в ней газов.
Приборы и реактивы
Мерные пальчиковые пробирки на 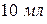 – 2 шт., мерный цилиндр на
– 2 шт., мерный цилиндр на 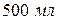 , посуда для хранения растворов на
, посуда для хранения растворов на 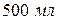 – 2 шт.
– 2 шт.
Жидкие реактивы: концентрированный раствор 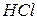 с известной плотностью, концентрированный раствор
с известной плотностью, концентрированный раствор 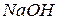 (
( 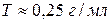 ).
).
4 Указания по технике безопасности (см. стр4)
