Задачи для самостоятельного решения. 1) На титрование навески технической соды массой 0,2005г израсходовано 20,00 мл 0,1010 М
1) На титрование навески технической соды массой 0,2005г израсходовано 20,00 мл 0,1010 М раствора HCl. Вычислить массовую долю Na2CO3 в анализируемом образце технической соды.
Ответ: ω(Na2CO3) = 53,39%.
2) Вычислить объем 0,1025 М раствора NaOH, израсходованный на титрование 0,0450 г молочной кислоты CH3CHOHCOOH.
Ответ: VNaOH = 4,87 мл.
3) Навеска пищевого уксуса массой 9,3600 г растворена в мерной колбе на 1 л, на титрование 10,00 мл полученного раствора израсходовано 10,5 мл 0,1040 М раствора NaOH. Вычислить массовую долю уксусной кислоты в анализируемом образце.
Ответ: ω(СН3СООН) = 70,00%.
4) На титрование 20,00 мл раствора муравьиной кислоты затрачено 15,85 мл раствора NaOH, в 1 мл которого содержится 0,004050 г NaOH. Рассчитать молярную концентрацию раствора муравьиной кислоты.
Ответ: с(НСООН) = 0,0803 М.
5) Какую навеску кальцита, содержащего 60% CaCO3, нужно взять для анализа, чтобы на титрование ее израсходовать 15 мл раствора НСl, 1 мл которого эквивалентен 0,003820 г НСl?
Ответ: 0,1311 г.
6) Навеску 0,6 г H2C2O4∙2H2O растворили в мерной колбе емкостью 100 мл. На титрование 20 мл полученного раствора израсходовали 18.34 мл раствора NaOH. Вычислите молярную концентрацию эквивалента раствора NaOH и сколько г H2C2O4∙2H2O эквивалентно 1 мл раствора NaOH.
Ответ: с(NaOH) = 0,1039 моль/л; 0,006546 г/мл.
7) В техническом этаноле содержание кислоты в пересчете на уксусную составляет 10 мг/л. Какой объем этанола нужно взять для определения кислот, чтобы на титрование расходовалось 2,50 мл 0,0125 М раствора КОН?
Ответ: 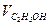 = 183,8 мл.
= 183,8 мл.
8) Навеска мрамора массой 0,2834 г растворена в 30 мл 0,3933 М раствора HCl. На титрование избытка кислоты израсходовано 14,1 мл 0,4409 М раствора NaOH. Вычислить массовую долю примесей в образце.
Ответ: ω(примесей) = 1,48%.
9) Раствор солей кальция и магния разбавили водой до 100,0 мл. На титрование аликвоты объемом 20,00 мл с эриохром черным Т израсходовали 18,45 мл 0,0102 М раствора ЭДТА, а на титрование с мурексидом при рН 12 – 14,5 мл ЭДТА. Какая масса Са2+ и Mg2+ содержалась в исходном растворе?
Ответ: m(Ca) = 0,0296 г; m(Mg) = 0,0049 г.
10) Сколько граммов меди обнаружили в растворе, если на его титрование израсходовано 15,20 мл раствора ЭДТА, 1 мл которого эквивалентен 0,002205 г бария?
Ответ: m(Cu) = 0,0155 г.
11) Вычислить содержание циркония в граммах, если общий объем раствора, содержащего цирконий, равен 100,0 мл. На титрование 10,00 мл этого раствора израсходовали 24,80 мл раствора ЭДТА, 1 мл которого эквивалентен 0,002800 г железа.
Ответ: m(Zr) = 1,1334 г.
12) Молибдат-ион осадили в виде CaMoO4. В осадке оттитровали кальций 12,50 мл раствора ЭДТА с молярной концентрацией 0,0450 М. Рассчитать массу MoO42- в растворе.
Ответ: m(MoO42-) = 89,97 мг.
13) Исследуемый раствор NiCl2 разбавили до 250 мл водой. К 25,00 мл этого раствора прибавили 15,00 мл 0,015 М раствора ЭДТА, избыток которого оттитрован 5,60 мл 0,015 М раствора сульфата магния. Рассчитать массу никеля в исследуемом растворе.
Ответ: m(Ni) = 82,78 мг.
14) Какую навеску щавелевой кислоты (Н2С2О4∙2Н2О) необходимо взять для приготовления 250,0 мл раствора с молярной концентрацией эквивалента 0,0500 М, используемого для определения концентрации раствора KMnO4 методом окислительно-восстановительного титрования.
Ответ: m(Н2С2О4∙2Н2О) = 0,7879 г.
15) Сколько процентов железа(II) содержится в анализируемом образце, если на титрование 25,00 мл раствора, полученного из навески 1,7614 г, растворенной в кислоте и разбавленной в мерной колбе вместимостью 250,0 мл, затрачено 15,50 мл раствора перманганата калия с молярной концентрацией эквивалента 0,1217 М?
Ответ: ω(Fe) = 59,80%.
16) Какой объем раствора KMnO4 с с(1/5 KMnO4) = 0,1525 М потребуется для титрования железа(II) из навески 5,0250 г сплава, содержащего 5% железа?
Ответ: 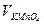 = 29,50 мл.
= 29,50 мл.
17) Из 3,000 г пергидроля приготовили 500,0 мл раствора. На титрование 25,00 мл этого раствора расходуется 40,50 мл перманганата калия с молярной концентрацией эквивалента 0,1000 М. Определить массовую долю Н2О2.
Ответ: ω(Н2О2) = 45,93%.
18) Вычислить рН раствора, в 0,5 л которого содержится 0,56 г КОН.
19) Вычислить рН 0,001 М раствора HCl.
20) Сколько моль NaOH содержится в 0,5 л раствора, рН которого равно 12.
21) Рассчитать рН раствора, в 1 л которого содержится 0,98 г H2SO4.
22) Вычислить рН 0,02 М раствора NaOH.
23) Рассчитать сколько моль HNO3 содержится в 2 л раствора, рН которого равно 1.
24) Рассчитать сколько моль NaOH содержится в 500 мл раствора, рН которого равно 10.
25) Рассчитать рН раствора, в 300 мл которого содержится 0,18 г HCl.
26) Вычислить рН 0,0001 М раствора NaOH
27) Вычислить рН раствора, в 100 мл которого содержится 0,0315 г HNO3.
28) Вычислить рН 0,015 М раствора КОН.
