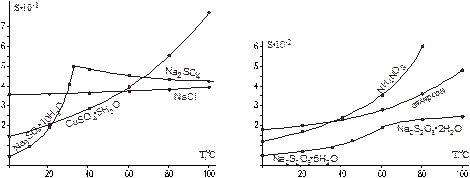Растворение и диссоциация ионных и молекулярных веществ.
Занятие №3
Глинка (2005г.):
1. Задачи на расчет концентраций веществ:
A) № 394, 399, 400, 402, 408
B) № 395, 418, 426 (Рассчитать массовую долю раствора гидроксида натрия, если известно, что его молярная концентрация 9.28 моль/л, плотность раствора 1.31 г/мл), 430(б).
2. Задачи на расчет концентраций ионов:
a) Рассчитать концентрацию катионов:
· в 0.2М растворе MgCl2;
· в 0.2М растворе Na2SO4;
· в насыщенном растворе CaF2
· в насыщенном растворе Ag2SO4
b) Рассчитать рН в растворе:
· серной кислоты (СМ = 0.5∙10-4 моль/л)
· уксусной кислоты (СМ = 10-4 моль/л)
· сероводородной кислоты (СМ = 10-4 моль/л)
· гидроксида калия (СМ = 10-4 моль/л)
· гидроксида бария (СМ = 10-4 моль/л)
· аммиака (СМ = 10-4 моль/л).
Занятие №4
Растворение и диссоциация ионных и молекулярных веществ.
1. Зависимость взаимной растворимости от природы веществ. Сравните строение предлагающихся ионных (молекулярных) веществ: вода, этанол, диэтиловый эфир, йод, сульфат меди. Оцените на основе строения способность к взаимному растворению в парах: вода-этанол, вода-диэтиловый эфир, этанол-диэтиловый эфир. Какие из этих трех жидкостей могли бы оказаться подходящими растворителями для кристаллического йода и сульфата меди?
В две широкие пробирки налейте по 10мл дистиллированной воды, прилейте в одну 3мл этанола, а в другую – 3 мл эфира. При отсутствии видимых признаков растворения, закройте пробирку пробкой и, не встряхивая, несколько раз переворачивая, перемешайте содержимое. Затем перелейте его в делительную воронку и разделите жидкие фазы в разные пробирки. Для доказательства, что частичное взаимное растворение состоялось, перелейте водную фазу в фарфоровую чашку и поднесите к ней горящую лучинку. В пробирку с эфирной фракцией добавьте ½ стеклянной ложечки безводного CuSO4.
Поместите в пробирку немного (в объеме булавочной головки) порошкообразного йода и долейте 2-3мл дистиллированной воды. Меняется ли объем твердой фазы? Появляется ли окраска в растворе? Долейте в ту же пробирку ~0.5мл этанола. Объясните наблюдения (продумайте их заранее).
2. Влияние природы твердых веществ на их растворимость в воде. Тепловые эффекты растворения. Влияние температуры на растворимость. Вам предлагаются следующие кристаллические вещества: сахароза, нитрат аммония, сульфат меди, пентагидрат сульфата меди, сульфат натрия. Учитывая состав твердой фазы, находящейся в равновесии с раствором при комнатных температурах (см. таблицу), а также в горячих растворах:
a)Оцените устойчивость гидратов предложенных веществ, спрогнозируйте знак и относительное значение DН°гидр-ции., знак DН°раст.
b)Применяя принцип Ле-Шателье, сверьте ваши прогнозы с видом кривых растворимости.
c)Почему в таблице и на графиках отсутствуют данные о растворимости CuSO4, Na2S2O3, Na2SO4 (вблизи комнатных температур)?
d)Спрогнозируйте знак и относительное значение DН°раст(NaCl) и дайте объяснение слабой температурной зависимости растворимости данной соли.
e)Дайте ответ на вопрос о температурной зависимости растворимости BaSO4 (см. таблицу).
Налить в пробирку 2–3 мл воды, измерить ее температуру и добавить 2 стеклянные ложечки сахарозы. Опустить термометр на дно пробирки и по изменению температуры определить знак DН°раст. Аналогичные опыты повторить с NH4NO3, CuSO4 и CuSO4∙5H2O.
| Состав кристаллизующихся фаз, т.е. фаз, находящихся в равновесии с раствором | 0 °С | 20 °С | 32 °С | 40 °С | 60 °С | 80 °С | 100 °С |
| Растворимость: масса вещества (г), которую удается растворить в 100г воды | |||||||
| С12Н22О11 | |||||||
| NH4NO3 | |||||||
| NaCl | 35.7 | 35.9 | 36.4 | 37.2 | 38.1 | 39.4 | |
| Na2SO4 | 48.4 | 45.3 | 43.3 | 42.3 | |||
| Na2SO4∙10H2O | 4.5 | 19.2 | 49.8 | ||||
| СuSO4∙5H2O | 14.3 | 20.5 | 28.7 | 39.5 | 55.5 | 77.0 | |
| BaSO4 | Очень маленькие значения. Как меняются – продумайте самостоятельно. | ||||||
| Na2S2O3·5H2O | 50.2 | 70.1 | 105.0 | 191.3 | |||
| Na2S2O3·2H2O | 230.0 | 245.0 |