Молекулярная физика и основы термодинамики
@@@Основы молекулярно-кинетической теории газов
195. Условие обязательного выполнения для того, чтобы газ можно было считать идеальным:
1 ничтожно малые силы взаимодействия между молекулами газа
2 малое расстояние между молекулами по сравнению с их размерами
3 преобладание сил отталкивания между молекулами газа
4 преобладание сил притяжения между молекулами газа
5 ничтожно малые скорости молекул
196. Температура 2г азота, занимающего объем 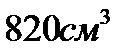 при давлении
при давлении 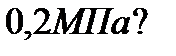 М=28 г/моль равна:
М=28 г/моль равна:
1 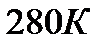
2 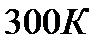
3 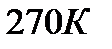
4 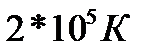
5 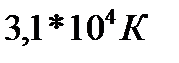
| T |
| P |
1 1
2 2
3 3
4 4
5 ось Т
198. Энергия молекулы идеального газа является:
1 кинетической
2 потенциальной
3 суммой кинетической и потенциальной
4 механической
5 внутренней
199. Баллон емкостью 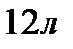 наполнен азотом при давлении
наполнен азотом при давлении 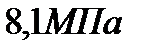 и температуре
и температуре 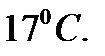 В баллоне находится масса азота, равная:
В баллоне находится масса азота, равная:
1 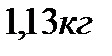
2 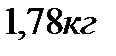
3 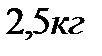
4 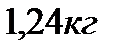
5 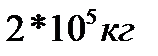
200. Число независимых координат для определения положения в пространстве двухатомной молекулы равно:
1. пять
2. три
3. одна
4. шесть
5. семь
201. Плотность водорода при температуре 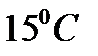 и давлении
и давлении 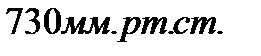 равна:
равна:
1. 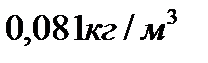
2. 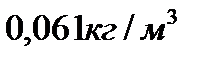
3. 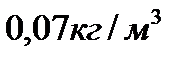
4. 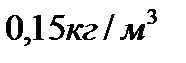
5. 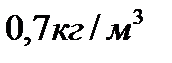
202. Самое большое число степеней свободы имеет:
1. 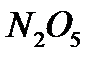
2. 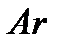
3. 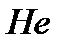
4. 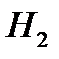
5. 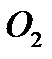
203. На рисунке изображено несколько изотерм. Изотерма, соответствующая самой высокой температуре, изображена кривой:
| 2 3 4 |
| V |
| P |
1. 4
2. 2
3. 3
4. 1
5. ось V
204. Зависимость средней длины свободного пробега молекул газа от его давления:
1. обратно пропорциональная
2. линейная
3. экспоненциальная
4. квадратичная
5. пропорциональная
205. Средняя квадратичная скорость 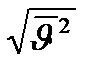 молекул воздуха при температуре
молекул воздуха при температуре 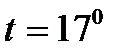 и молярной массе воздуха
и молярной массе воздуха 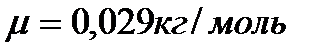 равна:
равна:
1. 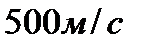
2. 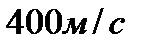
3. 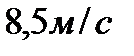
4. 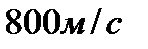
5. 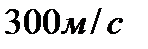
206. Средняя квадратичная скорость молекулы кислорода 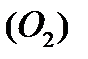 при
при 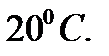 равна:
равна:
1. 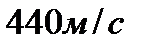
2. 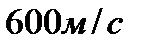
3. 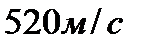
4. 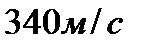
5. 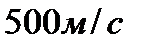
207. Соотношение, выражающее среднюю длину свободного пробега молекул газа, имеет вид:
1. 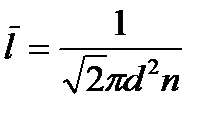
2. 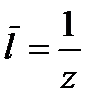
3. 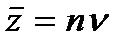
4. 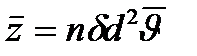
5. 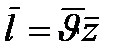
208. Молекулы аргона при нормальных условиях испытывают 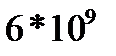 столкновений в секунду при средней длине свободного пробега
столкновений в секунду при средней длине свободного пробега 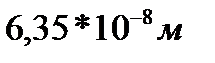 . Средняя скорость поступательного движения молекул аргона равна:
. Средняя скорость поступательного движения молекул аргона равна:
1. 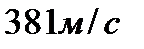
2. 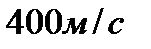
3. 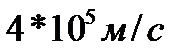
4. 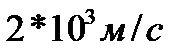
5. 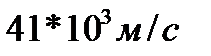
209. Число степеней свободы поступательного движения молекулы равно:
1. 3
2. 5
3. 6
4. 7
5. 2
210. Число степеней свободы одноатомной молекулы равно:
1. 3
2. 5
3. 6
4. 7
5. 2
211. Газ сжимают до половины его исходного объема при постоянной температуре. Средняя энергия молекул идеального газа при этом по отношению к исходной ….
1. не изменяется
2. уменьшается в 2 раза
3.увеличивается в 2 раза
4.увеличивается в 4 раза
5.уменьшается в 4 раза
212. Выберите правильное соотношение средних кинетических энергий молекул кислорода и водорода при одинаковой температуре:
1. Eк = Eв
2. Е к> Eв
3. Eк< Eв
4. соотношение может быть произвольным
5.соотношение зависит от массы названных газов
213. В ответах, представленных ниже, даны определения некоторых физических величин. Среди них выберите определение, соответствующее физической величине – постоянная Авогадро.
1. число молекул или атомов в моле вещества
2. отношение числа молекул в данном теле к числу атомов в 0,012 кг углерода
3. масса вещества, взятого в количестве одного моля
4. количество вещества, содержащее столько же молекул, сколько содержится атомов в 0,012 кг углерода
5. масса вещества
214. Концентрация какого газа выше: одного моля кислорода или одного моля водорода, если газы находятся при нормальных условиях?
1. одинаковы
2. больше для кислорода
3. больше для водорода
4. данных для ответа недостаточно
5. все зависит от давления газа
215. Какая из нижеприведенных формул выражает функцию распределения Максвелла для скоростей молекул газа?
1. 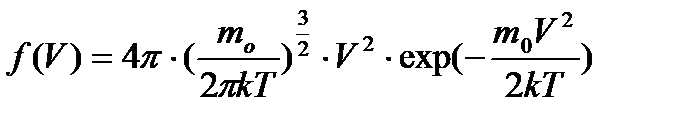
2. 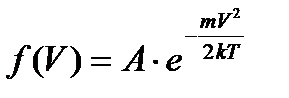
3. 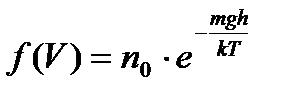
4. 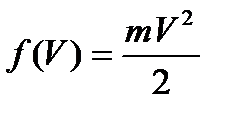
5. 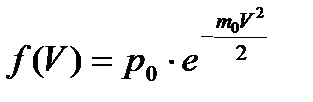
216. Какое из следующих утверждений неправильно:
1. все молекулы имеют одинаковые размеры и массы
2. эти молекулы находятся в постоянном движении, даже в твердых телах
3.вещества состоят из мельчайших частиц, называемых молекулами
4.твердое, жидкое и газообразное состояния вещества обусловлены различной степенью свободы движения составляющих его молекул
5.все приведенные утверждения правильны
217. Что представляет собой броуновское движение?
1. хаотическое движение частиц, взвешенных в жидкостях или газах, обусловленное столкновениями с молекулами
2.состояние, при котором прекращается тепловое движение молекул
3.характеристика степени нагретости тела
4.совокупность ударов молекул о данную поверхность
5.взаимное проникновение молекул соприкасающихся веществ, приводящее к их взаимному перемешиванию
218. Выберите выражение, описывающее распределение давления воздуха в атмосфере Земли.
1.Р=Рo exp(- mgz/ kT)
2.Р= n·к·Т
3.Р·V = const
4.А=Р·V
5.F(v)=А· е-mv ·VdV
219. При какой температуре прекращается тепловое движение?
1. 0 К
2. 273К
3. –2000 С
4. 00 С
5. – 270 С
220. Выберите правильное соотношение средних квадратичных скоростей молекул кислорода (V1) и водорода (V2 ) при одинаковой температуре:
1. V1 < V2
2. V1 > V 2
3. V1 =V2
4. средние квадратичные скорости молекул не зависят от температуры
5. соотношение для скоростей может быть любым
221. Как изменится давление идеального газа, если в данном объеме скорость каждой молекулы
газа уменьшилась в 2 раза, а концентрация молекул не изменилась?
1. уменьшилось в 4 раза
2. увеличилось в 2 раза
3. не изменилось
4. уменьшилось в 2 раза
5. увеличилось в 4 раза
222. Как изменится концентрация молекул газа, имеющего начальную температуру 300 К и
начальное давление 100 кПа, если газ изобарически охладить до -1230 С?
1. увеличится в 2 раза
2. уменьшится в 2раза
3. не изменится
4. уменьшится в 4 раза
5. уменьшится в 4 раза
223. Поскольку температура характеризует внутреннее состояние тел, то температура должна …..
1. определяться состоянием движения молекул
2. определяться сортом молекул
3. быть связана с объемом, занимаемым молекулами
4. определяться только температурой окружающей среды
5. зависеть от давления газа, от сил, действующих на тело
224. Какая из приведенных ниже величин соответствует порядку значения массы молекулы элемента или соединения?
1. 10-27 кг
2. 10-6 кг
3. 10-10 кг
4. 10-16 кг
5. 1027 кг
225. В молекулярной физике используется понятие «идеальный газ». Это понятие применимо, когда можно пренебречь(выберите наиболее полный и точный ответ)…
1. потенциальной энергией взаимодействия частиц и их размерами
2. потенциальной энергией взаимодействия частиц
3. кинетической энергией частиц
4. массой частиц
5. скорость частицы
226. Атмосферный воздух – это смесь газов. Одинаковы ли средние квадратичные скорости
движения молекул этих газов?
1. скорости молекул газов различны, т.к. они зависят и от молярной массы
2. скорости молекул газов одинаковы, т.к. одинакова температура
3. скорости молекул газов различны, т.к. они зависят от атмосферного давления
4. скорости молекул одинаковы, т.к. они не зависят ни от каких факторов
5. скорости молекул газов одинаковы, т.к. они зависят от атмосферного давления
227. Кислород массой 0,1 кг занимает объем 200 л при температуре 200 К. Какому давлению это
состояние газа соответствует?
1. Р=26 кПа
2. Р=0,26 мПа
3. Р=0
4. Р=2,66 кПа
5. Р=390 кПа
228. Что происходит с давлением газа при уменьшении средней квадратичной скорости движения его молекул?
1. давление уменьшается
2. давление возрастает
3. давление не изменяется
4. давление не зависит от скорости
5. трехкратно увеличится
229. Как изменится энергия молекул газа, если температура увеличится в 2 раза:
1. увеличится в 2 раза
2. не изменится
3. уменьшится в 2 раза
4. увеличится в 4 раза
5. уменьшится в 4 раза
230. Плотность какого газа больше при одинаковых давлении и температуре: одного моля кислорода или одного моля водорода?
1. плотность кислорода больше
2. плотность водорода больше
3. плотность газов одинакова
4. для оценки плотности необходимо задать давление газа
5. плотность не зависит от температуры
231. Чем обусловлено давление газа?
1. совокупностью ударов молекул о данную поверхность
2. хаотическим движением частиц, взвешенных в жидкостях или газах, обусловленным столкновениями с молекулами
3. степенью нагретости тела
4. состоянием ,при котором прекращается тепловое движение молекул
5. взаимным проникновением молекул соприкасающихся веществ, приводящим к их взаимному перемешиванию
233. В ответах, представленных ниже, даны определения некоторых физических величин. Среди них выберите определение, соответствующее физической величине - количество вещества.
1. отношение числа молекул в данном теле к числу атомов в 0,012 кг углерода
2. масса вещества, взятого в количестве одного моля
3. количество вещества, содержащее столько же молекул, сколько содержится атомов в 0,012 кг углерода
4. число молекул или атомов в моле вещества
5. масса вещества
234. Как изменится плотность идеального газа при изобарном охлаждении его?
1. увеличится
2. Уменьшится
3. Не изменится
4. данных недостаточно для ответа на вопрос
5. может измениться любым образом
235. В ответах, представленных ниже, даны определения некоторых физических величин. Среди них
выберите определение, соответствующее физической величине – моль вещества.
1. количество вещества, содержащее столько же молекул, сколько содержится атомов в
0,012 кг углерода
2. масса вещества, взятого в количестве одного моля
3. отношение числа молекул в данном теле к числу атомов в 0,012 кг углерода
4. число молекул или атомов в моле вещества
5. масса вещества
236. Масса газообразного водорода в сосуде равна 4 г. Сколько примерно молекул водорода находится в сосуде?
1. 12*1023
2. 1023
3.4*1023
4.2*10-23
5. 10-23
237. Как изменится средняя квадратичная скорость молекул азота, если температура газа увеличилась в 4 раза?
1. увеличится в 2 раза
2. уменьшится в 4 раза
3. увеличится в 4 раза
4. уменьшится в 2 раза
5. не изменится
238. Чем обусловлено броуновское движение?
1. столкновением молекул жидкости (или газа) с частицами, взвешенными в ней (в нем)
2. столкновением частиц, взвешенных в жидкости (или газе)
3. столкновением молекул жидкости (или газа) друг с другом
4. тепловым движением частиц жидкости
5. ни одной из указанных причин
239. В сосуде емкостью 0,83 м3 находится гелий. Масса газа 0,16 кг. При какой температуре гелий
оказывает давление на стенки сосуда, равное 60 кПа ?
1. Т= 150 К
2. Т=3000С
3. Т= 300К
4. Т=1500С
5. Т= 2,4•103 К
240. Оцените приблизительно массу 1 м3 воздуха при нормальном атмосферном давлении и температуре 300 К. Выберите из приведенных ниже значений наиболее близкое к полученному Вами результату.
1. 1 кг
2. 10 г
3. 100 г
4. 1 г
5. 10 кг
241. Если газ находится в нормальных условиях, то давление и температура его равны:
1. Р= 100 кПа, Т= 273 К
2. Р= 0, Т= 273 К
3. Р= 0 Па, t=00 C
4. Р=105 Па, Т= 0 К
5. Р= 1 атм, температура может быть любой
242. Cредняя квадратичная скорость молекул некоторого газа в первом сосуде в 3 раза больше средней квадратичной скорости молекул того же газа во втором сосуде. Чему равно отношение плотности газа в первом и во втором сосудах, если давление газов одинаково?
1. 1/9
2. 3
3. 1
4. 1/3
5. 9
243. К основным положениям молекулярно-кинетической теории следует отнести следующие высказывания:
1. размерами молекул можно пренебречь и молекулы, взаимодействуя между собой, движутся хаотично
2. молекулы веществ могут находиться только в поступательном или вращательном движении
3. молекулы веществ взаимодействуют между собой
4. размерами молекул можно пренебречь 
5. молекулы веществ могут находиться только в поступательном движении
244. Плотность идеального газа можно рассчитать по формуле:
1. 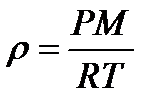
2. 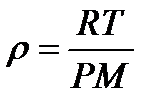
3. 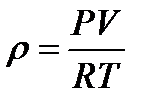
4. 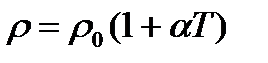
5. 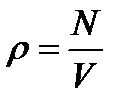
245. Распределение Максвелла – это распределение частиц по..
1. по уровням кинетической энергии
2. уровням потенциальной энергии
3. по уровням полной механической энергии
4. по координатам
5. по концентрации
246. Величина dn/n в распределении Максвелла определяет..
1. относительное число частиц, скорости которых лежат в интервале скоростей от V до (V+dV)
2. абсолютное число частиц, скорости которых лежат в интервале от V до (V+dV)
3. относительное число частиц, скорости которых лежат в единичном интервале скоростей около скорости V
4. вероятность для молекул иметь скорость V
5. изменение концентрации молекул газа
247. График функции распределения Максвелла схематически представлен на рисунке:
1. 2
2. 1
3. 3
4. 2 и возможно 3
5. 1 и возможно 2
248. Максимум на графике распределения молекул по скоростям (по Максвеллу) с увеличением температуры газа…
1. понижается и смещается вправо
2. понижается и смещается влево
3. повышается и остается на прежнем месте
4. повышается и смещается вправо
5. не изменяется
249. Наиболее вероятная скорость находится из условия:
1. 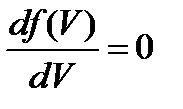
2. 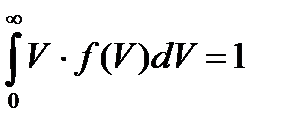
3. 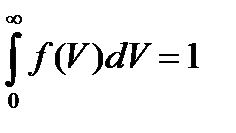
4. 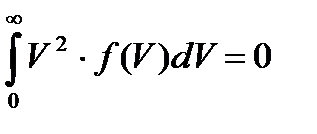
5. 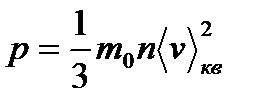
Молекулярная физика 1. (Молекулярно-кинетическая теория)
250. Какое количество степеней свободы имеет молекула двухатомного газа?
1. i = 5;
2. i = 3;
3. i = 6;
4. i = 7;
5. Может быть любым.
251. При нагревании идеального газа средняя квадратичная скорость теплового движения молекул увеличилась в 4 раза. Как изменилась абсолютная температура газа?
1. увеличилась в 16 раз
2. увеличилась в 4 раза
3. увеличилась в 8 раз
4. увеличилась в 2 раза
5. увеличилась в 12 раз
252. Какая из нижеприведенных формул является основным уравнением молекулярно-кинетической теории идеального газа?
1. 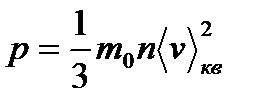
2. v2=v2x+ v2y
3. n= 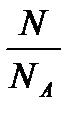
4. pV/N=kT
5. p V= 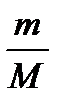 RT
RT
253. Молекулы каких газов (кислорода, водорода или азота), находящихся в воздухе комнаты, движутся быстрее?
1. водорода
2. кислорода
3. азота
4. скорости всех газов одинаковы
5. кислорода и азота
254. При изобарном нагревании идеальный газ переведен из состояния 1 в состояние 2. Как изменилось при этом давление газа? Масса газа постоянна.
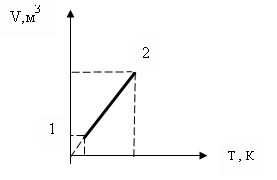
1. не изменилось.
2. уменьшилось.
3. увеличилось.
4. нужно знать массу газа.
5. для разных газов могут быть разные ответы.
255. Внутренняя энергия газа складывается из Ек -суммарной кинетической энергии молекул и ЕП – потенциальной энергии их взаимодействия. При каком соотношении между ЕК и ЕП состояние газа может быть описано уравнением Менделеева - Клайперона?
1. Е K¹0, Еn =0
2. ЕК =0, ЕП¹0
3. Е K = Еn
4. ЕK> 0 u Еn >0
5. Е K=0 и ЕП<0
256. Определить число степеней свободы молекул кислорода (О2).
1. 5
2. 3
3. 6
4. 9
5. 1
257. По какой формуле определяется среднее число соударений молекулы в 1 с?
1. 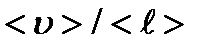
2. 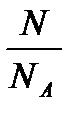
3. 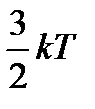
4. 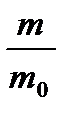
5. 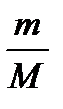
258. Укажите уравнение адиабаты.
1. рVg =const
2. рV =RT
3. рV=const
4. р/V=const
5. V/T=const
259. На графике изображен процесс охлаждения данной массы газа от Т1 до Т2. Как изменилась плотность газа в этом процессе?
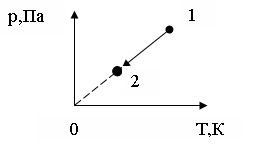
1. не изменилась
2. уменьшилась в два раза
3. уменьшилась
4. увеличилась
5. увеличилась в два раза
260. Указать формулу изохорного процесса.
1. 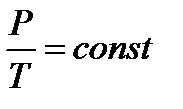
2. 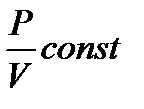
3. 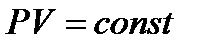
4. 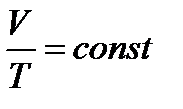
5. 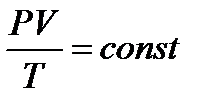
261. При температуре 270С давление газа в закрытом сосуде равнялась 75 кПа. Каким будет его давление при температуре 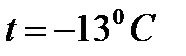 ?
?
1. 65 кПа
2. 5 кПа
3. 15 кПа
4. 20 кПа
5. 35 кПа
262. Один моль в системе СИ является единицей измерения…
1. количества вещества
2. массы вещества
3. молярной массы вещества
4. относительной молекулярной массы
5. массы молекулы
263. Чему равно отношение, средних квадратичных скоростей молекул водорода и кислорода при одинаковой температуре? Молярная масса водорода 2.10-3 кг/моль, кислорода 32.10-3 кг/моль.
1. 4
2. 2
3. 1
4. 16
5. 32
264. Чему равна средняя кинетическая энергия одной молекулы воды?
1. 6кТ
2. кТ
3. 2кТ
4. 3кТ
5. ½кТ
265. Распределение Максвелла представляет собой распределение молекул газа по …
1. по скоростям
2. по размерам
3. по направлениям движения
4. по потенциальным энергиям
5. по массам
266. Какая из формул определяет величину среднеквадратичной скорости поступательного движения частиц одноатомного газа?
1. 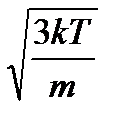
2. 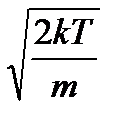
3. 
4. 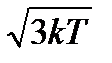
5. 
267. Идеальный газ при температуре Т0 имел давление Р0. При неизменной массе температуру газа при постоянном объеме увеличили в 1,5 раза. Как изменилось давление газа?
1. 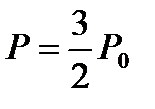
2. 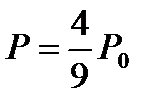
3. 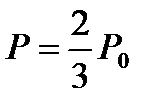
4. 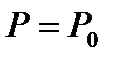
5. 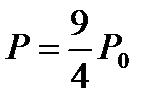
@@@ Основы термодинамики
268. Внутренней энергией идеального газа является:
1. кинетическая энергия хаотического движения молекул газа
2. кинетическая энергия движения газа вместе с сосудом
3. потенциальная энергия взаимодействия молекул
4.внутренняя энергия
Работа в цикле
269. Если заданы начальное и конечное состояния системы, то можно решить задачу:
1. вычисления изменения энтропии
2. определения работы, совершенной системой
3. вычисления количества теплоты, переданной системе
4. изменения импульса системы
5. изменения момента импульса системы
270. Энтропия замкнутой системы, совершающей обратимый цикл Карно:
1. не изменяется
2. уменьшается
3. увеличивается
4. изменение может быть любым
5. уменьшается и увеличивается
271. Рабочее тело идеального теплового двигателя получило от нагревателя 50 кДж
энергии при температуре 5270 С. Определите КПД двигателя и количество
теплоты, переданное холодильнику, если его температура 00 С.
1. 66%, 17 кДж
2. 62,5%, 18,75 кДж
3. 56%, 22 кДж
4. 62,5%, 31,25 кДж
5. 61%, 17 кДж
272. Какая из приведенных формул является уравнением адиабатического процесса?
1. PVy =const
2. PV= ν RT
3. PV=const
4. P = (N/V) kT
5. P/V = const
273. Сравните количество теплоты, полученное газом, и изменение внутренней энергии газа в результате процесса А-В-D и А-С-D
P
1. Q1 > Q2 ΔU1 = Δ U2 A B
2. Q1 > Q2 ΔU1 > Δ U2
3. Q1 < Q2 Δ U1 < ΔU2
4. Q1 < Q2 Δ U1 = Δ U2
C D
5. Q1 < Q2 Δ U1 = Δ U2
0 V
274. В каком направлении может изменяться энтропия незамкнутой системы?
1. Энтропия может вести себя любым образом
2. Энтропия может только увеличиваться
3. энтропия должна оставаться постоянной
4. энтропия может оставаться постоянной либо увеличиваться
5. энтропия незамкнутой системы всегда равна нулю
275. Тепловая машина за цикл получает от нагревателя количество теплоты 100 Дж и отдает
холодильнику 60 Дж. Чему равен КПД машины?
1. 40%
2. 60%
3. ~67%
4. 25%
5.16%
276. В каком из процессов работа газом не совершается?
1. изохорном
2. изобарическом
3. политропном
4. адиабатическом
5. изотермическом
278. Последовательностью каких процессов осуществляется цикл Карно?
1. изотермического- адиабатического- изотермического- адиабатического
2. изотермического- изобарического- адиабатического- изотермического
3. изотермического- изохорического- адиабатического –изотермического
4. адиабатического- изобарического- изотермического-изохорического
5. ни одна из предложенных в А-D последовательностей
279. Энтропия с термодинамической вероятностью связана по формуле:
1. 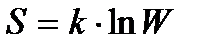
2. 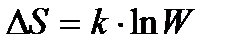
3. 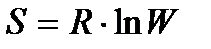
4. 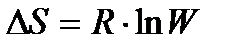
5. 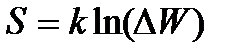
280. При адиабатическом расширении идеальный газ совершил работу А. Какие из приведенных соотношений для количества теплоты Q , полученной газом, и изменения внутренней энергии справедливы
1.Q = 0 -  U = А
U = А
2. Q = A  U = 0
U = 0
3. Q = 0  U = A
U = A
4. Q = - A  U = 0
U = 0
5. Q = 0  U = 0
U = 0
281. В ходе какого процесса работа, совершенная газом, равна убыли его внутренней энергии?
1. адиабатического
2. изохорического
3. изобарического
4. изотермического
5. такой процесс невозможен
282. Что происходит с внутренней энергией газа при изотермическом расширении?
1. остается неизменной
2. возрастает
3. уменьшается
4. может увеличиться или уменьшиться
5. постепенно уменьшается
283. Внутреннюю энергию системы можно изменить…(выберите наиболее точное продолжение фразы)
1. путем совершения работы и теплопередачи
2. путем совершения работы
3. путем теплопередачи
4. изменить внутреннюю энергию невозможно никаким образом
5. изменить можно только при условии обратимого процесса
284. Возможна ли теплопередача от холодного тела к горячему?
1. возможна за счет совершения работы
2. возможна за счет дальнейшего охлаждения холодного тела
3. невозможна ни при каких условиях
4. это зависит от процесса
5. возможна лишь в тепловой машине
285. Чем больше энтропия системы частиц, тем:
1. меньше порядок в системе
2. меньше энергия системы
3. больше энергия системы
4. больше порядок в системе
5. энтропия никак не характеризует поведение системы
286. Рабочее тело идеального теплового двигателя получило от нагревателя 50 кДж энергии при температуре 5270 С. Определите КПД двигателя и полезную работу, выполненную им, если температура холодильника 270 С.
1. 62,5%, 31,25 кДж
2. 56%, 22 кДж
3. 66%, 17 кДж
4. 62%, 18,75 кДж
5. 61%, 30 кДж
287. Холодильная машина:
1. забирает тепло из рабочего объема и рассеивает его в окружающем пространстве
2. производит холод
3. превращает тепло в холод
4. рассеивает тепло
5. холодильная машина является разновидностью тепловой машины
288. Коэффициент диффузии Д водорода при нормальных условиях, если средняя длина свободного пробега 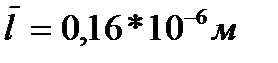 равен:
равен:
1. 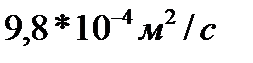
2. 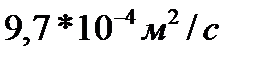
3. 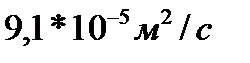
4. 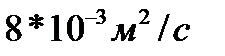
5. 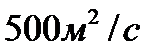
289. При изобарном нагревании некоторой массы кислорода 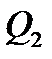 на
на 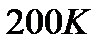 совершена работа
совершена работа 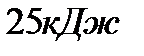 по увеличению его объема. Молярная масса кислорода и универсальная газовая постоянная равны соответственно:
по увеличению его объема. Молярная масса кислорода и универсальная газовая постоянная равны соответственно: 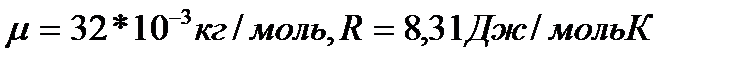 Масса кислорода равна:
Масса кислорода равна:
1. 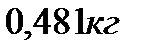
2. 0,520 кг
3. 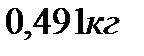
4. 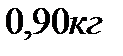
5. 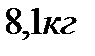
290. Газ изобарно увеличился в объеме в три раза при давлении 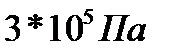 . На увеличение его объема потребовалось совершить работу в
. На увеличение его объема потребовалось совершить работу в 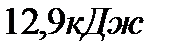 . Первоначальный объем газа равен:
. Первоначальный объем газа равен:
1. 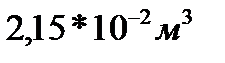
2. 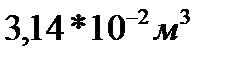
3. 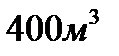
4. 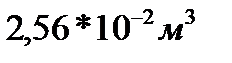
5. 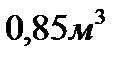
291. Сила сопротивления 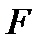 , действующая со стороны потока жидкости на медленно движущийся в ней шарик равна:
, действующая со стороны потока жидкости на медленно движущийся в ней шарик равна:
1. 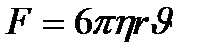
2. 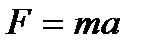
3. 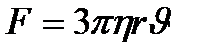
4. 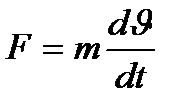
5. 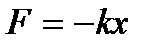
292. Явление переноса возникает в термодинамических системах, находящихся ….
1. в неравновесном состоянии
2. в любом состоянии
3. в равновесном состоянии
4.ответ на вопрос зависит от того, какая физическая величина переносится
5. в движении
293. Коэффициент теплопроводности численно равен…
1. количеству тепла, перенесенного в единицу времени через единичную площадку при единичном значении градиента температуры
2. количеству теплоты, перенесенному через единичную площадку
3. количеству тепла, перенесенного в единицу времени
4. количеству теплоты, перенесенному в единицу времени при единичном значении градиента температуры
5. единице
294. Эффективный диаметр молекул – это ..
1. расстояние, на которое сближаются центры молекул при столкновении
2. расстояние, пройденное молекулой между двумя столкновениями
3. расстояние, пройденное молекулой за 1 секунду
4. не характеристика для молекулы
5. среднее расстояние между молекулами, участвующими в тепловом движении
295. Уравнением диффузии является: (S –произвольная площадка)
1. 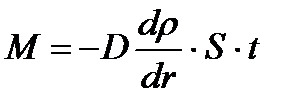
2. 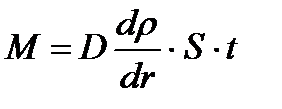
3. 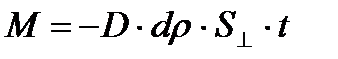
4. 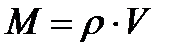
5. 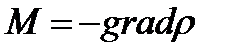
296. Теплопроводность может происходить в газе, если имеется отличный от нуля..
1. градиент температуры
2. градиент скорости направленного движения газа
3. градиент плотности вещества
4. градиент концентрации молекул газа
5. если нет никаких градиентов физических величин
297. Сила внутреннего трения равна:
1. 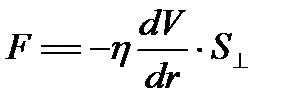
2. 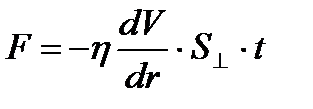
3. 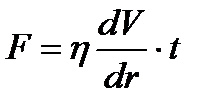
4. 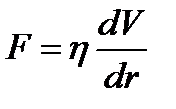
5. 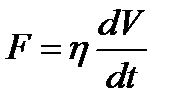
298. Холодильная машина:
1. забирает тепло из рабочего объема и рассеивает его в окружающем пространстве
2. производит холод
3. превращает тепло в холод
4. рассеивает тепло
5. холодильная машина является разновидностью тепловой машины
299. Коэффициент диффузии Д водородa при нормальных условиях, если средняя длина свободного пробега  равен:
равен:
1. 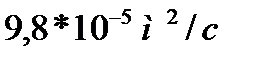
2. 
3. 
4. 
5. 
300 . При изобарном нагревании некоторой массы кислорода  на
на 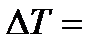
 совершена работа
совершена работа  по увеличению его объем1. Молярная масса кислорода и универсальная газовая постоянная равны соответственно:
по увеличению его объем1. Молярная масса кислорода и универсальная газовая постоянная равны соответственно: 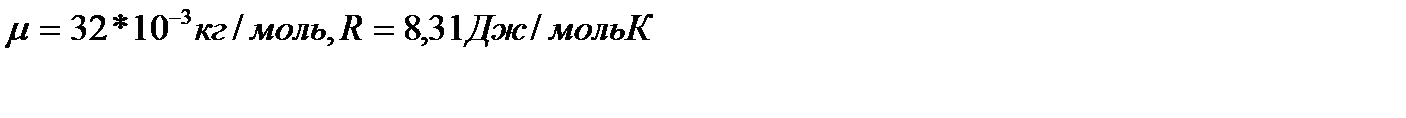 Масса кислорода равна:
Масса кислорода равна:
1. 0,481 кг
2. 0,520 кг
3. 0,491кг
4. 0,90 кг
5. 8,1 кг
301. Газ изобарно увеличился в объеме в три раза при давлении  . На увеличение его объема потребовалось совершить работу в
. На увеличение его объема потребовалось совершить работу в  . Первоначальный объем газа равен:
. Первоначальный объем газа равен:
1. 
2. 
3 
4. 
5. 
302. Сила сопротивления 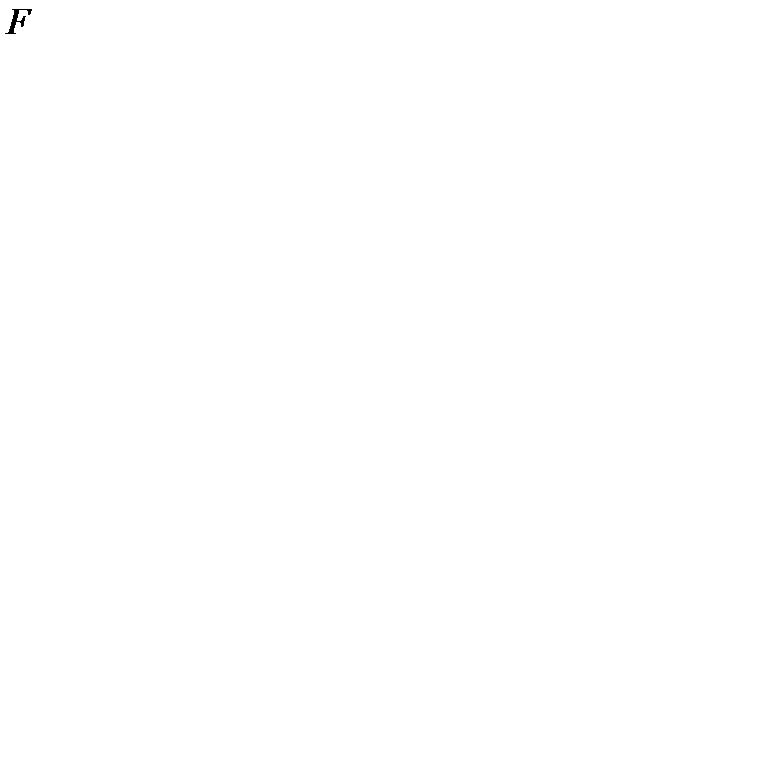 , действующая со стороны потока жидкости на медленно движущийся в ней шарик равна:
, действующая со стороны потока жидкости на медленно движущийся в ней шарик равна:
1. 
2. 
3. 
4. 
5. 
303. Явление переноса возникает в термодинамических системах, находящихся ….
1. в неравновесном состоянии
2. в любом состоянии
3. в равновесном состоянии
4. ответ на вопрос зависит от того, какая физическая величина переносится
5. в состоянии затвердевании
304. Уравнение теплопроводности численно равен…
1. количеству тепла, перенесенного в единицу времени через единичную площадку при единичном значении градиента температуры
2. количеству теплоты, перенесенному через единичную площадку
3. количеству тепла, перенесенного в единицу времени
4. количеству теплоты, перенесенному в единицу времени при единичном значении градиента температуры
5. единице
305. Эффективный диаметр молекул – это …
1. расстояние, на которое сближаются центры молекул при столкновении
2. расстояние, пройденное молекулой между двумя столкновениями
3. расстояние, пройденное молекулой за 1 секунду
4. не характеристика для молекулы
5. среднее расстояние между молекулами, участвующими в тепловом движении
306. Уравнением диффузии является: (S –произвольная площадка)
1. 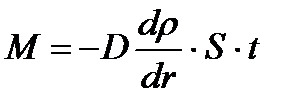
2. 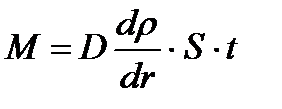
3. 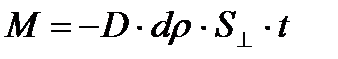
4. 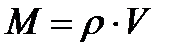
5. 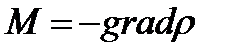
307. Теплопроводность может происходить в газе, если имеется отличный от нуля..
1. градиент температуры
2. градиент плотности вещества
3. градиент скорости направленного движения газа
4. градиент концентрации молекул газа
5. если нет никаких градиентов физических величин
308. Сила внутреннего трения равна:
1. 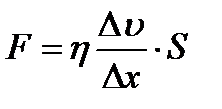
2. 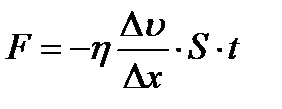
3. 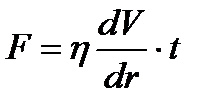
4. 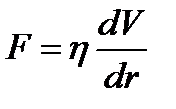
5. 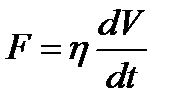
309. Изменение внутренней энергии зависит …
1. никак не зависит от вида процесса и определяется начальным и конечным состояниями газа
2. от вида процесса, совершаемого газом
3. от изменения объема, занимаемого газом
4. от вида функции P= f(V)
5. от вида теплообмена
310. Схема теплового двигателя представлена на рисунке:
| нагреватель |
| Рабочее тело |
| холодильник |
| нагреватель |
| Рабочее тело |
| нагреватель |
| Рабочее тело |
| холодильник |
1. рис.3
2. рис.1 и 2
3. рис.1
4. рис.2
5. рис. 1 и 3
311. Идеальная тепловая машина 30% тепла, полученного от нагревателя, отдает холодильнику. Найти температуру холодильника, если температура нагревателя равна 270 С.
1. 210 К
2. –183о С
3. 292 К
4. 483 К
5. 281 К
312. Цикл Карно изображен на рисунке …
1) P 2) S 3) P
1. рис.1
2. рис.2
3. рис.3
4. рис. 1 и 3
5. рис. 1 и 2
313. Процесс диффузии (перенос массы) состоится, если в газе имеется…
1. градиент плотности
2. градиент температуры
3. градиент скорости
4. градиент импульса
5. переноса массы в газе не может происходить
314. Укажите определение внутренней энергии идеального газа.
1. ФВЧР кинетической энергии хаотического движения молекул.
2. Физическая величина, численно равная (ФВЧР) произведению давления газа на изменение его объема при изобарическом процессе.
3. ФВЧР произведению изменения объема на давление при изохорическом процессе.
4. ФВЧР количеству теплоты для нагревания одного моля вещества на один кельвин.
5. ФВЧР потенциальной энергии взаимодействия молекул.
315 . Укажите определение работы газа при его изобарическом расширении.
1. Физическая величина, численно равная (ФВЧР) произведению давления газа на изменение его объема при изобарическом процессе.
2. ФВЧР произведению изменения объема на давление при изохорическом процессе.
3. ФВЧР количеству теплоты для нагревания одного моля вещества на один кельвин.
4. ФВЧР потенциальной энергии взаимодействия молекул.
5. ФВЧР кинетической энергии хаотического движения молекул.
316. Укажите метод определения отношения теплоемкостей при постоянном давлении к теплоемкости при постоянном объеме.
1. Метод Клемана-Дезорма.
2. Метод Стокса.
3. В опытах Перрена
4. В опытах Ньютона.
5. Методом Фурье
317. Укажите метод определения вязкости жидкостей.
1. Метод Стокса.
2. Метод Клемана-Дезорма.
3. В опытах Перрена.
4. В опытах Ньютона.
5. Методом Фурье
318. Какие процессы используются в методе Клемана-Дезорма при определении отношения теплоемкостей газов?
1. изохорный и адиабатный.
2. Изохорический и изобарический.
3. Изохорический и изотермический.
4. Изобарный и адиабатный
5. Изобарный и изотермический
319. Укажите формулировку первого начала термодинамики.
1. Сообщенное системе количество теплоты идет на совершение работы против внешних сил и изменение внутренней энергии системы.
2. Невозможен вечный двигатель второго рода.
3. Необратимые процессы в замкнутых системах происходят с возрастанием энтропии.
4. В замкнутом цикле Карно процессы происходят при постоянной энтропии.
5. Невозможен процесс самопроизвольной передачи тепла от холодного тела к горячему.
320. Укажите формулировку второго начала термодинамики.
1. Невозможен вечный двигатель второго рода.
2. Невозможен вечный двигатель первого рода.
3. В замкнутом цикле Карно процессы происходя при постоянной энтропии.
4. При совершении работы над системой возможен переход тепла от холодного тела к горячему.
5. В незамкнутых системах энтропия может как возрастать, так и уменьшаться
321. Укажите определение удельной теплоемкости вещества.
1. ФВЧР количеству теплоты для нагревания 1 кг вещества на 1 К
2. Физическая величина, численно равная (ФВЧР) количеству теплоты для нагревания одного моля газа на 1 К.
3. ФВЧР количеству тепла для изменения температуры единицы массы вещества на 1 К
4. ФВЧР количеству теплоты для плавления единицы массы вещества
5. ФВЧР количеству теплоты для парообразования единицы массы вещества.
322. Укажите переносимое свойство в явлении диффузии.
1. Масса молекул.
2. Импульс молекул.
3. Кинетическая энергия.
4. Скорость хаотического движения молекул.
5. Потенциальная энергия
323. Как изменяется энтропия при смешивании горячей и холодной воды?
1. Увеличивается.
2. Уменьшается.
3. Не изменяется
4. Увеличивается, если количество горячей воды больше количества холодной воды
5. Уменьшается, если количество горячей воды больше количества холодной воды.
324. Укажите уравнение адиабатического процесса.
1. Пуассона.
2. Бойля-Мариотта
3. Гей-Люссака.
4. Шарля
5. Ньютона
325. Укажите название отношения теплоты, полученной телом в изотермическом процессе, к температуре тела.
1. Приведенная теплота.
2. Энтропия.
3. Внутренняя энергия.
4. Работа.
5. Теплоемкость.
326. Укажите определение обратимого процесса.
1. Процесс происходящий как в прямом, так и в обратном направлении без изменений в окружающей среде.
2. Процесс, при котором система, пройдя через ряд состояний, возвращается в исходное.
3. Замкнутый цикл, протекающий по часовой стрелке при изображении на диаграмме.
4. Любой неравновесный процесс.
5. Процесс при постоянной температуре.
327. Газ переходит из одного и того же начального состояния в одно и то же конечное состояние в результате разных процессов: а)изобарного, б)последовательных изохорного и изотермического. В каком процессе работа расширения максимальна?
1. В процессе а)
2. В процессе б)
3. Работы одинаковы.
4. Нельзя определить.
5. Процессы неосуществимы.
328. Температура газа в цилиндре постоянна. Каково соотношение между сообщенным количеством теплоты и совершенной работой?
1. Количество теплоты равно совершенной работе.
2. Количество теплоты равно сумме работы и изменения внутренней энергии.
3. Количество теплоты равно разности изменения внутренней энергии и работы.
4. Количество теплоты равно разности работы и внутренней энергии.
5. Работа совершается не за счет теплоты, а за счет изменения внутренней энергии.
329. Какую работу совершает 1 моль идеального газа при нагревании на 1 К при постоянном объеме?
A. Работа не совершается.
B. 8,31 Дж\моль К
C. 1,38*10-23 Дж\K
D. Зависит от изменения объема.
E. Зависит от теплоемкости.
330. Какую работу совершает моль идеального газа при нагревании на 1 К при постоянном давлении?
1. 8,31 Дж
2. 1,38*10-23 Дж
3. Зависит от изменения объема.
4. Зависит от теплоемкости.
5. Работа не совершается.
331. От чего зависит внутренняя энергия идеального газа?
1. От температуры газа.
2. От сорта молекул и взаимодействия между ними.
3. От внешних условий.
4. От процесса.
5. От энтропии.
332. Укажите правильное соотношение между работой и теплотой.
1. Работа совершается при направленном движении макротела, а количество теплоты изменяет хаотическое движение микрочастиц и энергию.
2. Различия между ними нет, так как это – две формы изменения внутренней энергии.
3. Работа зависит от процесса.
4. Количество теплоты зависит от процесса.
5. Количество теплоты зависит от работы и изменения внутренней энергии.
Молекулярная физика 2. (Термодинамика)
333. Какой участок цикла Карно описывает адиабатический процесс?
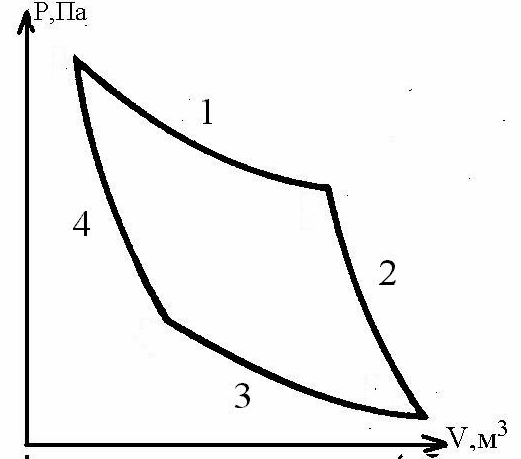
1. 2 и 4
2. 1 и 2
3. 3
4. 1
5. 1 и 3
334. Чему равна работа, совершаемая газом при переходе из состояния 1 в 2?
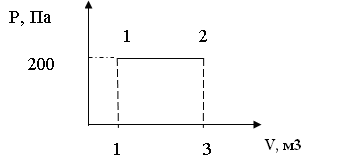
1. 400 Дж
2. 600 Дж
3. 200 Дж
4. 200 Дж
5. 0 Дж
335. Какой участок цикла Карно описывает изотермический процесс?
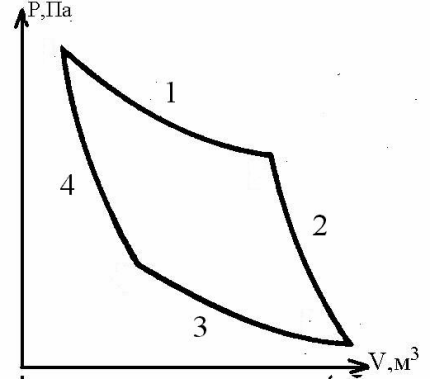
1. 1 и 3
2. 2
3. 2 и 4
4. 4
5. 4 и 3
336. Укажите формулу, выражающую первый закон термодинамики.
1. 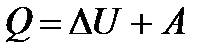
2. 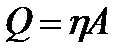
3. 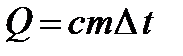
4. 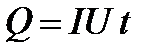
5. 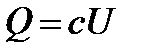
337. При изотермическом расширении идеальный газ совершает работу
А=20 Дж. На сколько изменится внутренняя энергия газа?
1. 0 Дж
2. 10 Дж
3. 20 Дж
4. 15 Дж
5. 5 Дж
338. Чему равна работа, совершенная газом при переходе из состояния 1 в состояние 2?
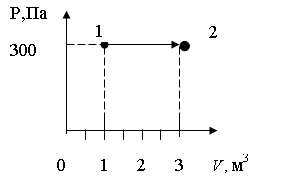
1. 600 Дж
2. 200 Дж
3. 300 Дж
4. 0 Дж
5. 900 Дж
339. Укажите первый закон термодинамики для изохорного процесса.
1. 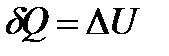
2. 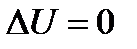
3. 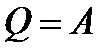
4. 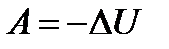
5. 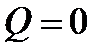
340. Диаграмма какого процесса изображена на рисунке?
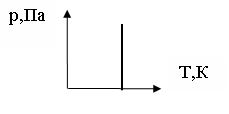
1. изотермы.
2. адиабаты.
3. изобары.
4. изохоры.
5. политропы.
341. В ходе цикла Карно рабочее вещество получает от нагревателя тепло 300 кДж. Температура нагревателя 450 К, температура холодильника 270 К. Определить полезную работу за один цикл.
1. 120 кДж
2. 90 кДж
3. 180 кДж
4. 240 кДж
5. 300 кДж
342. В диаграмме 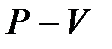 цикл Карно состоит из…
цикл Карно состоит из…
1. двух изотерм и двух адиабат
2. двух изохор и двух изотерм
3. двух изохор и двух адиабат
4. двух адиабат и двух изобар
5. двух изобар и двух изотерм
343. Что определяет второе начало термодинамики?
1. направление процессов в природе
2. закон сохранения импульса
3. закон сохранения массы
4. закон сохранения энергии
5. направление движения молекул газа при постоянной температуре
344. Как изменяется энтропия в необратимых процессах?
1. только возрастает
2. только убывает
3. остается неизменной
4. может возрастать или убывать
5. может убывать или оставаться постоянной
345. Каким процессам соответствуют графики 1-2, 2-3, 3-1?
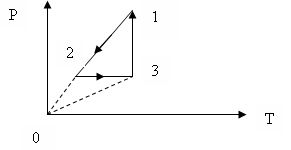
1. изохорный, изобарный, изотермический
2. изобарный, изохорный, изотермический
3. изотермический, изобарный, изохорный
4. изохорный, изотермический, изобарный
5. не соответствует никаким процессам
