Константы диссоциации некоторых слабых кислот и оснований 6 страница
192. Определить, сколько граммов глицерина надо добавить к 100 г воды, чтобы получившийся раствор не замерзал до температуры –3,2 °С.
193. При какой температуре начнется кристаллизация воды из раствора хлорида калия концентрацией 3 %, если кажущаяся степень диссоциации 89 %?
194. Определить кажущуюся степень диссоциации сульфата магния в его 0,1 н. растворе плотностью 1,02 г/см3, если этот раствор начинает кристаллизоваться при температуре –0,153 °С.
195. При какой температуре начнет кристаллизоваться раствор сульфата железа (II) концентрацией 2 %, если его температура кипения 100,136 °С?
196. При какой температуре закипит раствор глицерина в воде, если он кристаллизуется при температуре –1,5 °С?
197. Кажущаяся степень диссоциации некоторой соли, диссоциирующей на три иона, составляет 97 %. Определить, при какой температуре начнет кристаллизоваться раствор этой соли в воде, если он закипает при температуре 100,2 °С.
198. Относительное понижение давления паров воды над раствором сульфата калия концентрацией 3 % составляет 9,23×10-3. Определить, при какой температуре начнется кристаллизация воды из этого раствора.
199. Раствор хлорида калия в воде концентрацией 0,8 % и плотностью 1,02 г/см3 при температуре 27 °С имеет осмотическое давление 5,13×105 Па. Определить, при какой температуре начнется кристаллизация этого раствора.
200. Температура кристаллизации бензола +5,5 °С, а раствора, содержащего 0,2242 г камфары в 30,55 г бензола, +5,254 °С. Определить молярную массу камфары, если константа кристаллизации бензола 5,16 K×кг/моль.
201. Раствор некоторого органического вещества в этиловом спирте закипает при температуре 78,41 °С. Определить его молярную массу, если для приготовления раствора было взято 2 г этого вещества, 48 г этилового спирта, температура кипения которого 78,3 °С, Kэб = 1,19 К×кг/моль.
202. Сколько граммов хлористого натрия надо добавить к 100 г воды, чтобы получившийся раствор не замерзал до температуры –1,8 °С? Считать, что соль диссоциировала на 100 %.
203. Сколько сахара С12Н22О11 надо растворить в 200 г воды, чтобы полученный раствор кипел при температуре 100,3 °С?
204. Сколько граммов хлорида бария, диссоциирующего нацело, надо растворить в 1 л воды, чтобы получившийся раствор замерзал при температуре –3,2 °С?
205. Осмотическое давление раствора глицерина в воде при температуре 7 °С составляет 5,3×105 Па. Определить при какой температуре закипит этот раствор, если его плотность 1,02 г/см3.
206. Определить степень диссоциации бензойной кислоты С6Н5СООН, если раствор ее в бензоле кристаллизуется при температуре 5,32 °С. Температура кристаллизации индивидуального бензола 5,5 °С, Kкр = 5,16 К×кг/моль, а для приготовления раствора взято 62,5 г бензола и 0,26 г бензойной кислоты.
207. Определить молярную массу бензойной кислоты, если известно, что ее раствор в бензоле кристаллизуется при температуре 5,18 °С. Для бензола Ткрист = 5,5 °С, Kкр = 5,16 К×кг×моль, а для приготовления раствора взято 100 г бензола и 0,757 г бензойной кислоты. Считать, что в растворе кислота практически не диссоциирована.
208. При какой температуре закипит раствор иодида калия в воде, если для его приготовления взято 300 мл воды и 1,33 г соли, кажущаяся степень диссоциации 98 %?
209. Относительное понижение давления паров воды над раствором некоторой соли составляет 1 %. Определить, при какой температуре закипит этот раствор.
210. Относительное понижение давления паров над раствором некоторого сильного электролита в воде составляет 1,5 %. Определить, при какой температуре начнется кристаллизация этого раствора.
211. Раствор, в 100 мл которого находится 2,3 г вещества, обладает при 298 К осмотическим давлением, равным 618,5 кПа. Определить молярную массу вещества.
212. В 1 мл раствора содержится 1018 молекул растворенного неэлектролита. Вычислить осмотическое давление раствора при 298 К.
213. В каком отношении должны находиться массы воды и этилового спирта, чтобы при их смешении получить раствор, замерзающий при -20 °С?
214. При 25 °С осмотическое давление некоторого водного раствора 1,24 МПа. Вычислить осмотическое давление раствора при 0 °С.
4.3. Водородный показатель
Для характеристики кислотно-основных свойств растворов используют водородный показатель рН, равный отрицательному значению десятичного логарифма концентрации ионов водорода. Аналогично рассчитывают гидроксильный показатель рОН, равный отрицательному значению десятичного логарифма концентрации ионов гидроксила:
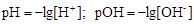 . (4.13)
. (4.13)
Концентрации ионов водорода и гидроксила связаны между собой равновесием диссоциации воды:
Н2О Û Н+ + ОН-.
Константу равновесия называют ионным произведением воды. При 298 К константа равновесия
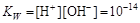 .
.
Прологарифмировав это уравнение, получим
рН + рОН = 14.
В чистой воде (нейтральная среда) рН = рОН = 7. В кислой среде рН < 7, в щелочной среде рН > 7.
Расчет рН в растворах сильных кислот и оснований. Для сильных кислот и щелочей, полностью диссоциированных на ионы,
[Н+] = zCк и [ОН-] = zCщ,
где Ск и Сщ - моляльные концентрации кислоты и щелочи соответственно; z - основность кислоты или кислотность основания.
Разбавление раствора сильного электролита учитывают в кислой и щелочной среде соответственно по уравнениям
рН2 = рН1 + lgn,
рН2 = рН1 – lgn,
где индекс 1 относится к исходному раствору (до разбавления), индекс 2 – к конечному раствору (после разбавления).
В среде, близкой к нейтральной, необходимо принять во внимание диссоциацию воды, в результате которой образуются ионы Н+иОН-.
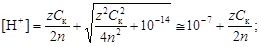 (4.14)
(4.14)
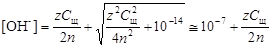 .
.
При смешивании растворов сильных кислот и оснований возможны два варианта:
· если смешивают два кислых или два щелочных раствора, т.е. рН1 < 7 и рН2 < 7 или рН2 > 7ирН2 > 7, то
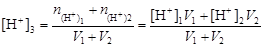 ; (4.15)
; (4.15)
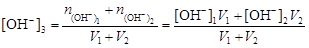 .
.
· если смешивают кислый и щелочной растворы, т.е. рН1 < 7 и рН2 > 7, то конечную концентрацию раствора рассчитывают по веществу, взятому в избытке. При избытке кислоты
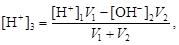
при избытке щелочи
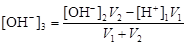 .
.
Расчет рН в растворах слабых кислот и оснований. Диссоциация многих электролитов протекает не полностью. Отношение числа диссоциированных молей к общему числу молей электролита в растворе называют степенью диссоциации. Для его количественного описания используют константу равновесия, называемую константой диссоциации. Для одноосновной кислоты, диссоциирующей по уравнению, НАn Û Н+ + Аn-, где Аn – кислотный остаток, константа диссоциации
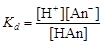 . (4.16)
. (4.16)
Так как [An–] = [H+] и [НAn] = C, то
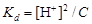 ;
;
(4.17)
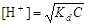 ,
,
где С – концентрация слабой кислоты, моль/л.
Для растворов слабых оснований
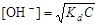 , (4.18)
, (4.18)
где С – концентрация слабого основания, моль/л.
По значению константы диссоциации можно рассчитать степень диссоциации слабого электролита:
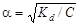 .
.
Многоосновные кислоты диссоциируют ступенчато, например: Н2S Û НS- + Н+(1-я ступень); НS- Û S2- + Н+ (2-я ступень).
При расчетах рН обычно учитывают только первую ступень диссоциации, пренебрегая второй и третьей ступенями. Таким образом, уравнения (4.16) и (4.18) справедливы и для многоосновных кислот при использовании первой константы диссоциации Kd1.
Константы диссоциации некоторых слабых кислот и оснований даны в прил.1.
Пример 10. Вычислить рН раствора серной кислоты концентрацией 0,3 % (d = 1,0 г/см3).
Решение. 1. Перейдем к моляльной концентрации серной кислоты. Для этого выделим мысленно 100 г раствора, тогда масса серной кислоты составит 0,3 г, а масса воды – 99,7 г. По уравнению (4.4) вычислим моляльную концентрацию:
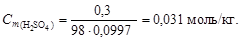
2. Согласно уравнению диссоциации H2SO4 ® 2H+ + SO42-, из 1 моль серной кислоты образуется 2 моль H+, следовательно, 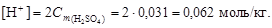
3. По уравнению (4.13) вычислим рН = –lg[H+] = –lg0,062 = = 1,21.
Пример 11. Вычислить рН раствора гидроксида бария концентрацией 0,0068 экв/л.
Решение. 1. По уравнению диссоциации Ba(OH)2 ® Ba2+ + + 2 OH- из 1 моль гидроксида бария образуется 2 моль гидроксил-ионов:
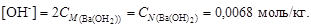
2. По уравнению (4.13) найдем рOН = –lg[OH-] = –lg0,0068 = = 2,17 и вычислим рН = 14 - рОН = 14 – 2,17 = 11,83.
Пример 12. Определить рН, если раствор одноосновной кислоты с рН = 5,5 разбавлен в 100 раз.
Решение. По уравнению (4.14) найдем концентрацию ионов водорода в конечном растворе
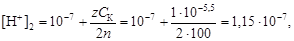
и вычислим
рН2 = –lg[H+]2 = –lg1,15×10-7 = 6,9.
Пример 13. Определить значение рН при смешении 10 л раствора с рН1 = 2 и 17 л раствора с рН2 = 4.
Решение. По уравнению (4.15) найдем концентрацию ионов водорода в конечном растворе
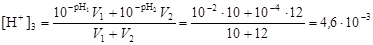
и вычислим рН3 = –lg[H+]3 = –lg(4,6×10-3) = 2,33.
Пример 14. Смешали 250 мл раствора с рН = 3 и 300 мл раствора гидроксида калия концентрацией 0,001 моль/л. Определить рН полученной смеси.
Решение. Обозначим объемы смешиваемых растворов V1 и V2 соответственно. Найдем число молей OH-:
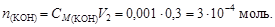
Согласно уравнению диссоциации KOH ® K+ + OH-, 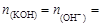
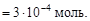
Найдем число молей H+:
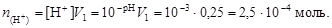
Очевидно, что в избытке находятся гидроксил-ионы. Их остаточную концентрацию в полученном растворе найдем по уравнению
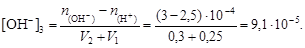
Вычислим
рН3 = 14 + lg[OH-]3 = 14 + lg(9,1×10-5) = 9,96.
Пример 15. Найти рН раствора борной кислоты с мольной долей 0,0025 (dр-р = 1,0 г/см3).
Решение. 1. выделим мысленно 1 кг раствора. Запишем
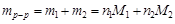 ,
,
где индекс 1 относится к растворителю, т.е. к воде, а индекс 2 – к растворенному веществу, т.е. к H3BO3. Так как M1 = 18 г/моль, М2 = 61,8 г/моль и
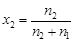 Þ
Þ 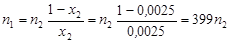 ,
,
то
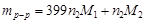 .
.
Вычислим
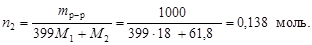
2. Так как плотность раствора 1 г/см3, то его объем соответствует 1 л, и молярная концентрация численно равна количеству вещества борной кислоты, т.е. СМ(Н3ВО3) = 0,138 моль/л.
3. Диссоциация борной кислоты по первой ступени протекает по реакции H3BO3 ® H+ + H2BO3-, для которой константа диссоциации Kd1 = 7,1×10-10. Второй и третьей ступенями диссоциации борной кислоты пренебрегаем.
4. В соответствии с уравнениями (4.17) и (4.13) вычислим
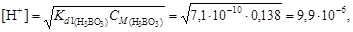
рН = –lg[H+] = –lg(9,9×10-6) = 5.
Пример 16. Сколько граммов бутиламина содержится в 1 л его раствора, имеющего рН = 11,5?
Решение. Гидрат бутиламина диссоциирует как основание по уравнению C4H9NH2×H2O Û C4H9NH3+ + OH-. Константа диссоциации Kd=4,57×10-4, pKd = 3,340, гидроксильный показатель рОН = 14 – рН = 2,5.
По формуле (4.18) найдем молярную концентрацию бутиламина
lgCМ = pKd – 2pOH = 3,34 – 2×2,5 = –1,66;
CМ = 10-1,66 = 0,022 моль/л.
Масса бутиламина, содержащаяся в 1 л раствора, Сг/л = CМM, где М – молярная масса бутиламина 73 г/моль. Тогда Сг/л =0,022×73 = 1,6 г/л.
Задание IV. Определить pH предложенного раствора сильного электролита (табл.4.2).
Таблица 4.2
| Номер задачи | Электролит | Концентрация раствора | Плотность раствора, г/см3 |
| Сa(OH)2 | 0,07 % | 1,00 | |
| Ba(OH)2 | 0,5 % | 1,003 | |
| H2SO4 | 0,01 мол. % | 1,0 | |
| Sr(OH)2 | 5×10-4 н. | 1,0 | |
| HCl | 1,36 % | 1,005 | |
| H2SO4 | 1,73 % | 1,012 | |
| KOH | 0,577 % | 1,003 | |
| H2SO4 | 5×10-4 М | 1,0 | |
| KOH | 0,001 н. | 1,0 | |
| HClO4 | 0,25 М | 1,013 | |
| NaOH | 2,5×10-3 М | 1,0 | |
| HCl | 1,0 % | 1,003 | |
| HNO3 | 3 % | 1,01 | |
| Ba(OH)2 | 5 % | 1,04 | |
| HCl | 0,3 % | 1,0 | |
| KOH | 5,8 г/л | 1,004 | |
| H2SO4 | 0,05 г/л | 1,0 | |
| KOH | 0,6 г/л | 1,0 | |
| Ba(OH)2 | 0,1 М | 1,02 | |
| H2SO4 | 0,1 н. | 1,0 | |
| H2SO4 | 0,5 % | 1,0 | |
| NaOH | 0,5 % | 1,0 | |
| HCl | 0,01 н. | 1,0 | |
| Сa(OH)2 | 0,02 н. | 1,0 | |
| KOH | 4 г/л | 1,0 | |
| NaOH | 5 г/л | 1,0 | |
| H2SO4 | 0,005 М | 1,0 | |
| HCl | 0,006 М | 1,0 | |
| LiOH | 0,8 г/л | 1,0 | |
| NaOH | 0,1 г/л | 1,0 | |
| RbOH | 1 % | 1,0 | |
| CsOH | 0,5 % | 1,0 | |
| HCl | 0,02 мол. % | 1,0 | |
| H2SO4 | 0,6 % | 1,003 | |
| HNO3 | 0,7 мол. % | 1,0 | |
| HClO4 | 0,08 мол. % | 1,0 | |
| H2SO4 | 0,3 % | 1,001 | |
| Окончание табл.4.2 | |||
| Номер задачи | Электролит | Концентрация раствора | Плотность раствора, г/см3 |
| HNO3 | 0,05 г/л | 1,0 | |
| HNO3 | 0,6 г/л | 1,0 | |
| H2SO4 | 0,03 н. | 1,0 | |
| Сa(OH)2 | 0,03 % | 1,00 | |
| Sr(OH)2 | 0,3 % | 1,001 | |
| Ba(OH)2 | 0,05 г/л | 1,0 | |
| HCl | 0,2 % | 1,0 | |
| H2SO4 | 0,0012 М | 1,0 | |
| HNO3 | 0,06 г/л | 1,0 | |
| Ba(OH)2 | 0,1 г/л | 1,0 | |
| Sr(OH)2 | 0,02 н. | 1,0 | |
| Сa(OH)2 | 0,09 г/л | 1,0 | |
| CsOH | 0,5 % | 1,002 |
Задание V. Определить pH следующих растворов.
265. Раствор гидроксида бария концентрацией 0,1 моль/л, если к 1 л этого раствора добавили 7,1 г гидроксида натрия.
266. Раствор серной кислоты концентрацией 0,1 моль/л, если к 1 л этого раствора добавили 7,1 г гидроксида бария.
267. Раствор после выщелачивания боксита по следующим данным: масса руды 1 т; ω(Al2O3∙Н2O) = 80 %; V(NaOH) = 3,1 м3; ω(NaOH) = 15 %.
268. 10-процентный раствор соляной кислоты (d = 1,047 г/мл) при условии, что к 20 л этого раствора прибавили 5 м3 воды, содержащей гидроксид кальция концентрацией 0,02 экв/л.
269. Раствор, содержащий 4 г KOH и 5 г NaOH в 1 л воды.
270. Раствор, содержащий 0,005 моль/л серной кислоты и 0,006 моль/л соляной кислоты.
271. Раствор после выщелачивания по реакции Li2O∙Al2O3∙4SiO2 + H2SO4 → Li2SO4 + Al2O3∙4SiO2∙H2O↓, если масса руды 1 т, w(Li2O∙Al2O3∙4SiO2) = 70 %; V(H2SO4) = 4 м3; w(H2SO4) = = 5 %, d = 1,032 г/мл.
272. Раствор после выщелачивания руды, если масса руды 1 т, в руде содержится 6 % Cu4(SO4)(OH)6; w(H2SO4) = 3 %, d = 1,03 г/мл, V(H2SO4) = 3 м3.
273. Раствор, полученный при разбавлении 20 л 10 % соляной кислоты (d = 1,047 г/мл) пятью кубометрами воды.
274. Рассчитать рН раствора азотнокислых стоков, если 10 л 5-процентной азотной кислоты сброшены в резервуар емкостью 5 м3.
275. Раствор соляной кислоты, если к 100 мл этого раствора, содержащего 5 мг HCl, прибавили 5 мг нитрата свинца (II).
276. Раствор объемом 10 м3, содержащий по 50 г серной и дихромовой кислот.
277. Щелочные стоки объемом 5 л, содержащие 2 мэкв щелочи.
278. Раствор дихромовой кислоты, если в нем содержится 2 мг/мл Cr (VI).
Задание VI. Определить pH и степень диссоциации предложенного раствора слабого электролита при температуре 25 °С (табл.4.3.)
Таблица 4.3
| Номер задачи | Электролит | Концентрация раствора | Плотность раствора, г/см3 |
| NH4OH | 2 % | 0,989 | |
| CH3COOH | 0,12 % | 1,0 | |
| HCOOH | 4,5 % | 1,01 | |
| CH3COOH | 2 % | 1,001 | |
| NH4OH | 2,35 % | 0,988 | |
| C6H5NH3OH | 93,02 г/л | - | |
| N2H5OH | 5 % | 1,01 | |
| C6H5OH | 5 % | 1,02 | |
| HCOOH | 0,5 % | - | |
| CH3COOH | 0,65 % | - | |
| HNO2 | 0,8 % | - | |
| HCN | 2,7 % | 1,01 | |
| C6H5OH | 9,4 г/л | - | |
| NH4OH | 0,1 % | - | |
| HCN | 8 % | 1,04 | |
| HCOOH | 2,3 % | 1,005 | |
| CH3COOH | 1 % | - |
Окончание табл.4.3
| Номер задачи | Электролит | Концентрация раствора | Плотность раствора, г/см3 |
| NH4OH | 0,34 % | 1,0 | |
| HCOOH | 3 % | 1,007 | |
| H2S | 0,32 н. | - | |
| NH4OH | 0,5 % | 1,0 | |
| H3PO4 | 1 % | 1,005 | |
| C9H7NHOH | 3 г/л | - | |
| Лимонная кислота | 120 г/л | - | |
| Бензойная кислота | 2 % | 1,003 | |
| N2H5OH | 0,5 % | - | |
| HCOOH | 4 % | 1,01 | |
| C6H5NH3OH | 0,56 г/л | - | |
| CH3NH3OH | 24,5 г/л | - | |
| C3H7NH3OH | 23,1 г/л | - | |
| C4H9NH3OH | 13,65 г/л | - | |
| C5H5NHOH | 1 г/л | - | |
| C2H5NH3OH | 0,5 г/л | - | |
| HNO2 | 2 % | 1,01 | |
| Винная кислота | 1 % | 1,02 | |
| H3BO3 | 5 % | 1,03 | |
| HBrO | 0,1 % | 1,0 | |
| H3BO3 | 10 % | 1,04 | |
| C6H5OH | 6,5 г/л | - | |
| H2S | 10 г/л | - | |
| H2CO3 | 8 % | 1,05 | |
| HF | 6 % | 1,03 | |
| C6H5СН2NH3OH | 5 г/л | - | |
| NH2OH×H2O | 6,2 г/л | - | |
| H3BO3 | 1,5 % | 1,01 | |
| (CH3)2NH2OH | 2 г/л | - | |
| (C2H5)2NH2OH | 2,8 г/л | - | |
| (CH3)3NНOH | 3 г/л | - | |
| C2H5ОNH3OH | 1,6 г/л | - | |
| CS(NH2)2×H2O | 20 г/л | - |
Задание VII. По заданному значению pH (табл.4.4) определить концентрацию предложенного раствора электролита при температуре 25 °С и выразить ее всеми возможными способами (считать, что плотность растворов 1 г/см3).
Таблица 4.4
| Номер задачи | Электролит | рН | Номер задачи | Электролит | рН |
| Сa(OH)2 | 11,0 | HClO4 | 2,35 | ||
| Сa(OH)2 | 11,8 | Ba(OH)2 | 13,8 | ||
| Ba(OH)2 | 12,8 | H2SO4 | 1,2 | ||
| KOH | 13,1 | HCl | 1,28 | ||
| H2SO4 | 1,95 | HNO3 | 3,1 | ||
| NaOH | 12,0 | KOH | 13,6 | ||
| Sr(OH)2 | 10,7 | HNO3 | 2,03 | ||
| H2SO4 | 2,2 | H2SO4 | 3,2 | ||
| HCl | 1,2 | H2SO4 | 1,5 | ||
| HCl | 2,8 | KOH | 12,03 | ||
| H2SO4 | 1,4 | Сa(OH)2 | 10,9 | ||
| LiOH | 12,5 | Ba(OH)2 | 13,3 | ||
| KOH | 13,0 | Sr(OH)2 | 10,7 | ||
| NaOH | 11,4 | H2SO4 | 1,9 | ||
| H2SO4 | 3,0 | Ba(OH)2 | 11,8 | ||
| RbOH | 13,0 | H2SO4 | 1,49 | ||
| KOH | 11,2 | HCl | 3,26 | ||
| CsOH | 12,5 | NaOH | 12,1 | ||
| HClO4 | 1,6 | H2SO4 | 2,6 | ||
| HCl | 1,95 | HCl | 2,3 | ||
| NaOH | 11,5 | HNO3 | 3,03 | ||
| H2SO4 | 1,91 | Сa(OH)2 | 11,4 | ||
| HCl | 1,56 | Ba(OH)2 | 11,1 | ||
| HNO3 | 1,41 | CsOH | 11,8 | ||
| HNO3 | 1,32 | Sr(OH)2 | 12,3 |
