Статистический характер второго закона термодинамики
Если первый закон т/д является абсолютным законом природы, то второй закон т/д - закон наибольшей вероятности или статистический. Это означает, что он выполняется с очень большой точностью для макросистем и тем менее применим, чем меньше размеры системы.
Каждая макросистема, находясь в определенном состоянии, может быть построена различными способами. Число способов построения системы называется термодинамической вероятностью системы (W).
И энтропия и т/д вероятность изолированной системы являются различными мерами в стремлении ее к равновесию. Обе величины возрастают в самопроизвольных неравновесных процессах, приближая систему к равновесию. Количественная связь между ними выражается уравнением Больцмана:
S = k ln W
k – константа Больцмана (k = R/Na = 1,38۰10-23 Дж/К)
Исходя из уравнения Больцмана можно вывести постулат Планка:
Правильный кристалл при 0К, когда прекращаются все движения, может быть построен одним единственным способом.
W = 1, тогда S = k ln 1 = 0 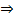 S = 0
S = 0
Вблизи абсолютного нуля не только теплоемкость, но и многие другие свойства тел (объем, давление насыщенного пара, плотность и др.) изменяются так, что их производная по температуре стремится к нулю. Этим объясняется принцип недостижимости абсолютного нуля, согласно которому никакие процессы не могут снизить температуру до 0 К.
Лекция №9.
Термодинамические потенциалы.
Энтропия позволяет предсказать возможность или невозможность самопроизвольного протекания процессов, но ее можно использовать только в изолированной системе. Для преодоления этой трудности начали искать критерии возможности протекания самопроизвольных процессов в более простых условиях. Например, для этого можно использовать работу, т.к. в самопроизвольных процессах она положительна, а в несамопроизвольных отрицательна, но работа в общем случае не является функцией состояния. Поэтому стали искать функции состояния, изменение которых можно выразить через работу. Было найдено несколько таких функций, которые называются термодинамическими потенциалами.
I. Изохорно-изотермический потенциал (свободная энергия Гельмгольца).
δQ = dU + δA
δA = δQ – dU 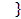 => δA ≤ TdS - dU
=> δA ≤ TdS - dU
dS ≥ 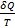
TdS≥δQ
В равновесном процессе δA = TdS – dU
В неравновесном δA < TdS – dU => δAравн > δAнеравн
Проинтегрируем выражение δAравн при Т=const
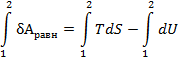
Amax = T(S2-S1) – (U2-U1) = TS2 – TS1 – U2 + U1 = (U1 – TS1) – (U2 – TS2)
U – TS = F => Amax = F1 – F2 = -ΔF
F – функция состояния, называемая изохорно-изотермическим потенциалом или свободной энергией Гельмгольца.
Т.о. Amax в равновесных процессах, протекающих при Т=const и V=const равна убыли изохорно-изотермического потенциала.
U = F + TS внутренняя энергия складывается из двух частей: свободной энергии (F) и связанной энергии (TS)
Только часть внутренней энергии (свободная – F) в изотермических процессах может превратиться в работу при равновесии, а в неравновесных процессах она частично или полностью переходит в теплоту. Связанная энергия всегда превращается в теплоту, т.к.
TdS = δQ
В неизотермических условиях (Т≠ const) такое деление провести нельзя.
Возьмем полный дифференциал от F = U – TS :
dF ≤ -PdV – SdT
В равновесном процессе: dF = -PdV – SdT
В неравновесном: dF < -PdV – SdT
При Т=const dF = -PdV
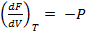 => свободная энергия F возрастает при уменьшении объема системы и уменьшается при его увеличении.
=> свободная энергия F возрастает при уменьшении объема системы и уменьшается при его увеличении.
V=const => dF = – SdT; 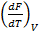 = - S => с уменьшением температурыF возрастает, а сростом убывает.
= - S => с уменьшением температурыF возрастает, а сростом убывает.
При одновременном V=const и Т=const
(dF)V,T ≤ 0 => F уменьшается в самопроизвольном неравновесном процессе при V=const и Т=const; т.к. dF < 0; в равновесии dF = 0 => F=const. А поскольку все неравновесные процессы (самопроизвольные) идут в сторону достижения равновесия и F в них уменьшается, то в состоянии равновесия она будет иметь постоянное и минимальное значение.
Т.о. условие равновесия запишется в виде:
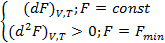
Все выводы справедливы, если А- работа расширения. В случае наличия других видов работы необходимо в последнее уравнение включать условия постоянства факторов, включающих другие виды работы.
II. Изобарно-изотермический потенциал.
Рассмотрим случай, когда в системе кроме работы расширения совершается работа химической реакции.
δA = PdV + δA’
δA’ – элементарная работа химической реакции .
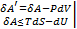 => δA’ ≤ TdS – dU - PdV
=> δA’ ≤ TdS – dU - PdV
В момент равновесия: δA’ = TdS – dU – PdV
Интегрируем при Р = const и Т = const:
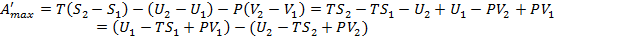
Обозначим G= U-TS+PV*–изобарно-изотермический потенциал (свободная энергия Гиббса).
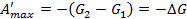
Максимальная работа химической реакции равна убыли изобарно-изотермического потенциала при Р = const и Т = const
G=U-TS=PV
F=U-TS => G = F + PV
H=U=PV G = H – TS
Продифференцировав уравнение (*) получим:
dG ≤ -SdT + VdP (**)
Возьмем частные производные от уравнения (**) в момент равновесия:
А) при Т= const => dG = VdP
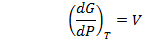
Б) при Р = const => dG = -SdT
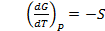
Следовательно свободная энергия Гиббса возрастает при уменьшении температуры и увеличении давления.
Условие равновесия Р = const и Т = const
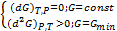 следовательно свободная энергия Гиббса убывает в самопроизвольных процессах протекающих при постоянных температуре и давлении и остается постоянной в равновесных процессах. В состоянии равновесия изобарный потенциал имеет постоянное и минимальное значение.
следовательно свободная энергия Гиббса убывает в самопроизвольных процессах протекающих при постоянных температуре и давлении и остается постоянной в равновесных процессах. В состоянии равновесия изобарный потенциал имеет постоянное и минимальное значение.
III. Изохорно-изэнтропный термодинамический потенциал.
Возьмем уравнения первого и второго законов термодинамики
δQ = δA + dU
dU = δQ – δA
dS ≥ 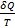 => δQ ≤ TdS следовательно dU ≤ TdS – PdV
=> δQ ≤ TdS следовательно dU ≤ TdS – PdV
(dU)S,V ≤ 0
Внутренняя энергия убывает в самопроизвольном неравновесном процессе при постоянстве S и V (dU<0) и остается постоянной в равновесных процессах (dU=0).
Следовательно, в состоянии равновесия внутренняя энергия имеет постоянное и минимальное значение.
Условие равновесия: 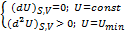
IV. Изобарно-изэнтропный термодинамический потенциал.
H = U + PV; U ≤ TdS - δA; A = PdV; dH = dU + PdV + VdP
Следовательно: dH ≤ TdS + VdP
При постоянных S и P: (dH)S,P ≤ 0
Энтальпия убывает в самопроизвольных неравновесных процессах, протекающих при Р = const и S = const и остается постоянной в равновесных процессах.
Т.о. в состоянии равновесия Энтальпия имеет постоянное и минимальное значение.
Условие равновесия: 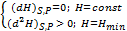
Внутренняя энергия и энтальпия в качестве критериев возможности протекания процессов используются гораздо реже чем свободная энергия Гельмгольца и свободная энергия Гиббса, т.к. их можно применять при условиях постоянства энтропии. Этот контроль весьма затруднен. В повседневной жизни используют термодинамические потенциалы, которые характеризуют процессы при более простых условиях.
Лекция № 10
