Лекция №7. Поверхностные явления. Адсорбция
До сих пор свойства гетерогенных систем описывались с помощью параметров и функций состояния, характеризующих каждую из фаз в целом. Однако свойства участка фазы, примыкающего к её поверхности, отличаются от свойств фазы в объеме: фактически частицы, находящиеся на поверхности каждой фазы, образуют особую поверхностную фазу, свойства которой существенно отличаются от свойств внутренних областей фазы. Частицы, расположенные на поверхности, находятся в другом окружении по сравнению с частицами, находящимися в объеме фазы, т.е. взаимодействуют как с однородными частицами, так и с частицами другого рода. Следствием этого является то, что средняя энергия gs частицы, находящейся на поверхности раздела фаз, отличается от средней энергии такой же частицы в объеме фазы gv (причем энергия частицы на поверхности может быть как больше, так и меньше энергии частицы в объеме).
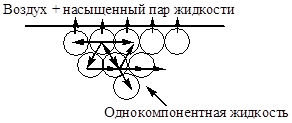
Поэтому важнейшей характеристикой поверхностной фазы является поверхностная энергия Gs – разность средней энергии частицы, находящейся на поверхности, и частицы, находящейся в объеме фазы, умноженная на число частиц на поверхности N:
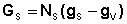 (1)
(1)
Очевидно, что общая величина поверхностной энергии фазы будет определяться величиной её поверхности S. Поэтому для характеристики поверхности раздела, отделяющей данную фазу от другой, вводится понятие поверхностное натяжение σ – отношение поверхностной энергии к площади поверхности раздела фаз; величина поверхностного натяжения зависит только от природы обеих фаз.
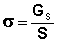 (2)
(2)
Как и поверхностная энергия фазы, поверхностное натяжение может иметь как положительное, так и отрицательное значение. Поверхностное натяжение положительно, если находящиеся на поверхности частицы взаимодействуют с частицами этой же фазы сильнее, чем с частицами другой фазы (и, следовательно, gs > gv). Согласно принципу минимума свободной энергии, любая фаза будет стремиться самопроизвольно уменьшить свою поверхностную энергию; поэтому в случае положительного поверхностного натяжения (σ > 0) фаза стремится уменьшить свою поверхность. В случае если σ < 0, поверхностная энергия фазы будет уменьшаться при увеличении площади поверхности.
На границе конденсированной (т.е. твердой или жидкой) фазы с газом поверхностное натяжение всегда положительно, поскольку частицы конденсированной фазы взаимодействуют друг с другом сильнее, чем с молекулами газа. Однако, состояние с избытком энергии неустойчиво. Поэтому в гетерогенных системах самопроизвольно протекают процессы, сопровождающиеся уменьшением свободной энергии. Процессы, которые приводят к изменению запаса энергии молекул, находящихся на поверхности фазы, называются поверхностными явлениями.
Примером такого самопроизвольно протекающего процесса является сорбция. Сорбция – это процесс сгущения растворенного или парообразного вещества на поверхности твердого тела или жидкости. Сорбция, происходящая только на поверхности тела, называется поверхностным поглощением, или адсорбцией, а процесс поглощения объемом, называется абсорбцией. Поглощающее вещество называется сорбентом, а поглощаемое – сорбтив или сорбат.
Различают два вида адсорбции: физическую и хемосорбцию. В случае физической адсорбции молекулы сорбтива связаны с поверхностными атомами сорбента слабыми ван-дер-ваальсовыми силами (дисперсионными, индукционными и ориентационными). Физическая адсорбция – процесс обратимый, т.е. молекулы сорбтива могут переходить обратно в объем (десорбция).
Хемосорбция обусловлена проявлением химических, валентных сил между адсорбированными молекулами и атомами поверхности адсорбента. Особенно большое значение имеет адсорбция из газовой фазы на поверхности твердых веществ, которая зависит от давления, температуры и природы газа.
