| Т: 38-57,58, 60, 61, 63, 65,66 14,17 |
| *Зависимость термодинамических параметров для адиабатного процесса(без вывода) |
, где 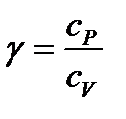 >1 >1 |
| молярная теплоемкость газа при постоянном давлении (ниже) |
| молярная теплоемкость газа при постоянном объеме (ниже) |
| c ↓V увеличивается не только концентрация молекул (как в изотермическом процессе), но и ↑Т, т.е. увеличивается средняя кинетическая энергия молекул, поэтому р газа растет быстрее. |
| I закон термодинамики для идеального газа при различных процессах |
| rоличество теплоты идет только на увеличение U |
| работа газа происходит за счет уменьшения его внутренней энергии |
| количество теплоты извне не поступает |
| либо в тепло-изолированных сосудах |
| либо так быстро, что тепло-обмен с окружающей средой не успевает произойти |
| например, быстрое расширение газа в баллончике сифона |
| все тепло идет на совершение работы |
| Изотермический Процесс Т = const |
| количество теплоты идет на работу газа и на увеличение его U |
| Если у движущихся молекул тела i степеней свободы, то справедливо: |
| для двухатомного ид. газа |
| если атомы жестко связаны, то молекула участвует еще и во вращательном движении отн. ценра массы, и положение атомов такой молекулы можно определить 5 величинами |
| для трех- и более-атомного ид.газа |
| если атомы жестко связаны, то молекулы участвуют не только в поступательном движении, но и во вращательном, и положение атомов такой молекулы можно определить 6 величинами |
| для одноатомного ид. газа |
| молекулы участвуют только в поступательном движении, и положение такой молекулы можно определить 3 величинами (координатами) |
| ** Внутренняя энергия двухатомного, трех- и более-атомного идеального газа |
| - справедлива для средней кинетической энергии молекул, участвующих только в поступательном движении |
- Для поступательного движения характерны три степени свободы (х, у,z) – минимальное количество независимых величин, с помощью которых может быть задано положение молекулы
- Для поступательно хаотически движущихся молекул все оси равновероятны, поэтому на каждую степень свободы приходится
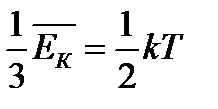 . . |
| I закон термодинамики по сути – это закон сохранения полной энергии (в данном случае - механической и внутренней) системы В замкнутой теплоизолированной системе тел полная энергия тел есть величина постоянная |
| Е = U+ Емех = const ∆Е = 0 |
| Если система получает из вне количество теплоты, то: |
| Если система тел получает количество теплоты Q, но механическая работа при этом не совершается, то: при этом могут идти процессы изменения агрегатного состояния тел: с – удельная теплоемкость = количеству теплоты, которое поглощает (выделяет) 1 кг вещества при нагревании (охлаждении) на 1оС=1К; λ – удельная теплота плавления= количеству теплоты, которое поглощает (выделяет) 1 кг вещества при плавлении (кристаллизации) (только для кристаллических тел); L – удельная теплота парообразования = количеству теплоты, которое поглощает (выделяет) при испарении (конденсации) 1 кг вещества при постоянной температуре |
| Количество теплоты, получаемое системой, идет на увеличение ее внутренней энергии и работу, совершаемую системой над внешними телами |
| ∆U1 + ∆U1 + … + ∆UN = 0 (1) |
| Если система тел, имеющих разную температуру, теплоизолирована (Q = 0) и при этом не совершается механическая работа, то: т.е в системе тел самопроизвольно идет теплопередача до тех пор, пока температура всех тел не сравняется. Внутренняя энергия каждого тела меняется, но полное изменение энергии системы = 0; если учесть, что у i – того тела ∆Ui = Qi, то (1) можно записать: |
| Другой вид уравнения теплового баланса: |
| уравнение теплового баланса |
| при этом: Qi =∆Ui > 0, если to↑ - забирают Q Qi =∆Ui < 0, если to↓ - отдают Q |
| Q1 + Q2 + …+ QK = |QK+1| +| QK+2| + …+|QN| |
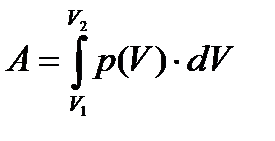 = площади под графиком р(V) = площади под графиком р(V) |
| Газ замечателен тем, что может существенно расширяться и, следовательно, совершать работу над внешними телами (например, над поршнем) за счет своей внутренней энергии |
| Работа газа над внешними телами |
| эту формулу можно использовать только, если р = const, т.е. при изобарных процессах |
| В общем случае, когда р ≠ const: |
| полная работа: А = dА1+dА2 + … = р1dV1 + р2dV2 + … |
| бесконечно малое изменение объема, такое, что рпрактически не изменяется |
| над поршнем при р = const |
| Пусть: F - сила давления, с которой газ действует на поршень (тело) ; F′ - сила, с которой поршень (тело) действует на газ в соответствии с III законом Ньютона: |
| Т: 1-5, 9-13, 15,16,18-20 |
т.к. ЕП = 0 то: 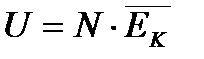 |
| одно из основных понятий термодинамики это: |
- Шарик, подвешенный на нити длиной l, отвели в
положение В и отпустили (рис. 3). После удара о стенку шарик отклонился на угол α до положения С. На сколько повысилась температура шарика, если k % потерянной мех анической энергии перешло во внутреннюю энергию шарика? Удельную теплоемкость с вещества шарика считать известной. Рис. 2 А В С t,оС Q,Дж Рис. 1 А В С t, мин |
| наука о тепловых явлениях без учета молекулярного строения вещества |
| внутренняя энергия тела, U кинетическая энергия хаотического (теплового) движения всех молекул и потенциальная энергия их взаимодействия |
| максимальное для идеального газа, для жидкостей и твердых тел ЕП < 0 |
| изменение внутренней энергии одноатомного идеального газа: |
| Справедливо только для поступательного движения молекул, а следовательно, для одноатомного газа |
| внутренняя энергия одноатомного идеального газа |
| Способы изменения внутренней энергии тела |
| передача внутренней энергии от одного тела к другому |
| мера изменения внутренней энергии тела |
| работа в этом случае является мерой превращения механической энергии во внутреннюю или наоборот |
| при неупругих соударениях |
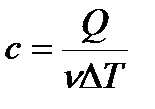 , , |
но: 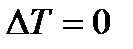 |
| Теплоемкость газа - не постоянная характеристика (у твердых тел и жидкостей – практически постоянная) |
| расчет молярной теплоемкости идеального газа |
| зависит от способа нагревания (охлаждения) газа |
| только для одноатомного ид.газа |
| все поступающее кол-во теплоты идет на ↑Т (↑U) |
| только часть кол-ва теплоты идет на ↑Т, другая часть – на совершение газом А |
A= 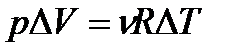 |
| только для адноатомного ид.газа |
| количество теплоты, необходимое для нагревания всего тела на 1К |
| количество теплоты, необходимое для нагревания 1 кг вещества на 1К |
| количество теплоты, необходимое для нагревания 1 моля вещства на 1К |
| молярная теплоемкость ид. газа при постоянном объеме |
| ** Удельная теплоемкость двухатомного, трех- и более-атомного идеального газа |
| для одноатомного ид. газа |
| молекулы участвуют только в поступательном движении |
| для двухатомного ид. газа |
| если атомы жестко связаны и молекула участвует еще и во вращательном движении отн. ценра массы, то положение атомов такой молекулы можно определить 5 величинами |
| для трех- и более-атомного ид.газа |
| если атомы жестко связаны и молекулы участвуют не только в поступательном движении, но и во вращательном, то положение атомов такой молекулы можно определить 6 величинами |
| Если у движущихся молекул тела i степеней свободы, то справедливо: |

| устройства, в которых внутренняя энергия топлива превращается в кинетическую энергию: UT EМЕХ |
| двигатель внутреннего сгорания |
| газообразное рабочее тело |
| Условия, необходимые для работы теплового двигателя (ТД) |
| такую работу может совершать газ, благодаря своей способности расширяться |
| само топливо не может совершать работу над внешними телами |
| ТД должен работать по замкнутому циклу |
| по окончании расширения газа поршень (и газ) необходимо вернуть в исходное положение |
| меньше |А2| газ должен иметь меньшее давление при сжатии меньшую Т2 нужен |
| площадь, ограниченная контуром V1abcV2 = А1 – работа газа при расширении |
| площадь, ограниченная контуром V1adcV2 = А′2 – работа над газом при сжатии |
| больше А1 газ должен иметь большее давление при расширении большую Т1 нужен |
| атмосфера, спец. охладители |
| ∆U1 +∆U2 = 0, т.к. цикл замкнут |
| полезная работа Ап: А1 – А′2 = (Qн-∆U1)– (∆U2-Qх )=Qн+Qх= Qн-|Qх| |
| вот если бы количество теплоты, переданное холодильнику самопроизвольно (без участия внешних тел) вновь возвращалось бы нагревателю, то η = 100% был бы возможен, но! |
| в циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую энергию всего количества теплоты, полученного от нагревателя, т.к. часть количества теплоты будет передано холодильнику: |
| все реальные самопроизвольные процессы (т.е. процессы в системе, идущие без участия внешних тел) являются необратимыми - т.е. не могут идти самопроизвольно в обратном направлении |
| - самопроизвольно не идет |
| газ расширяется самопроизвольно, но не может самопроизвольно сжаться |
| маятник самопроизвольно останавливается, но не может самопроизвольно раскачаться |
| КПД любого реального двигателя всегда меньше ηид ηреального<40% |
| Идеальный двигатель(Карно) |
| двигатель с максимальным КПД |
КПД = 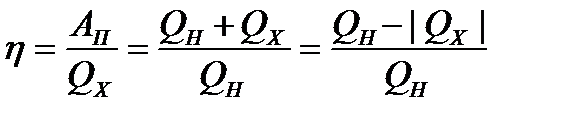 |
| тепловая машина, в которой количество теплоты передается от менее нагретого к более нагретому телу, при этом процесс - не самопроизвольный |
| изменение состояния рабочего тела (газа) происходит по обратному циклу |
| < 0 газ отдает тепло нагревателю |
| > 0 газ получает тепло от холодильника |
Наши рекомендации
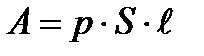
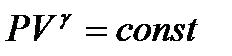
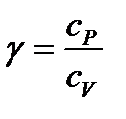 >1
>1 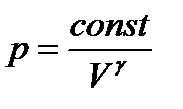
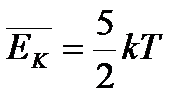
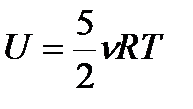
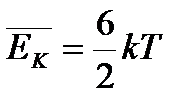
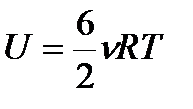
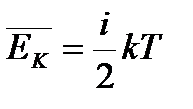
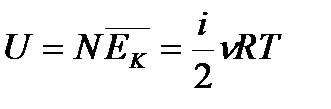
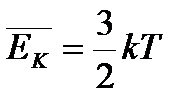
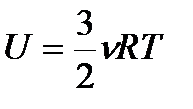
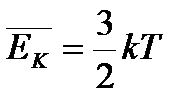
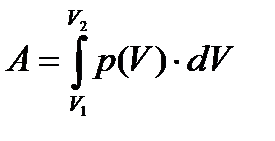 = площади под графиком р(V)
= площади под графиком р(V) 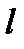
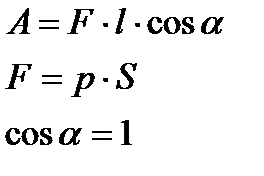
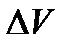
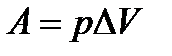
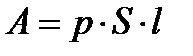
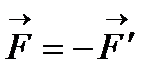
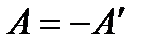
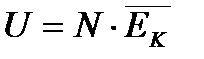
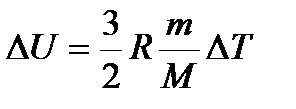
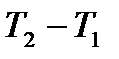
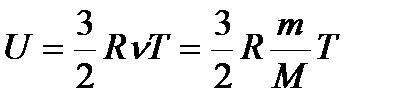
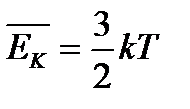
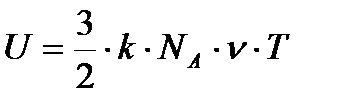
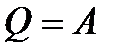
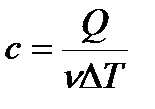 ,
, 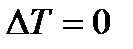
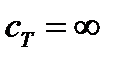
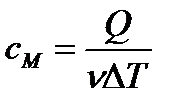
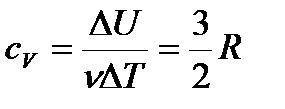
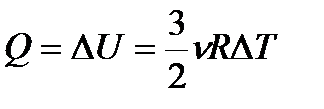
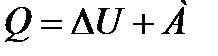
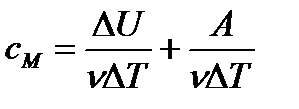
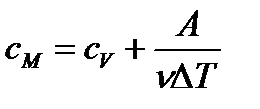
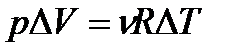
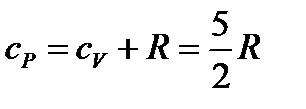
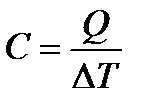
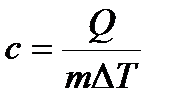
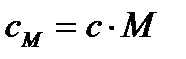
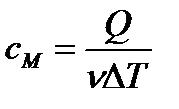
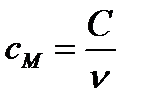
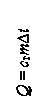
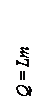
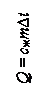
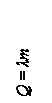
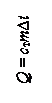
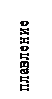
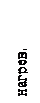
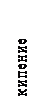
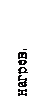

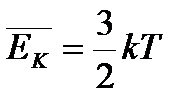
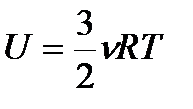
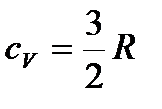
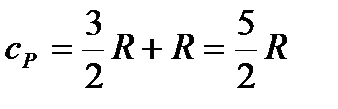
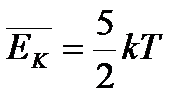
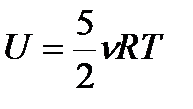
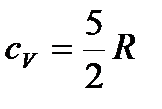
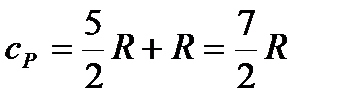
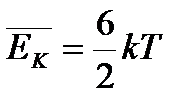
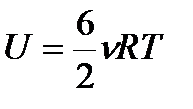
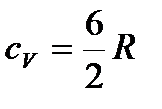
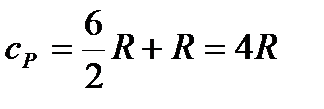
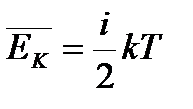
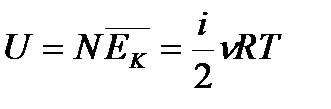
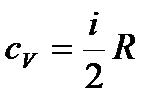
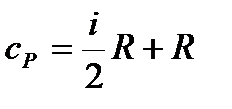

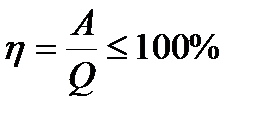
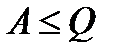
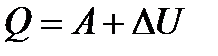
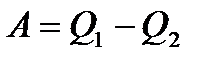
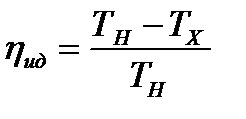
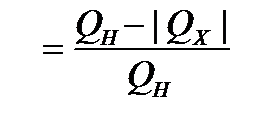
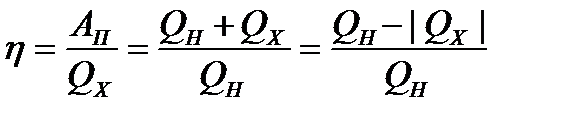
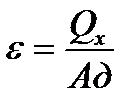
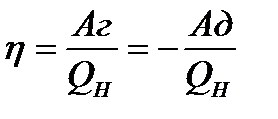
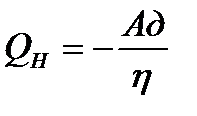
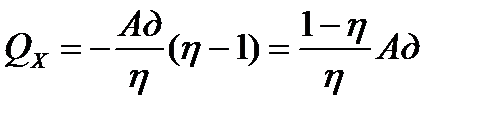
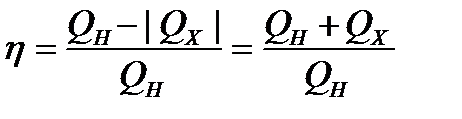

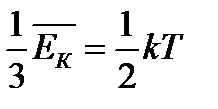 .
.