Задачи и упражнения для самостоятельного решения. 31.1.Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
31.1.Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
Al4C3 → CH4 → CH3Br → C2H6 → CO2 → CO → CH4.
Указать условия протекания реакций.
31.2. При сгорании 4,3 г образца алкана выделились 6,3 г воды и 6,72 л СО2 при нормальных условиях. Определить формулу алкана.
31.3. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
СН3−СН3 → СН2=СН2 → СН3−СН2ОН.
Указать условия протекания реакций.
31.4.Сколько граммов 1,6 %-й бромной воды может обесцветить 1,12 л пропилена при нормальных условиях? (Ответ: 500 г).
31.5.20 г карбида кальция обработали избытком воды, выделившийся ацетилен пропустили через бромную воду, получив 86,5 г 1,1,2,2-тетрабромэтана. Определить выход продукта реакции. (Ответ: 80 %).
31.6.Какие реакции следует провести, чтобы различить следующие газы: пропан, пропен и пропин? Написать уравнения соответствующих реакций.
31.7. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения: метан → Х → бензол.
Назвать вещество Х. Указать условия протекания реакций.
31.8. Из 3,36 л ацетилена (условия нормальные) получили 2,5 мл бензола. Определить выход продукта. Плотность бензола равна 0,88 г/мл.
(Ответ: 56,4 %).
31.9. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
CH3−CH2−CH2Br → CH3−CH=CH2 → CH3−CH2Br−CH3.
Указать условия протекания реакций.
31.10.Какой объем метана (условия нормальные) выделится: а) при гидролизе 72 г Al4C3; б) из 4,1 г безводного ацетата натрия? (Ответ: 33,6 л; 1,12 л).
31.11.Составить уравнения реакций, при помощи каких реакций можно осуществить следующие превращения:
CH4 → CH3Cl → C2H6 → C2H5Cl → C3H8.
31.12.Как, исходя из метана, можно получить бензол? Сколько литров метана при нормальных условиях необходимо затратить на получение 7,8 г бензола?
(Ответ: 13,4 л).
31.13.Какой объем 90 %-го раствора азотной кислоты (плотность 1,483 г/мл) потребуется для нитрования бензола, чтобы получилось 24,6 г нитробензола? (Ответ: 9,44 мл).
31.14. Состав соединения выражается формулой С4Н6. Известно, что это вещество легко взаимодействует с бромной водой, не реагирует с аммиачным раствором оксида серебра, но присоединяет воду в присутствии солей ртути (II). Написать структурную формулу соединения и назвать его.
31.15. Написать уравнения реакций, при помощи которых можно осуществить превращения: Al4C3 → X → Y → Cu2C2. Назвать соединения Х и Y.
31.16.Алкен нормального строения содержит двойную связь при первом углеродном атоме. 0,7 г этого алкена присоединил 1,6 г брома. Определить формулу алкена и назвать его.
31.17.Углеводород, состав которого выражается формулой С3Н4, взаимодействует с бромной водой и с натрием с выделением водорода. Определить структурную формулу углеводорода и назвать его.
31.18.При сгорании 3,6 г алкана образуется 5,6 л СО2 при нормальных условиях. Какой объем кислорода потребуется для реакции? (Ответ: 8,96 л).
31.19. Органическое вещество содержит углерод (массовая доля 84,21 %) и водород (15,79 %). Плотность паров вещества по воздуху составляет 3,93 (условия нормальные). Определить формулу этого вещества.
31.20.Массовая доля углерода в углеводороде составляет 83,33 %. Плотность паров углеводорода по водороду равна 36 (условия нормальные). Определить формулу углеводорода.
Спирты, альдегиды, кетоны
Теоретическое введение
Спирты– это производные углеводородов, у которых один или несколько атомов водорода замещены на гидроксильные группы −ОН.
Химические свойства спиртов определяются гидроксильной группой −ОН, входящей в состав молекулы. Химические реакции спиртов могут проте-
кать с участием всей группы (с разрывом связи С−О) или идти по водороду гидроксильной группы (с разрывом связи О−Н), например реакция этерификации:
уксусноэтиловый эфир (этилацетат)
Фенолы – это органические соединения, в которых гидроксильная группа соединена непосредственно с атомом углерода бензольного кольца. Простейшим представителем фенолов является гидроксибензол или фенол, имеющий одну гидроксильную группу в бензольном кольце:
или С6Н5−ОН
Фенол – твердое кристаллическое вещество с характерным запахом, плохо растворяющееся в воде. Химические свойства фенолов определяются гидроксильной группой и связанным с ней бензольным кольцом.
Кислотные свойства. Фенолы проявляют кислотные свойства и взаимодействуют со щелочными металлами и щелочами:
2C6H5OH + 2Na → 2C6H5ONa + H2;
C6H5OH + NaOH → C6H5ONa + H2O.
Реакции замещения в бензольном кольце. Гидроксильная группа оказывает очень большое влияние на бензольное кольцо, увеличивая его реакционную способность. Поэтому фенол легко вступает в реакции электрофильного замещения (с ориентацией заместителей в о- и п-положения). Например, он легко бромируется бромной водой с образованием 2,4,6-трибромфенола.
Качественная реакция на фенол. Фенол образует с FeCl3 комплексную соль, окрашенную в фиолетовый цвет.
Под действием окислителей (K2Cr2O7, KMnO4) в присутствии H2SO4 спирты окисляются с образованием альдегидов и кетонов, например:
3С2H5OH + K2Cr2O7 + 4H2SO4 → Cr2(SO)3 + K2SO4 + 3 + 7Н2О
уксусный альдегид
Альдегиды и кетоны содержат в молекуле карбонильную группу
В молекулах альдегидов карбонильная группа соединена с углеводородным радикалом и атомом водорода. Первым членом гомологического ряда аль-
дегидов является метаналь
формальдегид
40 %-ный водный раствор формальдегида называется формалином.
В молекулах кетонов карбонильная группа соединена с двумя разными R−CO−R′ или одинаковыми радикалами. Например,
ацетон
По своим химическим свойствам альдегиды являются восстановителями, которые легко окисляются в кислоты. Например, при окислении альдегидов аммиачным раствором оксида серебра образуется карбоновая кислота и происходит выделение металлического серебра. Оно тонким блестящим слоем покрывает стенки сосуда, в котором проводилась реакция, поэтому данная реакция называется «реакцией серебряного зеркала» и является качественной на альдегиды:
+ 2[Ag(NH3)2]OH → + 2Ag↓ + 4NH3 + H2O.
пропаналь пропановая кислота
Кетоны окисляются значительно труднее альдегидов и только сильными окислителями. При этом происходит разрыв углеродной цепи и образование смеси продуктов. Кетоны не вступают в реакцию серебряного зеркала.
Примеры решения задач
Пример 32.1.Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
С2Н4 → Х → Y → С2Н5−О−С2Н5.
Указать условия протекания реакций. Назвать вещества Х и Y.
Решение. Конечный продукт – диэтиловый эфир – получается из этилового спирта, следовательно, вещество Y – этанол. Перейти от этилена к этанолу можно через промежуточное соединение – галогенопроизводное этана (вещество Х).
При взаимодействии этилена с бромоводородом образуется бромэтан:
C2H4 + HBr → C2H5Br.
Бромэтан гидролизуется до спирта действием водного раствора NaOH:
C2H5Br + NaOH → C2H5OH + NaBr.
При нагревании этанола до 140 °С в присутствии серной кислоты в качестве катализатора образуется диэтиловый эфир:
C2H5OH 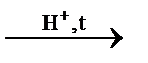 С2Н5−О−С2Н5 + H2O.
С2Н5−О−С2Н5 + H2O.
Пример 32.2. Какая масса пропилата натрия может быть получена при взаимодействии 15 г пропанола-1 с 9,2 г натрия?
Решение. Записываем уравнение реакции между пропанолом-1 и металлическим натрием:
2CH3−СH2−СН2−OH + 2Na → 2CH3−СH2−СН2−ONa + H2.
Определяем количества вещества пропанола-1 и натрия:
υ (С3Н7ОН) = 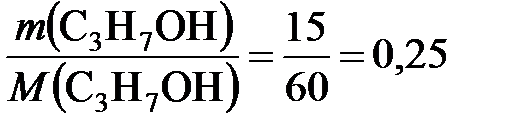 моль;
моль;
υ (Na) = 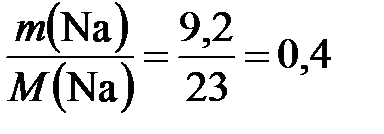 моль.
моль.
Из уравнения реакции следует, что число моль спирта и натрия должны быть равны, следовательно, натрий взят в избытке.
На основании уравнения реакции записываем:
υ (C3H7ONa) = υ(C3H7OH); υ (C3H7ONa) = 0,25 моль.
Определяем массу пропилата натрия, которую можно получить:
m (C3H7ONa) = υ(C3H7ONa) ∙ M(C3H7ONa);
m (C3H7ONa) = 0,25 ∙ 82 = 20,5 г.
Пример 32.3. Формалин представляет собой 40 %-ный водный раствор формальдегида. Рассчитать массу метанола, которую необходимо окислить для получения 600 г формалина.
Решение. Вычисляем массу формальдегида, который потребуется для приготовления формалина:
m (CH2O) = 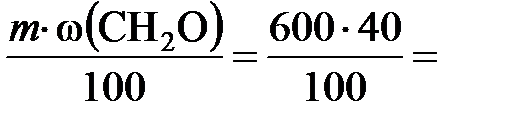 240 г.
240 г.
Количество вещества требуемого формальдегида равно
υ (CH2O) = 
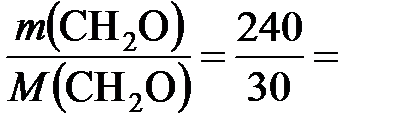 8 моль.
8 моль.
Составляем уравнение реакции окисления метанола:
CH3OH + [O] → CH2O + H2O.
Из уравнения реакции следует, что υ (CH3OH) = υ(CH2O); υ(CH2O) = 8 моль.
Масса требуемого метанола равна
m (CH3OH) = υ(CH3OH) ∙ M (CH3OH);
m (CH3OH) = 8 ∙ 32 = 256 г.
