Получение геля кремниевой кислоты
Лабораторный способ
- Разложение жидкой муравьиной кислоты под действием горячей концентрированной серной кислоты, либо пропускание газообразной муравьиной кислоты над оксидом фосфора P2O5. Схема реакции:
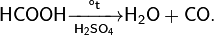
Можно также обработать муравьиную кислоту хлорсульфоновой. Эта реакция идёт уже при обычной температуре по схеме:
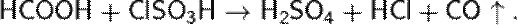
- Нагревание смеси щавелевой и концентрированной серной кислот. Реакция идёт по уравнению:
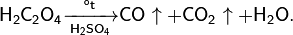
- Нагревание смеси гексацианоферрата(II) калия с концентрированной серной кислотой. Реакция идёт по уравнению:
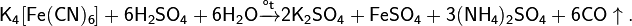
- Восстановлением из карбоната цинка магнием при нагревании:
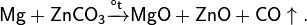
Кремний
Опыт 11
С водородом кремний непосредственно не реагирует, соединения кремния с водородом — силаны с общей формулой SinH2n+2 — получают косвенным путем. Моносилан SiH4 (его часто называют просто силаном) выделяется при взаимодействии силицидов металлов с растворами кислот, например:
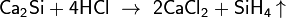
Образующийся в этой реакции силан SiH4 содержит примесь и других силанов, в частности, дисилана Si2H6 и трисилана Si3H8, в которых имеется цепочка из атомов кремния, связанных между собой одинарными связями (—Si—Si—Si—).
Для травления кремния наиболее широко используют смесь плавиковой и азотной кислот. Некоторые специальные травители предусматривают добавку хромового ангидрида и иных веществ. При травлении кислотный травильный раствор быстро разогревается до температуры кипения, при этом скорость травления многократно возрастает.
- Si+2HNO3=SiO2+NO+NO2+H2O
- SiO2+4HF=SiF4+2H2O
- 3SiF4+3H2O=2H2SiF6+↓H2SiO3
Для травления кремния могут использоваться водные растворы щёлочей. Травление кремния в щелочных растворах начинается при температуре раствора более 60 °C.
- Si+2KOH+H2O=K2SiO3+2H2↑
- K2SiO3+2H2O↔H2SiO3+2KOH
опыт 12
Получение
Силаны обычно получают, разлагая кислотами силициды металлов (например, силицид магния):
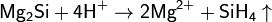
Для синтеза моносилана используют разложение триэтоксисилана в присутствии Na, и нагревании (t=80 °C):
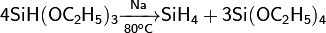
либо применяют реакцию:
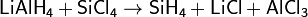
Получение силана
Соединения металлов с кремнием называются силицидами. Силицид магния - порошок черного цвета. Поместим порошок силицида магния в очень слабый раствор соляной кислоты. На поверхности раствора образуются пузырьки газа. Они лопаются и загораются на воздухе. Это горит силан. Он образуется при взаимодействии кислоты с силицидом магния. Продуктами сгорания силана являются оксид кремния и вода.
Mg2Si + 4HCl = SiH4 + 2MgCl2
SiH4 + 2O2 = SiO2 + 2H2O
Опыт 14
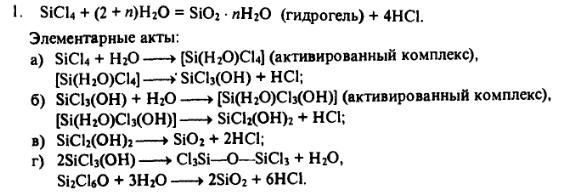
опыт 15
Получение геля кремниевой кислоты
Кремниевая кислота – слабая кислота. Она легко выделяется из растворов солей кремниевой кислоты при действии на них более сильными кислотами. К раствору силиката натрия прильем сильно разбавленный раствор соляной кислоты. При этом кремниевая кислота выделяется не в виде осадка, а в виде геля. Раствор немного мутнеет и «застывает». При опрокидывании стакана гель не выливается.
Na2SiO3 + 2HCI = H2SiO3 + 2 NaCI
опыт 16
Кремниевую кислоту получают косвенным путем, действуя . кислотой на силикат калия или натрия:
Na2SiO3+2HCl=2NaCl+H2SiO3
Кремниевую кислоту нельзя получить в чистом виде. В водных растворах она образует коллоидный раствор, или золь, который существует очень малый промежуток времени. Золь далее коагулирует, и образуется гель. При высушивании геля образуются продукты с пористой структурой — силикагели, применяемые в качестве осушителей и адсорбентов.
H2SiO3 — кислота очень слабая, в воде малорастворимая. При нагревании легко распадается аналогично угольной кислоте:
H2SiO3=H2O+SiO2
