Классификация легочного сердца
(по Б.Е. Вотчалу, 1964)
| Характер течения | Состояние компенсации | Преимущественный патогенез | Особенности клинической картины |
| Острое легочное сердце: развитие в течение нескольких часов | Декомпенсированное | Васкулярный Бронхолегочный | Массивная тромбоэмболия легочной артерии. Клапанный пневмоторакс. Затяжной приступ бронхиальной астмы. Пневмония (с большой площадью поражения) |
| Подострое легочное сердце: развитие в течение нескольких недель, месяцев | Компенсированное Декомпенсированное | Васкулярный Бронхолегочный Торакодиафрагмальный | Повторные мелкие тромбоэмболии в системе легочной артерии: тромбы, эмболы, яйца паразитов и др. Повторные затяжные приступы бронхиальной астмы. Раковый лимфангит легких. Хроническая гиповентиляция центрального и периферического происхождения при ботулизме, полиомиелите, миастении и др. |
| Хроническое легочное сердце: развитие в течение нескольких лет | Компенсированное Декомпенсированное по правожелудочковому типу | Васкулярный Бронхолегочный Торакодиафрагмальный | Первичная легочная гипертония. Артерииты. Повторные эмболии. Резекция легкого. Обструктивные процессы в бронхах и легких (хронический бронхит, бронхиальная астма, эмфизема легких, диффузный пневмосклероз с эмфиземой). Рестриктивные процессы (фиброзы, гранулематозы). Поликистоз легких. Поражение позвоночника и грудной клетки с ее деформацией. Плевральные шварты. Ожирение (синдром Пиквика) |
При формулировке диагноза называют основное заболевание, приведшее к формированию легочного сердца, и степень выраженности легочной (дыхательной) недостаточности. Затем указывают на наличие легочного сердца и его стадии (компенсированное, декомпенсированное). Степень сердечной недостаточности оценивают по общепринятой классификации.
Графы 3 и 4 вышеуказанной классификации легочного сердца способствуют пониманию его патогенеза и выбору тактики лечения.
Патогенез. В основе формирования легочного сердца лежит легочная гипертензия в малом круге кровообращения (в прекапиллярной системе), приводящая к гипертрофии правого желудочка, а затем к его дилатации и сердечной недостаточности.
Среди механизмов, способствующих возникновению легочной гипертензии, различают функциональные и анатомические. Решающая роль принадлежит функциональным механизмам, к которымотносят:
- повышение тонуса и рефлекторный спазм легочных артериол при низких значениях в альвеолярном воздухе Р О2 (альвеолярная гипоксия) и высоких - Р СО2 (гиперкапния), выключающий из перфузии плохо вентилируемые участки легкого и тем самым уменьшающий гипоксемию;
- повышение давления в бронхиолах и альвеолах, приводящее к сдавлению артериол и капилляров;
- повышение содержания в крови вазоактивных биогенных аминов и метаболитов;
- рефлекторное увеличение минутного объема крови при гипоксемическом раздражении хеморецепторов аортально-каротидной зоны;
- компенсаторный эритроцитоз, повышение вязкости крови.
Функциональные механизмы являются “мишенью” для лечения.
Анатомическими механизмами, способствующими легочной гипертензии являются:
- закрытие просвета сосудов системы легочной артерии в результате облитерации или эмболизации;
- сдавление легочной артерии извне;
- значительное уменьшение русла малого круга кровообращения в результате пульмонэктомии.
На ранних стадиях формирования хронического легочного сердца преобладают компенсаторно-приспособительные реакции, которые обеспечиваются большой площадью альвеолярного аппарата и капиллярной сети легких, мощностью дыхательных и сердечной мышц. Истощение компенсаторных механизмов способствует прогрессированию и клиническим проявлениям процесса.
Пусковым фактором патогенеза хронического легочного сердца является альвеолярная гипоксия, возникающая при обструктивных или рестриктивных нарушениях легочной вентиляции и приводящая к артериальной гипоксемии. В результате гипоксии легочной ткани выделяются биологически активные вещества (гистамин, серотонин, ангиотензин, молочная кислота, простагландины и др.), вызывающие локальное или генерализованное повышение тонуса легочных артериол и мелких артерий. Гипоксическая легочная вазоконстрикция выключает из перфузии плохо вентилируемые участки легкого и тем самым уменьшает гипоксемию (рефлекс Эйлера-Лильестранда). Повышению тонуса легочных артериол в условиях гипоксии способствует снижение выработки эндотелием легочных сосудов простациклина и эндотелийрасслабляющего фактора, действующим началом которого является окись азота – NO. Одновременно увеличивается продукция тромбоцитами тромбоксана и тканевого ангиотензина –II, вызывающего сильное сосудосуживающее действие. Генерализованное повышение тонуса мелких легочных сосудов приводит к легочной артериальной гипертензии.
Развивающаяся артериальная гипоксемия способствует повышению давления в легочной артерии вследствие увеличения минутного объема крови при раздражении хеморецепторов аортально - каротидной зоны, а также в результате увеличения сопротивления легочному кровотоку из-за компенсаторной полицитемии и повышенной вязкости крови. Происходит образование агрегатов тромбоцитов, что способствует гипертензии в микроциркуляторном русле легких.
Легочной гипертензии способствуют также механическое сдавление и склеротическое запустевание артериол и капилляров. Эти последовательные процессы наблюдаются при эмфиземе легких и бронхообструктивном синдроме вследствие стойко повышенного давлении в альвеолах и бронхиолах, особенно при непродуктивном надсадном кашле, интенсивной физической нагрузке и повышении внутригрудного давления в фазе затрудненного выдоха. Появление клинических признаков хронического легочного сердца происходит при склеротической облитерации 5-10% общей площади легочных капилляров. Поддерживает гипертензию расширение бронхиальных сосудов и формирование бронхиально-пульмональных анастомозов.
В последние годы механизм гипоксической вазоконстрикции связывают с прямым действием гипоксии на гладкие мышцы легочных артерий.
Под влиянием вышеуказанных патогенетических факторов возникает гипертрофия правого желудочка, а затем и правого предсердия (компенсированное хроническое легочное сердце). Усиленная работа правых отделов сердца в условиях артериальной гипоксемии быстро приводит к дистрофическим изменениям миокарда, последующей миогенной дилатации и правожелудочковой сердечной недостаточности, т.е. декомпенсированному легочному сердцу.
В настоящее время большинство ученых считают, что при хроническом легочном сердце развиваются структурно - функциональные нарушения и со стороны левого желудочка. Их связывают, прежде всего, с воздействием артериальной гипоксемии, способствующей ремоделированию миокарда обоих желудочков, а также легочных и периферических артерий. Дисфункция левого желудочка может быть связана и со смещением межжелудочковой перегородки влево вследствие гипертрофии или дилатации правого желудочка.
Проводится параллель между патогенетической ролью активации плазменной и тканевых ренин-ангиотензин-альдостероновой систем (РААС) в развитии хронической левожелудочковой недостаточности и хронического легочного сердца. Установлено, что при хронических заболеваниях легких и легочной гипертензии уровень ангиотензинпревращающего фермента (АПФ) и компонентов РААС нарастает параллельно увеличению степени гипоксемии с момента развития дыхательной недостаточности при отсутствии признаков нарушения кровообращения. Указанные нейро-гормональные изменения, стимулируя процессы фиброза, способствуют ремоделированию миокарда обеих желудочков и развитию сначала диастолической, а затем систолической их дисфункции.
Основные звенья патогенеза хронического легочного сердца представлены на рис. 31.
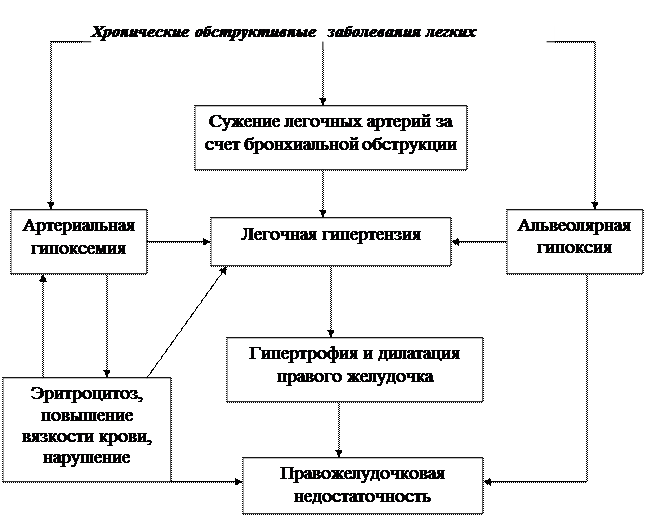

Рис. 31. Патогенез хронического легочного сердца
Клиника. Хроническое легочное сердце в 80% случаев развивается в результате хронической патологии бронхолегочной системы, поэтому в клинической картине долгое время доминируют признаки основного заболевания и легочной (дыхательной) недостаточности.
Легочная (дыхательная) недостаточность – состояние организма, при котором не обеспечивается поддержание нормального газового состава крови, либо оно достигается за счет более интенсивной работы аппарата внешнего дыхания и повышенной нагрузки сердца.
Различают три степени легочной недостаточности:
I степень – одышка и тахикардия возникают только при повышенной физической нагрузке, цианоза нет; показатели функции внешнего дыхания (МОД, ЖЕЛ) в покое соответствуют должным, но при выполнении нагрузки изменяются; МВЛ снижается; газовый состав крови не изменен; кислотно- основное состояние и функция кровообращения в норме.
II степень – одышка и тахикардия появляются при незначительной физической нагрузке, выражен цианоз; МОД и ЖЕЛ в покое снижены, МВЛ значительно снижена; в альвеолярном воздухе снижается Р О2 и увеличивается Р СО2; содержание газов в крови благодаря усилению вентиляции не изменено; определяется дыхательный алкалоз; могут быть первые проявления нарушения функции кровообращения.
III степень – одышка и тахикардия наблюдаются в покое, резко выражен цианоз; значительно снижена ЖЕЛ, а МВЛ невыполнима; гипоксемия, гиперкапния, дыхательный ацидоз; выражены проявления сердечной недостаточности.
Понятие “дыхательная недостаточность” шире, чем “легочная недостаточность”, так как определяет недостаточность не только внешнего, но и тканевого дыхания, развивающуюся при декомпенсированном легочном сердце. Легочное сердце развивается на фоне дыхательной недостаточности II и чаще III степени.
Находясь в тени основного заболевания, хроническое легочное сердце нередко диагностируется только в стадии декомпенсации с появлением признаков правожелудочковой недостаточности. Некоторые симптомы дыхательной и сердечной недостаточности сходны по своим клиническим проявлениям, что затрудняет диагностику и декомпенсированного легочного сердца.
В стадии компенсации основной жалобой является одышка, усиливающаяся при физической нагрузке или наблюдающаяся в покое. Одышка не сопровождается ортопноэ, уменьшается от применения бронхолитиков и ингаляций кислорода и не реагирует на введение сердечных гликозидов. Такая одышка связана с дыхательной недостаточностью.
С хронической гипоксией связаны жалобы на общую слабость, головные боли, сонливость днем и бессонницу ночью, сердцебиение, колющие или постоянные боли в сердце. Причинами кардиалгий могут быть метаболические нарушения миокарда, рефлекторное сужение правой коронарной артерии (пульмокоронарный рефлекс), снижение наполнения коронарных артерий при повышении конечного диастолического давления в гипертрофированном правом желудочке.
При осмотре выявляется теплый диффузный цианоз, обусловленный артериальной гипоксемией. Гиперкапния обуславливает расширение мелких сосудов и связанную с этим теплоту рук. В результате длительной гипоксемии формируются специфические признаки – утолщение концевых фаланг пальцев в виде “барабанных палочек” и ногтей в форме ”часовых стекол”.
На выдохе могут появляться набухшие шейные вены из-за нарушения венозного возврата крови вследствие повышения внутригрудного давления на фоне тяжелой бронхиальной обструкции.
Клиническим проявлением гипертрофии правого желудочка является усиленный разлитой сердечный толчок, определяемый в прекардиальной или в подложечной области. При выраженной эмфиземе легких, когда сердце прикрыто и оттесняется от передней грудной стенки расширенными легкими, указанный симптом выявляется редко. Выявление эпигастральной пульсации может свидетельствовать о гипертрофии правого желудочка или низком стоянии диафрагмы при эмфиземе, что уменьшает ее диагностическое значение.
Перкуторно может выявляться расширение правой границы сердца, однако из-за эмфиземы легких этот клинический признак легочного сердца обычно отсутствует. При аускультации тоны сердца лучше выслушиваются в эпигастральной области. Косвенным признаком гипертрофии правого желудочка являются аускультативные данные, свидетельствующие о легочной гипертензии. К ним относятся акцент II тона и расщепление его во II межреберье слева, которые появляются при повышении давления в легочной артерии не менее чем в два раза. При высокой степени легочной гипертензии здесь же может выслушиваться диастолический шум Грехема-Стилла в связи с дилатацией легочной артерии.
Уточнению диагноза способствует проведение инструментальных методов обследования:
1. Анализы крови обнаруживают эритроцитоз, высокое содержание гемоглобина, повышение гематокрита, замедленную СОЭ, склонность к повышенной коагуляции. При обострении бронхолегочной инфекции возможны лейкоцитоз и небольшое ускорение СОЭ.
2. Рентгенография и компьютерная томография органов грудной клетки выявляют ранний признак легочного сердца – выбухание конуса и ствола легочной артерии (в 1-м косом положении) и расширение ее. Прикорневые сосуды расширены при обедненном периферическом рисунке (“обрубленность” корней легких). Важным критерием легочной гипертензии является расширение правой нисходящей ветви легочной артерии до 19 мм и более. Отмечается увеличение правого желудочка и предсердия.
3. Электрокардиография определяет наличие гипертрофии правого желудочка по следующим признакам:
- высокий или преобладающий зубец R в V1-2 , глубокий зубец S в левых грудных отведениях;
- сдвиг переходной зоны к V4-6 ;
- полная или неполная блокада правой ножки пучка Гиса;
- появление зубца Q в V 1-2 при перегрузке правого желудочка;
- уплощение или инверсия зубца Т в V 1-2;
- появление высокого остроконечного зубца Р (Р-pulmonale) во II, Ш, аVF и правых грудных отведениях при перегрузке правого предсердия.
Мерцательная аритмия для хронического легочного сердца не характерна.
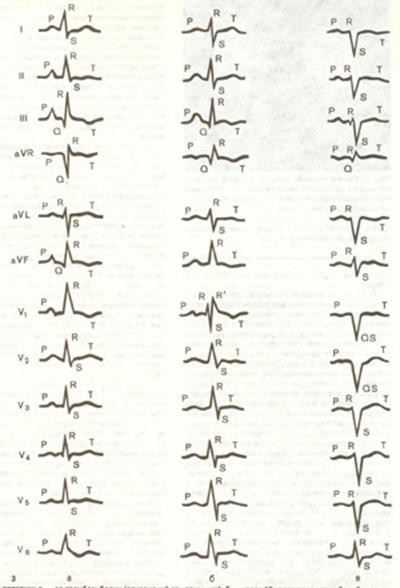 |
| Рис. 34. Основные типы ЭКГ при хроническом легочном сердце |
4. Эхокардиография выявляет гипертрофию правых отделов сердца (увеличение толщины стенки желудочка более 2-3 мм) и расширение полости правого желудочка. Определяются давление в правом желудочке, наличие и степень выраженности легочной гипертензии.
5. Реография органов грудной клетки позволяет определить величину давления в легочной артерии.
6. Фонокардиография отражает усиление II тона и диастолический шум над легочной артерией.
7. Катетеризация правого желудочка и легочной артерии (проводимая только в специализированных отделениях) наиболее достоверно выявляет легочную гипертензию.
8. Спирография помогает определить только характер (обструктивный, рестриктивный, смешанный) и степень нарушения функции внешнего дыхания, зависящие от основного заболевания, но не диагностирует легочное сердце.
Декомпенсация легочного сердца часто наступает в результате обострения хронического или присоединения острого бронхолегочного заболевания, увеличивающего бронхиальную обструкцию и легочную гипертензию.
Распознавание начальных стадий сердечной недостаточности (I-IIА) затруднено схожестью клинических проявлений с дыхательной недостаточностью (одышка, утомляемость, цианоз, сердцебиение и др.). Важен анализ динамики жалоб и клинических симптомов.
Одышка становится постоянной и выраженной даже в покое. Она не уменьшается после приема бронхолитиков, усиливается после кашля и проявляется увеличением частоты дыхания, а не удлинением выдоха (в отличие от дыхательной недостаточности, обусловленной бронхообструктивным синдромом). Развивается ортопноэ - вынужденное положение сидя. Дыхательная недостаточность достигает III степени (одышка в покое). Прогрессируют утомляемость, сонливость и головные боли, как результат гипоксемии и гиперкапнии. Гемодинамическая перегрузка миокарда в условиях гипоксии вызывает частые боли в сердце, не проходящие от приема нитроглицерина. Возможны приступы удушья из-за внезапных подъемов давления в системе легочной артерии. Появляются жалобы на тяжесть в правом подреберье, отеки, увеличение размеров живота вследствие застойных явлений в большом круге кровообращения.
При осмотре выявляется постоянное (на вдохе и выдохе) набухание шейных вен, положительный венный пульс. На фоне диффузного теплого цианоза, связанного с дыхательной недостаточностью, появляется холодный сердечный акроцианоз. Появляется и нарастает пастозность голеней. Определяется выраженная эпигастральная пульсация правого желудочка. Тоны сердца становятся глухими, выслушивается систолический шум у мечевидного отростка грудины, связанный с относительной недостаточностью трикуспидального клапана.
Определяется увеличенная, чувствительная или болезненная при пальпации печень. В начальных стадиях выявляется увеличение преимущественно левой доли, во II-Б - III стадиях печень может определяться на уровне пупка. Появляется симптом Плеша – надавливание на увеличенную болезненную печень вызывает набухание шейных вен. Следует помнить, что при эмфиземе легких печень может выступать из-под края реберной дуги и без сердечной недостаточности – вследствие опущения, поэтому важно определять размеры печени по Курлову. При тяжелой сердечной недостаточности выявляются отеки нижних конечностей, асцит, анасарка, гидроторакс, трофические нарушения кожи.
Дополнительные методы исследования в стадии декомпенсации легочного сердца выявляют более выраженное увеличение и перегрузку правых отделов сердца, прогрессирование гемодинамических изменений в системе легочной артерии, замедление общего кровотока и повышение венозного давления, выраженную артериальную гипоксемию и гиперкапнию. На фоне прогрессирования правожелудочковой недостаточности выявляется дисфункция и левого желудочка.
Дифференциальный диагноз хронического декомпенсированного легочного сердца проводят с хронической сердечной недостаточностью IIБ-III стадий, обусловленной пороками сердца, кардиомиопатиями, ишемической болезнью сердца, миокардиосклерозом и другими заболеваниями. В пользу легочного сердца свидетельствуют: анамнез (указание на хроническую бронхолегочную патологию), особенности клинических проявлений (одышка без ортопноэ, диффузный теплый цианоз, отсутствие мерцательной аритмии); данные ЭКГ и ЭХО КГ (признаки гипертрофии и перегрузки правых отделов сердца, отсутствие перегрузки левого предсердия), рентгенологические данные (наличие бронхолегочной патологии и легочной гипертензии, увеличение правых отделов сердца).
Лечение. Лечебный режим при хроническом легочном сердце предусматривает отказ от курения, ограничение физических нагрузок, назначение при декомпенсации диеты с ограничением жидкости и поваренной соли (стол № 10).
Первостепенное значение имеет адекватная терапия основного заболевания, приведшего к развитию легочного сердца.
Лечение хронического легочного сердца должно быть ранним и комплексным, направленным на основные звенья патогенеза: нарушения газообмена, легочную гипертензию, дыхательную и правожелудочковую недостаточность.
1. Важная роль в уменьшении альвеолярной гипоксии принадлежит оксигенотерапии. Применяется длительная или ночная оксигенотерапия с 30 % содержанием кислорода во вдыхаемом воздухе, со скоростью потока 2-3 л/мин. в покое и 5 л/мин. при нагрузке. Для доставки кислорода в дыхательные пути пациента используют носовые канюли, маски или транстрахеальные катетеры. Продолжительность эффективной оксигенотерапии должна быть не менее 15 часов в сутки. По показаниям может быть использована вспомогательная искусственная вентиляция легких сеансами по 20-30 мин. в течение 4 недель.
Применение оксигенотерапии способствует уменьшению артериальной гипоксемии, уменьшению бронхиального и бронхо-альвеолярного сопротивления, снижению давления в легочной артерии и улучшению сократительной функции правого желудочка.
С целью улучшения кислородотранспортной функции крови применяется гипербарическая оксигенация. Усилению отщепления кислорода в тканях способствуют нитраты.
Имеет перспективы использование при хроническом легочном сердце ингаляций окиси азота (NO), оказывающего эндотелийрасслабляющий эффект, приводящий к снижению давления в легочной артерии и повышению парциального давления кислорода в крови.
2. Улучшение бронхиальной проходимости достигается назначением антибактериальных препаратов и ингаляционных кортикостероидов, уменьшающих воспаление и отек слизистой оболочки бронхов, и бронхолитиков – ингаляционных β2-агонистов и антихолинергических средств, метилксантинов и антагонистов кальция.
Особое место занимают метилксантины – эуфиллин и пролонгированные теофиллины, так как они не только уменьшают бронхиальную обструкцию, но и улучшают гемодинамику малого круга кровообращения и почечный кровоток, оказывают также и небольшой диуретический эффект.
Бронхиальному дренажу способствуют муколитики и отхаркивающие средства, комплекс лечебной физкультуры.
3. С целью снижения легочной гипертензии применяются метилксантины, антагонисты кальция, блокаторы ангиотензинпревращающего фермента, нитраты, антагонисты альдостерона. Эуфиллин назначается внутривенно или в свечах при усилении бронхиальной обструкции или легочной гипертензии. Для поддерживающей терапии предпочтительны пролонгированные теофиллины (теопек, теотард, теолонг), продолжительность действия которых достигает 12-24 часов. Их суточная доза, разделенная на два приема, составляет 0,4 - 0,6 г; при легочной гипертензии с недостаточностью кровообращения она снижается до 0,2 – 0,4 г из-за риска кумуляции.
Применение периферических вазодилататоров у больных с легочным сердцем не должно вызывать системной артериальной гипотензии, поэтому лечебные дозы препаратов определяются с учетом исходного уровня АД.
С ранних стадий легочной гипертензии назначаются антагонисты кальция - нифедипин – 40-80 мг в сутки, верапамил – 80- 240 мг в сутки, дилтиазем – 75 мг в сутки. Препаратами выбора являются пролонгированные (ретардные) формы препаратов. Антагонисты кальция оказывают непосредственное вазодилатирующее влияние на сосуды легочного круга, а также бронхорасширяющее действие. При декомпенсированном легочном сердце антагонисты кальция не показаны в связи с активацией симпатоадреналовой системы и РААС.
Хороший эффект как при стабильной легочной гипертензии, так и при начинающейся декомпенсации оказывают пролонгированные нитраты(нитросорбид, нитронг, сустак, изомак-спрей и др.), уменьшающие гипоксемическую вазоконстрикцию и снижающие давление в легочной артерии. Кроме того, нитраты уменьшают венозный приток к правому сердцу (разгрузку объемом), что определяет их эффективность при декомпенсированном легочном сердце.
Ингибиторы АПФ назначаются при компенсированном и декомпенсированном легочном сердце. Препараты снижают давление в легочной артерии, общее периферическое сопротивление, улучшают почечную гемодинамику, но не оказывают прямого бронходилатирующего эффекта. При сочетании с эуфиллином гипотензивный эффект в малом круге кровообращения усиливается. Наряду с ингибиторами АПФ применяются антагонисты рецепторов ангиотензина –II (козаар, ларзартан).
Антагонисты альдостерона (верошпирон, спиронолактон) при легочной гипертензии действуют подобно антагонистам кальция, оказывая прямое вазодилатирующее и бронхорасширяющее действие. При длительном приеме антагонисты альдостерона предупреждают прогрессирование сердечной недостаточности.
4.Лечение правожелудочковой недостаточности проводится согласно общим принципам лечения сердечной недостаточности (периферические вазодилататоры, ингибиторы АПФ, сердечные гликозиды, диуретики).
Сердечные гликозиды назначают только при выраженной застойной сердечной недостаточности с присоединением мерцательной аритмии. Компенсаторная тахикардия при дыхательной недостаточности не является показанием к назначению сердечных гликозидов. Препаратом выбора с учетом меньшей наклонности к кумуляции является коргликон, применяемый в виде 0,06% раствора внутривенно по 0,5-1 мл 1-2 раза в сутки. На фоне гипоксической и дисметаболической миокардиодистрофии применение гликозидов очень быстро приводит к гликозидной интоксикации и аритмиям сердца, что, также может повысить давление в легочной артерии из-за увеличения сердечного выброса и общего периферического сопротивления.
При появлении отеков применяют мочегонные(фуросемид, лазикс, калийсберегающий препарат триамтерен). В связи с тем, что при легочной гипертензии быстро развивается вторичный гиперальдостеронизм (до появления признаков правожелудочковой недостаточности) рекомендуется раннее и длительное назначение больным антагонистов альдостерона (верошпирон по 0,05 г 3 раза в сутки). Кроме мочегонного установлены их вазодилатирующий, бронхорасширяющий и противовоспалительный эффекты, что важно при лечении больных с обострением хронической обструктивной болезни легких.
4. С целью коррекции гемореологических нарушений, развивающихся у больных с хронческим легочным сердцем, и профилактики микротромбирования сосудов малого круга кровообращения применяют антикоагулянты(гепарин, фраксипарин) и дезагреганты (курантил, трентал, ацетилсалициловая кислота), реополиглюкин по 200-400 мл внутривенно капельно 2 раза в неделю.
Иногда для снижения давления в легочной артерии применяют кровопускание. Показанием к нему является эритроцитоз, увеличение гематокрита более 55-60%. Количество удаляемой крови составляет 200 - 400 мл с заместительной реинфузией реополиглюкина. Кровопускание способствует выходу в кровь молодых эритроцитов, обладающих хорошими газотранспортными свойствами, а реополиглюкин восстанавливает объем циркулирующей крови и микроциркуляцию.
5. Назначаются средства, повышающие энергетические обменные процессы в миокарде, – калия оротат (по 0,5 г 3 раза в сутки), рибоксин (по 0,2 - 0,6 г 3 раза в сутки), инозие - Ф (по 0,4 - 0,6 г 3 раза в сутки), кокарбоксилаза (по 0,1 г 1 раз в сутки внутримышечно), предуктал (по 0,02 г 3 раза) и др. В качестве антиоксиданта рекомендуется а-токоферола ацетат внутрь в течение 1-2 месяцев, с повторным курсом через 3 месяца.
Из немедикаментозных методов лечения при хроническом легочном сердце применяют гемосорбцию (удаление из крови фибриногена, продуктов деградации фибрина), эритроцитаферез (удаление патологически измененных эритроцитов), электростимуляцию диафрагмы.
Прогноз.Хроническое легочное сердце ухудшает прогноз многих легочных заболеваний, поэтому необходимо проводить его активную терапию уже на ранних стадиях развития. Продолжительность жизни больных с декомпенсированным легочным сердцем составляет в среднем 1,5-3 года.
Профилактиказаключается в предупреждении и своевременном лечении хронических обструктивных заболеваний легких и другой патологии, приводящей к развитию легочного сердца.
