Системная красная волчанка
Схема 39. Патогенез ревматических болезней
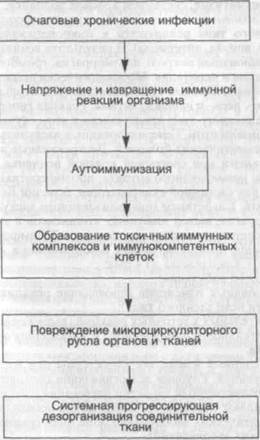
Патогенез ревматических болезней.Обусловлен возникающими иммунопатологическими реакциями в органах и тканях (схема 39). Очаг хронической инфекции вызывает напряжение и извращение иммунной реакции организма, в результате чего возникает аутоиммунизация, образуются токсичные иммунные комплексы и иммунокомпетентные клетки, повреждающие микро-циркуляторное русло тех или иных органов или тканей. Вследствие этого развертывается системная прогрессирующая дезорганизация соединительной ткани, являющаяся основным морфологическим проявлением ревматических заболеваний.
РЕВМАТИЗМ
• Ревматизм (болезнь Сокольского — Буйо) — инфекционно-аллергическое заболевание с преимущественным поражением сердца и сосудов, волнообразным течением, периодами обострения и затихания.
Этнология.Возбудителем является (i-гемолитический стрептококк группы А, который вызывает сенсибилизацию организма (повторные ангины). Большое значение в возникновении болезни имеют генетические факторы и возраст.
Патогенез.При ревматизме возникает сложный иммунологический ответ на присутствие возбудителя в сенсибилизированном организме. Следует отметить, что стрептококк имеет перекрестно реагирующие антигены с антигенами миоцитов сердца, поэтому продуцирующиеся в организме антитела направлены не только против антигенов стрептококка, но и против миоцитов сердца. Возникает процесс аутоиммунизации. Некоторые ферменты стрептококка разрушают окружающую миоциты соединительную ткань, в результате чего образуются антитела, направленные против соединительной ткани сердца.Появившиеся в крови иммунные комплексы и клетки-эффекторы повреждают микро-циркуляторное русло, попадают в окружающую соединительную ткань, подвергая ее фибриноидному изменению, вплоть до некроза. В результате некроза ткани освобождается тканевая тром-бокиназа, которая запускает систему свертывания крови, через тромбоциты активируется фактор пролиферации фибробластов. С другой стороны, некроз вызывает развитие макрофагальной клеточной реакции (характер реакции определяется особенностями антигена). Макрофаги, кроме осуществления фагоцитоза, вырабатывают ряд мембраноатакующих факторов: интерлей-кин-1, который активирует Т-лимфоциты, способствует хемотаксису нейтрофильных лейкоцитов; фактор пролиферации тромбоцитов, определяющий увеличение числа тромбоцитов на месте повреждения и усиливающий процессы свертывания крови; фак-
тор пролиферации фибробластов, способствующий пролиферации и созреванию фибробластов. В результате некроза образуется фактор некроза опухоли (ФНО), который углубляет процессы некроза ткани, повреждает эндотелий капилляров и таким образом способствует образованию микротромбов в области поражения, вызывает пролиферацию В-лимфоцитов, ответственных за образование циркулирующих антител. Пролиферация фибробластов в конечном итоге приводит к склерозу на месте повреждения. Все описанные изменения реализуются морфологически в виде сочетания реакций гиперчувствительности немедленного или замедленного типа. При ревматизме системная дезорганизация соединительной ткани (клапанов, стромы, пристеночного эндокарда и эпикарда) складывается из 4 фаз:
- мукоидного набухания (обратимый процесс);
- фибриноидных изменений (необратимый процесс);
- клеточной воспалительной реакции;
- склероза.
Мукоидное набухание и фибриноидные изменения вплоть до некроза являются выражением реакции ГНТ. Клеточная воспалительная реакция отражает гиперчувствительность замедленного типа. В результате клеточной реакции формируется гранулема, в центре которой располагается фибриноидный некроз, вокруг веерообразно располагаются клетки макрофа-гального типа с крупными гиперхромными ядрами. Гранулема, состоящая из таких крупных макрофагов, называется цветущей. В последующем клетки начинают вытягиваться, образуется большое количество фибробластов. Такая гранулема называется увядающей. В конечном итоге фибробласты замещают макрофаги, образуют большое количество коллагеновых волокон. Эту гранулему называют рубцующейся. Все описанные изменения гранулемы сопровождаются присутствием в окружающей ткани лимфоцитов и плазматических клеток.
Морфогенез ревматической гранулемы был подробно описан Л.Ашоффом (1904) и позднее В.Т.Талалаевым (1921), поэтому эту гранулему называют еще ашофф-талалаевской.
Гранулема располагается в соединительной ткани клапанов, пристеночного эндокарда, миокарда, эпикарда, адвентиции сосудов.
При ревматизме наблюдается также неспецифическая клеточная реакция, имеющая очаговый или диффузный характер. Эта реакция представлена лимфогистиоцитарными инфильтратами в строме различных органов. Кроме того, при ревматизме возникают распространенные васкулиты, которые рассматриваются как неспецифическая реакция. Васкулиты встречаются в различных органах и тканях.
Клинико-морфологические формы.В зависимости от преимущественного поражения того или иного органа различают 4 формы ревматизма: кардиоваскулярную, полиартритическую, нодоз-ную и церебральную.
Кардиоваскулярная форма. Эта форма наиболее частая, встречается как у взрослых, так и у детей. Основные проявления заболевания касаются сердца и сосудов. В соединительной ткани всех слоев сердца развиваются воспалительные и дистрофические изменения.
Эндокардит — главное проявление этой формы ревматизма. По локализации различают клапанный, хордальный, пристеночный эндокардит. Наиболее выраженные изменения обычно развиваются в створках левого предсердно-желудочкового (митрального) и аортального клапанов. Поражение створок правого предсердно-желудочкового (трехстворчатого) клапана встречается редко, сочетается с поражением митрального или аортального клапанов.
Выделяют 4 вида ревматического клапанного эндокардита: диффузный (или вальвулит), острый бородавчатый, фибропла-стический, возвратно-бородавчатый.
Диффузный эндокардит (вальвулит В.Т.Талалаева) характеризуется мукоидным набуханием, отеком соединительнотканной основы клапана, полнокровием капилляров. Эндотелий не поражен, тромботические наложения отсутствуют. При проведении лечения процесс обратим, структура клапанов восстанавливается полностью.
Острый бородавчатый эндокардит сопровождается не только мукоидным набуханием, но и фибриноидным некрозом соединительной ткани и эндотелия клапанов. Особенно сильно страдают края клапанов. В результате деструкции эндотелия создаются условия для образования тромбов, которые располагаются по краю клапана и представлены в основном фибрином (белый тромб). Тромботические наложения на клапанах называют бородавками.
Фибропластический эндокардит развивается как следствие двух предыдущих форм эндокардита и характеризуется преобладанием процессов склероза и рубцевания.
Возвратно-бородавчатый эндокардит проявляется процессами дезорганизации соединительной ткани в склерозированных клапанах. Обязательным компонентом этого эндокардита являются некроз эндотелия и образование на клапанах бородавок (тромботических наложений различного размера).
В исходе эндокардита развиваются склероз, гиалиноз клапанов, и формируется порок сердца.
Порок сердца при ревматизме представлен либо стенозом, либо недостаточностью клапанов. Наиболее часто встречается
комбинация этих видов пороков. Поражаются чаще всего митральный (75 %) и аортальный (до 25 %) клапаны. Нередко наблюдается сочетание митрального и аортального пороков сердца. В результате дистрофических изменений, некроза и склероза створки утолщаются, деформируются, срастаются, в них откладывается известь. Всегда отмечаются склероз и петрификация фиброзного кольца. Хорды клапанов утолщены, укорочены и склерозированы. Створки клапанов подтянуты к папиллярным мышцам. Отверстие клапанов обычно резко сужено, имеет вид рыбьей пасти (порок сердца типа "воронки"). Если преобладает недостаточность клапанов, то возникает порок типа "диафрагма", который всегда сопровождается выраженной рабочей гипертрофией левого желудочка сердца. Длительное существование у больного порока сердца приводит в конечном итоге к развитию острой или хронической сердечно-сосудистой недостаточности, которые являются причиной гибели больных.
Миокардит — одно из частых проявлений ревматизма. Выделяют 3 формы миокардита: узелковый (гранулематозный), диффузный интерстициальный (межуточный) экссудативный, очаговый интерстициальный (межуточный) экссудативный.
Узелковый миокардит характеризуется образованием гранулем в периваскулярной соединительной ткани различных отделов сердца. Гранулемы находятся в различных фазах развития: "цветущие", "увядающие", "рубцующиеся". В миоцитах отмечается различной степени выраженности белковая или жировая дистрофия. Узелковый миокардит заканчивается диффузным мелкоочаговым кардиосклерозом.
Диффузный интерстициальный экссудативный миокардит описан М.А.Скворцовым. Встречается преимущественно у детей, характеризуется диффузной инфильтрацией стромы лимфоцитами, гистиоцитами, нейтрофильными и эозинофильными лейкоцитами. Сосуды полнокровные, выражен отек стромы. Миокард теряет тонус, становится дряблым, полости сердца расширяются, поэтому клиническим проявлением этого миокардита всегда является тяжелая сердечно-сосудистая недостаточность. В исходе в миокарде развивается диффузный кардиосклероз.
Очаговый интерстициальный экссудативный миокардит имеет такие же морфологические проявления, что и диффузный, только процесс носит очаговый характер. Клинически протекает обычно латентно. В исходе возникает очаговый кардиосклероз.
Перикардит при ревматизме бывает серозным, фибринозным и серозно-фибринозным. При этом следует отметить, что для ревматизма характерен полисерозит. Перикардит заканчивается образованием спаек в полости перикарда. Иногда возможны полная облитерация полости перикарда и даже обызвествление фибринозных наложений (панцирное сердце).
При сочетании поражения всех слоев сердца при ревматизме говорят о панкардите, если поражены эндокард и перикард, то говорят оревматическом кардите.
Ревматические васкулиты, особенно микроциркуляторного русла, очень характерны. В артериях и артериолах развиваются фибриноидный некроз, тромбоз, пролиферация эндотелиальных и адвентициальных клеток. Проницаемость стенок сосудов повышена. Возможны диапедезные кровоизлияния и иногда более крупные кровоизлияния. В исходе ревматических васкулитов возникает артериосклероз.
Пол и артритическая форма ревматизма. Встречается у 10—15 % больных. Поражаются главным образом мелкие и крупные суставы. В полости суставов развивается се-розно-фибринозное воспаление. Синовиальная оболочка полнокровная, выражены васкулиты, пролиферация синовиоцитов, соединительная ткань подвергается мукоидному набуханию, в полости сустава формируется экссудат (обычно серозный). Суставной хрящ в процесс не вовлекается, поэтому при ревматизме деформации суставов обычно не наблюдается. Изменения других органов и тканей обычно выражены слабо, хотя отмечается выраженное в той или иной мере поражение сердца и сосудов.
Нодозная (узловатая) форма ревматизма. Встречается у детей. Характеризуется явлениями дезорганизации соединительной ткани в околосуставной области и по ходу сухожилий. В участках поражения обнаруживаются крупные очаги фибриноидного некроза, окруженные клеточной реакцией (лимфоциты, макрофаги, гистиоциты). Развивается так называемая нодозная эритема. При благоприятном течении на месте этих узлов образуются небольшие рубчики. В других органах у таких больных также находят характерные изменения, но яркая клиническая симптоматика отсутствует.
Церебральная форма ревматизма. Обусловлена развитием ревматического васкулита. Встречается у детей, называется малой хореей. Кроме ревматических васкулитов, особенно на уровне микроциркуляции, находят дистрофические и некробиотические изменения мозговой ткани, мелкие кровоизлияния. Поражение других органов и тканей представлено слабо, хотя всегда выявляется при целенаправленном обследовании.
Следует отметить, что при всех формах ревматизма имеет место заинтересованность иммунной системы, в которой выявляется гиперплазия лимфоидной ткани и плазмоклеточная трансформация.
Осложненияревматизма чаще всего связаны с развитием тромбоэмболического синдрома, обусловленного бородавчатым эндокардитом. При пороке сердца развивается сердечно-сосуди-
стая недостаточность, которая связана с декомпенсацией миокарда. Иногда различные осложнения может вызвать спаечный процесс в полостях перикарда, плевры, брюшной полости.
СИСТЕМНАЯ КРАСНАЯ ВОЛЧАНКА
• Системная красная волчанка (болезнь Либмана — Сакса) — системное заболевание с выраженной аутоиммунизацией, имеющее острое или хроническое течение и характеризующееся преимущественным поражением кожи, сосудов и почек.
Системная красная волчанка (СКВ) встречается с частотой 1 на 2500 здоровых людей. Болеют молодые женщины (90 %) в возрасте 20—30 лет, однако заболевание встречается также у детей и пожилых женщин.
Этиология.Причина возникновения СКВ неизвестна. В то же время накопилось много данных, которые указывают на глубокий полом иммунокомпетентной системы под влиянием вирусной инфекции (наличие вирусоподобных включений в эндотелии, лимфоцитах и тромбоцитах; персистенция вирусной инфекции в организме, определяемая с помощью антивирусных антител; частое присутствие в организме вирусов кори, парагриппа, краснухи и др. Способствующим фактором возникновения СКВ является наследственный фактор. Известно, что у больных СКВ чаще всего определяются антигены HLA-DR2, HLA-DR3, заболевание развивается у однояйцовых близнецов, у больных и их родственников снижена функция иммунокомпетентной системы. Неспецифическими провоцирующими факторами развития СКВ являются ряд лекарственных препаратов (гидразин, D-пеницилла-мин), вакцинация по поводу различных инфекций, ультрафиолетовое облучение, беременность и др.
Патогенез.Доказано, что у больных СКВ имеет место резкое снижение функции иммунокомпетентной системы, приводящее к извращению ее функции и образованию полиорганных аутоанти-тел. Основной полом касается процессов регуляции иммунологической толерантности за счет снижения Т-клеточного контроля -Аутоантитела и клетки-эффекторы образуются к компонентам клеточного ядра (ДНК, РНК, гистоны, различные нуклеопротеи-ды и др., всего насчитывается более 30 компонентов). Циркули рующие в крови токсичные иммунные комплексы и клетки-эф фекторы поражают микроциркуляторное русло, в котором воз никают преимущественно реакции гиперчувствительности не медленного типа, происходит полиорганное поражение opга низма.
Патологическая анатомия.Морфологический характер изме нений при СКВ очень разнообразен. Превалируют фибриноид ные изменения в стенках сосудов микроциркуляторного русла
ядерная патология, проявляющаяся вакуолизацией ядер, карио-рексисом, образованием так называемых гематоксилиновых телец; характерны интерстициальное воспаление, васкулиты (мик-роциркуляторное русло), полисерозиты. Типичным для СКВ феноменом являются волчаночные клетки (фагоцитоз нейтрофиль-ными лейкоцитами и макрофагами ядра клетки) и антинуклеар-ный, или волчаночный, фактор (антиядерные антитела). Все эти изменения сочетаются в различных взаимоотношениях в каждом конкретном наблюдении, определяя характерную клиническую и морфологическую картину заболевания.
Наиболее тяжело при СКВ поражаются кожа, почки и сосуды.
На коже лица отмечается красная "бабочка", которая морфологически представлена пролиферативно-деструктивными ва-скулитами в дерме, отеком сосочкового слоя, очаговой перива-скулярной лимфогистиоцитарной инфильтрацией. Иммуногисто-химически выявляются депозиты иммунных комплексов в стенках сосудов и на базальной мембране эпителия. Все эти изменения расцениваются как подострый дерматит.
В почках возникает волчаночный гломерулонефрит. Характерными признаками СКВ при нем являются "проволочные петли", очаги фибриноидного некроза, гематоксилиновые тельца, гиалиновые тромбы. Морфологически выделяются следующие типы гломерулонефрита: мезангиальный (мезангиопроли-феративный, мезангиокапиллярный) очаговый пролифератив-ный, диффузный пролиферативный, мембранозная нефропатия. В исходе гломерулонефрита может возникнуть сморщивание почек. В настоящее время поражение почек является основной причиной смерти больных СКВ.
Сосуды разного калибра подвергаются значительным изменениям, особенно сосуды микроциркуляторного русла — возникают артериолиты, капилляриты, венулиты. В крупных сосудах в связи с изменением vasa vasorum развиваются эла-стофиброз и эластолиз. Васкулиты вызывают вторичные изменения в органах в виде дистрофии паренхиматозных элементов, очагов некроза.
Всердце у части больных СКВ наблюдается абактериаль-ный бородавчатый эндокардит (эндокардит Либмана — Сакса), характерным признаком которого является наличие в очагах некроза гематоксилиновых телец.
В иммунокомпетентной системе (костный мозг, лимфатические узлы, селезенка) обнаруживаются явления плаз-матизации, гиперплазии лимфоидной ткани; в селезенке характерно развитие периартериального "луковичного" склероза.
Осложненияпри СКВ обусловлены в основном волчаночным нефритом — развитие почечной недостаточности. Иногда в свя-
зи с интенсивным лечением кортикостероидами и цитостатиче-скими препаратами могут возникнуть гнойные и септические процессы, "стероидный" туберкулез.
РЕВМАТОИДНЫЙ АРТРИТ
• Ревматоидный артрит (инфекционный полиартрит) — хроническое заболевание, основу которого составляет прогрессирующая дезорганизация соединительной ткани оболочек и хряща суставов, ведущая к их деформации.
В основном ревматоидным артритом болеют женщины (70 %) и дети (5—7 %), у мужчин это заболевание встречается редко.
Этиология и патогенез.Причина ревматоидного артрита (РА) неизвестна. Допускается, что источником заболевания являются В-гемолитический стрептококк, диплострептококк, микоплазма, вирус Эпштейна — Барр. Персистирующая инфекция приводит к повреждению синовиальной оболочки, оголению антигенов кол-лагеновых волокон, на которых развивается гуморальная и клеточная реакции. Условием, определяющим реализацию инфекции, является наличие антигенов HLA-B27, В8, HLA-DR4,3. Известно, что у носителей этих генов гистосовместимости риск заболевания увеличивается в десятки раз.
Гуморальная иммунная реакция представлена образованием аутоантител, относящихся к классу IgM, возможно IgG, IgA, IgD, направленных к собственному IgG. Эти аутоантитела называют ревматоидным фактором. Он продуцируется в синовио-цитах, клетках инфильтратов суставов, обнаруживается в синовиальной жидкости, крови в виде циркулирующего иммунного комплекса. Присоединение к такому иммунному комплексу компонентов комплемента СЗ или С5 определяет его повреждающее действие на синовиальную оболочку и на микроциркуляторное русло, а также хемотаксис нейтрофильных лейкоцитов. Эти же комплексы взаимодействуют с макрофагами и моноцитами, активируют синтез ими интерлейкина-1, простагландинов Е, фактора пролиферации фибробластов и тромбоцитов, которые способствуют образованию коллагеназы синовиоцитами, процессам некроза и склероза. Иммунный комплекс, циркулируя в крови и фиксируясь в микроциркуляторном русле, вызывает генерализованные васкулиты в органах и тканях.
Клеточная иммунная реакция представлена выраженной инфильтрацией оболочек суставов лимфоцитами (преимущественно Т4), макрофагами, В-лимфоцитами, вплоть до формирования лимфоидных фолликулов. Эти клетки принимают активное участие в поддержании гуморальной иммунной реакции и участвуют в реакции клеточного цитолиза.
Клинико-морфологическивыделяют следующие формы ревматоидного артрита: - Ревматоидный артрит взрослых; - Ювенильный хронический полиартрит: полиартритическая форма; системная висцеральная форма; моноартритическая форма; - Особые формы:
болезнь Бехтерева;
болезнь Стилла;
аллергический субсепсис Висслера — Фанкони;
синдром Фелти;
синдром Рейтера.
Патологическая анатомия.Основные изменения при РА возникают в суставах. Развивается прогрессирующая дезорганизация соединительной ткани, в синовиальной оболочке — синовит.
Выделяют три стадии синовита.
В первой стадии синовита в полости сустава образуется серозная жидкость, содержащая большое количество белка и нейтрофильные лейкоциты, которые называют рагоцитами. Нейтрофильные лейкоциты при разрушении освобождают про-теазы, которые способствуют лизису ткани и прогрессированию процесса. Синовиальная оболочка набухшая, полнокровная. Ворсины отечные, в них определяются участки мукоидного и фибри-ноидного набухания, вплоть до некроза. Ворсины, подвергшиеся некрозу, отделяются, попадают в полости суставов и из них образуются "рисовые тельца". Сосуды синовиальной оболочки окружены макрофагами, лимфоцитами, нейтрофильными лейкоцитами, плазматическими клетками, в их стенках обнаруживаются фибриноид и иммунные комплексы. Синовиоциты ворсин проли-ферируют. Суставной хрящ в эту стадию сохранен. Первая стадия продолжается месяцы, иногда годы.
Во второй стадии синовита происходит разрастание ворсин: усиливается пролиферация синовиоцитов, в стро-ме — инфильтрация лимфоцитами, плазматическими клетками, формируются лимфоидные фолликулы, в стенках сосудов выражено пролиферативное воспаление. По краям суставных концов костей постепенно образуется грануляционная ткань, пронизанная лимфоидными, плазматическими клетками, макрофагами, нейтрофильными лейкоцитами. Эта ткань в виде пласта — паннуса — наползает на синовиальную оболочку, разрушая ворсины, и на гиалиновый хрящ, который истончается; костная поверхность эпифизов обнажается, развивается остеопороз эпифизов костей. Грануляционная ткань резко сужает суставную щель, наблюдается тугоподвижность суставов, легко возникают вывихи или подвывихи.
Третья стадия синовита характеризуется появлением фиброзно-костного анкилоза. Развивается у больных через 15—30 лет от начала заболевания. Особенностью изменений в третьей стадии является продолжающееся прогрессирование процесса в суставах, что приводит к полной обездвиженности больных. Характерно образование в околосуставной соединительной ткани ревматоидных узлов, представляющих собой очаги фибриноидного некроза, окруженные гистиоцитами, макрофагами, гигантскими клетками рассасывания. Размеры очагов могут достигать величины лесного ореха и часто рассматриваются в клинике как опухоль.
Висцеральные изменения при РА представлены полисерозитами, в почках возникает гломерулонефрит. Довольно часто отмечаются васкулиты в легких, сердце. В качестве осложнений наблюдается пиелонефрит, амилоидоз (АА) внутренних органов. Изменения костного мозга, селезенки и лимфатических узлов характеризуются выраженной плазмотизацией и гиперплазией лимфоидной ткани.
Смерть больных чаще всего возникает от почечной недостаточности, обусловленной амилоидозом, или присоединения вторичной инфекции: пневмонии, сепсиса, туберкулеза и др.
