Изоосмоляльная гипергидратация
Для изоосмоляльной гипергидратации характерно увеличение объема внеклеточной жидкости нормальной осмоляльности.
Причины изооосмоляльной гипергидратации:
¾ инфузия больших количеств изотонических растворов (0,9% раствора Na Cl, 10% раствора глюкозы и др.) при неправильной коррекции водно-электролитных нарушений;
¾ сердечно-сосудистая недостаточность, ведущая к увеличению объемов внутрисосудистого и межклеточного секторов;
¾ гипоксия и интоксикация, вызывающие повышение сосудистой проницаемости и фильтрации жидкости в ткани (при некоторых инфекциях, токсикозе беременных);
¾ уменьшение содержания белка в плазме крови при нарушении его поступления в организм (голодание), синтеза в печени при ее недостаточности, потере белка с мочой (нефротический синдром), что обуславливает выход жидкости из сосудов в ткани;
¾ затруднение лимфооттока (закупорка лимфососудов, метастазы в лимфоузлах и лимфососудах).
Клинические проявления.
В условиях нормального функционирования системы регуляции водного обмена развивающаяся легкая или умеренная гипергидратация может сравнительно быстро разрешиться вследствие включения механизмов компенсации. Последние направлены на удаление воды из организма прежде всего путем усиления диуреза, например за счет торможения продукции и секреции АДГ. При выраженной гипергидратации клиническая картина зависит от гиперволемии и развития отеков (рис. 10).
Увеличение объема крови — гиперволемия и повышение АД, сохраняющиеся в течение длительного времени — вызывают перегрузку сердца, развитие сердечной недостаточности и отека легких. При остро развивающейся гипергидратации может возникать серьезная угроза в виде отека мозга и последующего коматозного состояния. Увеличение жидкости в интерстициальном пространстве характеризуется образованием отеков различных тканей, патогенез которых связан с нарушениями гемо- и лимфодинамики, снижением величины КОД (гипоонкией), повышением проницаемости клеточных мембран. Для больного характерны симптомы сердечной недостаточности и отеков различных органов.
Лабораторные показатели:
¾ осмоляльность плазмы в пределах нормы;
¾ повышение ОЦК, АД, ЦВД;
¾ снижение уровня белка в плазме крови;
¾ уменьшение Ht, Hb.

Отек
Внеклеточная гипергидратация нередко проявляется в виде системных отеков.
Отек — это расстройство водного баланса, проявляющееся скоплением избытка жидкости в межклеточном пространстве и в полостях тела.
Различают отечную жидкость невоспалительного генеза, бедную белком (менее 2%), называемую «транссудат», и отечную жидкость, выходящую из сосудистого русла в ткани при воспалении, богатую белком (более 3%) и форменными элементами крови, — «экссудат».
Таблица 13. Классификация отеков
| Принцип классификации | Виды отеков |
| По патогенезу (основной патогенетический фактор) | — гидростатический — лимфогенный — онкотический — осмотический — мембраногенный |
| По распространенности | — местный (например, при воспалении в месте его развития) — общий (например,гипопротеинемический при белковой недостаточности) |
| По локализации | — анасарка (тотальный отек подкожной клетчатки тела) — водянка (скопление транссудата в полости тела) — асцит — в брюшной полости — гидроторакс — в плевральной полости — гидроперикард — в околосердечной сумке — гидроцеле — между листками серозной оболочки яичка — гидроцефалия — в желудочках мозга и в субарахноидальном и субдуральном пространствах |
| По скорости развития | — молниеносный (в течение секунд; например, после укуса насекомых) — острый (в течение часа; например, отек легких при остром инфаркте миокарда) — хронический (в течение нескольких суток или недель; например, отек при голодании) |
Механизмы возникновения отека
Согласно теории Э. Старлинга, обмен воды между внутрисосудистым и межклеточным пространствами зависит от:
— эффективного гидростатического давления (ЭГД), т. е. разности между гидростатическим давлением крови в микрососудах (в артериальном конце капилляра кожи человека — 30–32 мм. рт. ст., в венозном конце — 8–10 мм рт. ст.) и гидростатическим давлением межклеточной жидкости (–6 мм рт. ст.). Следовательно, в норме ЭГД в артериальной части составляет ≈36 мм рт. ст. [30–(–6)], в венозной — 14 мм рт. ст.[8–(–6)];
— эффективной онкотической всасывающей силы (ЭОВС) крови, т. е. разности между онкотическим давлением крови (25–28 мм рт. ст.) и онкотическим давлением интерстициальной жидкости (≈5 мм. рт. ст.), составляющей 20–23 мм рт. ст.;
— проницаемости стенки обменных микрососудов для воды и белков.
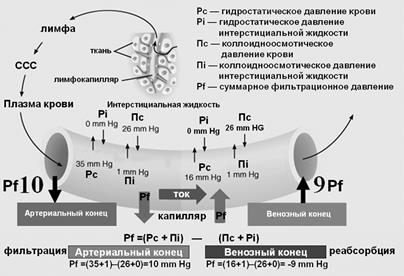
Рис. 11. Закон Франка–Старлинга
В норме в артериальной части микрососудов ЭГД превышает ЭОВС крови (36–25=13), вследствие чего происходит фильтрация воды из сосудов в межклеточное пространство. В венозной части микрососудов, напротив, ЭГД меньше ЭОВС (14–23=–9), в силу чего происходит резорбция жидкости из интерстиция в сосудистое пространство (рис. 11).
Очевидно, что нарушение обмена воды между кровью и интерстициальной жидкостью с развитием отека будет определяться изменением величин ЭГД и ЭОВС и их соотношением в разных отделах микрососудов, а также повышением проницаемости стенок последних.
Гидростатический фактор
При патологии, когда происходит увеличение ЭГД крови и оно превышает ЭОВС крови, развивается механический, или застойный, отек. Наиболее частыми причинами увеличения ЭГД являются повышение венозного давления вследствие нарушения центральной гемодинамики (сердечная недостаточность) или вследствие местного венозного застоя (обтурация венозного сосуда тромбом, сдавление вен опухолью, рубцом) и увеличение ОЦК (гиперволемия, общая гипергидратация организма — водное отравление). Повышение ЭГД в венозном отделе микрососудистого русла тормозит резорбцию воды из интерстиция, что обуславливает накопление ее в межклеточном пространстве, т. е. развитие отека.
Лимфогенный фактор
Затруднение оттока лимфы, который в норме обеспечивает отведение воды и белков из межклеточного пространства и возвращение их в кровяное русло, может быть вызвано механическим препятствием, например, сдавлением лимфососудов (опухолью, рубцом и т. д.) или их обтурацией (эмболия кусочками тромба, паразитами, опухолевыми клетками), спазмом лимфососудов. При этом формируется отек с выраженным увеличением массы ткани. Например, при закупорке лимфососудов филяриями возникает отек конечностей, масса ноги при этом может достигать 50 кг (слоновость).
Повышение давления в системе верхней полой вены (правожелужочковая недостаточность) сопровождается прессорным рефлексом на лимфатические сосуды организма, что затрудняет отток лимфы из тканей. Развитие отека может быть связано с динамической лимфатической недостаточностью. Она возникает при избыточном лимфообразовании, когда лимфатические сосуды не справляются с транспортом избыточного объема лимфы в общий кровоток. Такая ситуация возникает, например, у больных с нефротическим синдромом, когда вследствие выраженной гипопротеинемии (менее 40 г/л ) резко снижается ЭОВС крови и увеличивается выход воды из сосудов в ткань, что приводит к резкому увеличению лимфообразования.
Онкотический фактор
Уменьшение содержания белков в плазме крови — гипопротеинемия, особенно снижение высокогидрофильных альбуминов — гипоальбуминемия — определяет снижение величины онкотического давления крови. Гипоальбуминемия возникает в результате недостаточного поступления белков с пищей (общее или белковое голодание) или нарушения их переваривания и всасывания (например, при резекции части кишечника, синдроме мальабсорбции); при снижении синтеза альбумина в печени (например, при циррозе печени); вследствие потери альбуминов через почки (например, при нефротическом синдроме), через ЖКТ (диарея), через кожу (обширные ожоги, экссудативные кожные заболевания).
Снижение онкотического давления крови вызывает уменьшение ЭОВС плазмы крови, что ведет к усилению фильтрации воды из артериального отдела микрососудов в интерстициальную жидкость и к уменьшению резорбции воды из интерстиция в венозный отдел микрососудов, следствием чего является формирование отека. Гипопротеинемические отеки имеют генерализованный характер.
Осмотический фактор
Проявляется в снижении осмоляльности плазмы крови и/или повышении осмоляльности межклеточной жидкости. Уменьшение осмотического давления крови может быть результатом гемодилюции при инфузии пациентам избыточных количеств гипотонических растворов, например с целью коррекции дегидратации организма. Однако при нормально функционирующих почках избыток воды быстро выводится из организма. Гипоосмия плазмы крови может возникать при повышении секреции АДГ, вызывающего задержку воды в организме.
Повышение осмоляльности интерстициальной жидкости возникает:
— при поступлении в нее осмотически активных веществ (катионов K, Na, Ca; глюкозы, азотистых метаболитов), освободившихся из поврежденных или разрушеных клеток;
— при усилении диссоциации солей и органических веществ в интерстициальной жидкости вследствие гипоксии и ацидоза;
— при снижении оттока крови по венулам (уменьшение оттока осмотически активных веществ);
— при перемещении Na+ из плазмы крови в интерстициальное пространство по градиенту концентрации (например при гиперальдостеронизме).
Во всех перечисленных случаях вода переходит из сосудов в область более высокого осмотического давления — интерстициальное пространство.
Мембраногенный фактор, или повышение проницаемости стенок микрососудов для воды и белков плазмы крови, имеет определяющее значение в развитии мембраногенного отека.
Непосредственными причинами повышения проницаемости стенок микрососудов в этих случаях выступают ацидоз, вызывающий неферментный гидролиз основного вещества базальной мембраны сосудов и ее разрыхление, а также ферментативный гидролиз компонентов базальной мембраны гидролитическими, преимущественно лизосомными ферментами; вазоактивные медиаторы воспаления (например, гистамин путем увеличения межэндотелиальных щелей, кинины, эйкозаноиды и др.); гипоксия и механическое перерастяжение клеток микрососудов (например, при венозном застое).
Повышение проницаемости стенок микрососудов облегчает фильтрацию воды из сосуда в интерстиций, однако этот процесс может уравновешиваться усилением реабсорбции воды в венозном отделе капилляров. Поэтому решающим фактором является повышение проницаемости стенки микрососудов для плазменных белков и усиление их транспорта в интерстиций. Это приводит к гиперонкии межклеточной жидкости, гипоонкии крови и, следовательно, снижению величины ЭОВС, т. е. задержке воды в межклеточном пространстве.
В патогенезе различных видов отеков значение перечисленных факторов неодинаково, и они выступают в различных комбинациях. Заметим, что в механизме развития любого отека, встречающегося при различных патологических состояниях, участвует обычно несколько патогенетических факторов, из которых один является первичным (запускающим процесс), тогда как другие факторы присоединяются в процессе развития отека вторично. Например, первичным фактором мембраногенного отека является повышение проницаемости стенок микрососудов, однако весьма значимой является роль онкотического и осмотического факторов (гиперонкия и гиперосмия межклеточной жидкости), усиливающих действие первичного фактора.
В патогенезе отеков при сердечной недостаточности первичным фактором является гидростатический, проявляющийся в системном повышении венозного давления вследствие снижения сократительной функции сердца. Повышение венозного давления и, как следствие, увеличение ЭГД в венозной части капилляров вызывает уменьшение резорбции жидкости из межклеточного пространства. Вторично присоединяются и другие патогенетические факторы отека:
осмотический — за счет альдостеронзависимой и независимой реабсорбции Na+ в канальцах почек, задержки его в тканях и повышения в них осмотического давления, а также за счет нарушения оттока из ткани осмотически активных веществ (в результате венозного застоя);
онкотический — за счет гипоальбуминемии, обусловленной торможением белкового синтеза в печени (вследствие застоя в ней крови) и усилением выхода альбуминов в интерстициальное пространство (вследствие повышения проницаемости стенок микрососудов в условиях гипоксии), что приводит к снижению ЭОВС и, следовательно, отеку;
мембраногенный — повышение проницаемости стенок микрососудов для белка, обусловленной повышением циркуляторной гипоксии и ацидоза;
лимфогенный — за счет развития механической лимфатической недостаточности, обусловленной увелечением венозного давления, центрального и в периферических венозных сосудах, что увеличивает объем интерстициальной жидкости и таким путем степень отека.
Таким образом, в развитии отека при сердечной недостаточности участвуют все патогенетические факторы отека, и именно их сочетание и взаимоусиливающее действие обеспечивают его формирование.
ГЛАВА 5.
