Количественное определение. Прозрачная бесцветная жидкость со своеобразным острым запахом
Описание
Прозрачная бесцветная жидкость со своеобразным острым запахом. Смешивается во всех соотношениях с водой и спиртом.
Подлинность.
Теоретическая часть
Подтверждение подлинности основано на реакции взаимодействии формальдегида с фенолами в присутствии серной кислоты, в результате чего образуются окрашенные продукты. В качестве реактива в данном случае берут производное фенола – 2-гидроксибензойную кислоту (салициловую кислоту).
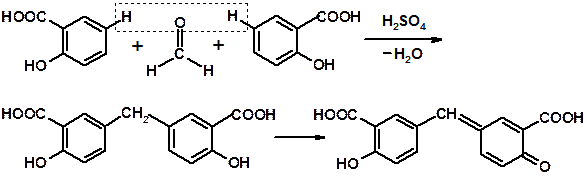
Другая характерная реакция основана так называемой реакции «серебряного зеркала».
2[Ag(NH3)2]OH + HCОH = 2Ag + HCOONH4 + 3NH3 + H2O
Ход анализа
1. К раствору, состоящему из 0,02 – 0,03 г салициловой кислоты в 5 мл концентрированной серной кислоты прибавить 2 капли препарата и нагреть, появляется красное окрашивание.
2. К 2 мл аргентум нитрата прибавить 10-12 капель раствора аммиака и 2-3 капли препарата, нагреть на водяной бане с температурой 50 - 60ºС. Выделяется металлическое серебро в виде зеркала или серого осадка.
Содержание муравьиной кислоты в препарате.
Теоретическая часть
В растворе формальдегида возможна примесь муравьиной кислоты, которая может образовываться при получении формальдегида. Присутствуя в формальдегиде, муравьиная кислота способствует полимеризации формальдегида в параформ (СН2О)n и выпадению параформа в осадок, особенно в присутствии окислов металлов (Fe, Cu и др.). Поэтому устанавливается допустимый предел кислотности в препарате, а для предупреждения возможных окислительно-восстановительных процессов и для стабилизации препарата к нему добавляют метиловый спирт (не более 1%).
Ход анализа
В конической колбе вместимостью 25 мл взвешивают 10 см3 препарата (точная навеска) и титруют раствором натрия гидроксида с молярной эквивалентной концентрацией 0,1моль/дм3 в присутствии до розового окрашивания (индикатор - фенолфталеин). 1 см3 раствора натрия гидроксида соответствует 0,0046 г муравьиной кислоты, которой в препарате должно быть не более 0,2%.
Количественное определение
Теоретическая часть
Количественное определение формальдегида основано на окислении его избытком йода в щелочной среде в муравьиную кислоту, с последующим оттитровыванием избытка йода раствором натрия тиосульфата.
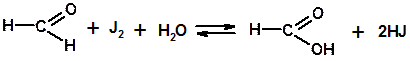
Так как данная реакция обратима, выделяющиеся кислоты нейтрализуют щелочью. Но с щелочью реагирует и йод с образованием гипойодида и йодида:
J2 + 2NaOH → NaJ + NaOJ + H2O
Образование гипойодида дает возможность окисления формальдегида:

При стоянии гипойодид переходит йодат:
3NaOJ → 2NaJ + NaJO3
После того, как формальдегид окислится, добавляют серную кислоту, которая вытесняет йод из оставшихся солей (NaOJ и NaJO3) и эквивалентного им количества йодида натрия.
NaJ + NaOH + H2SO4 → Na2SO4 + J2 + H2O
5NaJ + NaJO3 + 3 H2SO4 → 3Na2SO4 + 3J2 + 3H2O
Выделившийся йод титруют раствором натрия тиосульфата:
J2 + Na2S2O3 → 2NaJ + Na2S2O6
Ход анализа
Около 1 г препарата (точная навеска) перенести в мерную колбу вместимостью 100 см3 довести объём раствора водою до метки. Для анализа в коническую колбу отобрать 5 см3 приготовленного раствора , добавить 20 см3 раствора J2 с молярной эквивалентной концентрацией 0,1 моль/дм3 и 10 см3 раствора NaOH с молярной эквивалентной концентрацией 0,1 моль/дм3, взбалтывают и оставляют в темном месте на 10 минут.
Затем прибавляют 11 см3 раствора серной кислоты и выделившийся йод титруют раствором Na2S2O3 с молярной эквивалентной концентрацией 0,1 моль/дм3 до обесцвечивания раствора (индикатор крахмал).
Расчеты
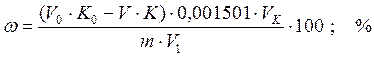
где V0 – объем J2, который добавили к раствору, см3;
К0 – поправочный коэффициент для приведения J2 до точной концентрации 0,1 моль/дм3;
V – объем раствора Na2S2O3, пошедший на титрование, см3;
К – поправочный коэффициент для приведения Na2S2O3 до точной концентрации 0,1 моль/дм3;
VK – объем мерной колбы, в которой растворяли навеску препарата, см3;
m – масса препарата, взятого для анализа, г;
V1 – аликвота раствора препарата, взятая для анализа, см3.
0,001501 – масса СН2О, которая соответствует 1 см3 раствора J2 с молярной эквивалентной концентрацией 0,1 моль/дм3, г.
Содержание СН2О в препарате должно быть 36,5 – 37,5%.
Реактивы и оборудование.
1. Колбы мерные на 100 см3.
2. Колбы конические на 25 см3.
3. Бюретки на 25 см3
4. Пипетки на 1,2, 10 и 20 см3
5. Раствор J2 с молярной эквивалентной концентрацией 0,1 моль/дм3
6. Раствор Na2S2O3 молярной эквивалентной концентрацией 0,1 моль/дм3
7. Раствор индикатора фенофталеина.
8. Раствор натрия гидроксида с молярной эквивалентной концентрацией 0,1моль/дм3.
9. Раствор аргентум нитрата
10. Раствор аммиака.
11. Кислота серная концентрированная.
12. Салициловая кислота.
Приготовление растворов для анализов:
1. Раствор аргентум нитрата. 20 г аргентум нитрата растворяют в воде и разбавляют раствор водой до 1 дм3.
2. Раствор аммиака. 440 мл концентрированного раствора аммиака разбавляют водой до 1 дм3.
2. Раствор индикатора фенолфталеина. 1г фенолфталеина растворяют в спирте и разбавляют водой до 1 дм3 и фильтруют.
3. Раствор крахмала. 1 г крахмала растирают в ступке с 5 мл воды до получения однородной кашицы и смесь медленно вливают при постоянном помешивании в 100 мл кипящей воды. Кипятят в течение 2-3 минут до получения слегка опалесцирующей жидкости. Срок хранения раствора 2-3 дня.
Вопросы для самостоятельного изучения(письменно)
1. На чем основано применение раствора формальдегида как дезинфицирующего средство.
2. Благодаря какому свойству формальдегида, его растворы применяются для консервации анатомических и биологических препаратов.
3. Почему раствор формальдегида нельзя хранить при температуре ниже 9ºС.
4. Для п.3 данной лабораторной работы привести формулу для расчета содержания муравьиной кислоты в препарате, в % масс.
