Применение реакции нейтрализации в фармакотерапии.
Для проведения коррекции кислотно-основного состояния необходимо выявить, какое звено в его регулировке нарушено. Для этого необходимо определить значения рН биологических жидкостей и содержание буферных оснований.
В основе фармакологических действий лежит реакция нейтрализации.
Например, в качестве экстренной меры при ацидозе применяется внутривенное вливание раствора гидрокарбоната натрия 4,5%, а в острых случаях – 8,4%. Второе эффективное средство – трисамин 3,66%, который связывает избыточные протоны. Он эффективен только при внутривенном введении. Также в качестве средства, коррегирующего ацидоз, используют лактат натрия 11% раствор.
Для устранения явления алкалоза в некоторых случаях используют раствор аскорбиновой кислоты 5%. В гастроэнтерологии применяют средства, нормализующие секреторную функцию желудка. При пониженной кислотности желудочного сока назначают разбавленную соляную кислоту, при повышенной кислотности – различные антацидные препараты: оксид магния, основной карбонат магния, карбонат кальция, гидрокарбонат натрия.
Вопросы для самоконтроля
1. Какие растворы называются буферными растворами ?
2. Классификация буферных растворов.
3. Механизм буферного действия.
4. Уравнение Гендерсона – Гассельбаха для определения рН и рОН протолитических буферных растворов.
5. Факторы, влияющие на рН и рОН буферных растворов.
6. Буферная ёмкость.
7. Зона буферного действия.
8. Количественное определение буферной ёмкости.
9. Буферные системы крови: гидрокарбонатная, фосфатная, гемоглобиновая и протеиновая.
10. Взаимодействие буферных систем в организме.
11. Кислотно-основное равновесие.
12. Основные показатели КОР
13. Возможные причины и типы нарушений КОР организма
Упражнения.
1. Константа диссоциации NH4OH равна 1,8 · 10-5. Можно ли приготовить аммиачный буфер с рОН = 4,7
2. Можно ли приготовить ацетатный буфер с рН = 5,4, если Кд (СН3СООН) = 1,6 · 10 -7?
3. Рассчитайте рОН буфера, состоящего из 50 мл 0,1 н р-ра СН3СООН и 100 мл 0,01 н р-ра СН3СООNa, если рК = 4,7.
4. Рассчитайте рН буфера, состоящего из 40 мл 0,2 н р-ра NH4ОН и 80 мл 0,01 н р-ра NH4CI, если рК = 4,4.
5. Для приготовления буфера взяты 50 мл 2 н р-ра NH4ОН и 100 мл 0,1 н р-ра NH4С1 (рК = 4,4). Как изменится рОН этого раствора, если к нему добавить: а) 10 мл р-ра 0, 1 н НС1, б) 200 мл воды ?
6. Для приготовления ацетатного буфера взяты 100 мл 0,01 н р-ра СН3СООН и 50 мл 0,01 н р-ра СН3СООNa, (рК = 4,7). Как изменится рОН этого раствора, если к нему добавить: а) 25 мл 0,1н р-ра NaОН, б) 25 мл воды?
7. Рассчитайте буферную ёмкость буфера, состоящего из 0,05 моль/экв соли и 0,1 моль/экв кислоты, если к 1 л этого буфера добавить 20 мл 0,5 N р-ра НС1 (рК к-ты = 4,7).
8. Какова буферная ёмкость фосфатного буфера, если при добавлении 3 мл 0,1 н р-ра НСI К 20 мл этого буфера рН меняется от 7,4 до 7,1 ?
Лабораторные работы
Работа 1. Определение буферных свойств биологических жидкостей
Опыт 1 В четыре одинаковые пробирки с помощью пипетки отмерить по 1 мл сыворотки крови. Первую пробирку оставить для контроля, во вторую добавить 5 кап. 0,025 N раствора NаОН, в третью - 0,025 N раствора НСl, в четвёртую – 5 кап. воды. Затем во все пробирки добавить по 1-2 капли универсального индикатора и по цветной шкале универсального индикатора определите приблизительное значение рН.
Опыт 2. В четыре одинаковые пробирки с помощью пипетки отмерить по 1 мл ацетатного буфера. Первую пробирку оставить для контроля, во вторую добавить 5 кап. 0,025 N раствора NаОН, в третью - 0,025 N раствора НСl, в четвёртую – 5 кап. воды. Затем во все пробирки добавить по 1-2 капли универсального индикатора и по цветной шкале универсальног индикатора определите приблизительное значение рН.
Опыт 3. В две одинаковые пробирки с помощью пипетки отмерить: в первую – 5 кап. воды, во вторую 5 кап. слюны. Добавить в каждую пробирку по 1-2 капли универсального индикатора и определить примерное значение рН. Затем добавить в обе пробирки по 1 капли 0,01 N раствора НСl. Что наблюдаете? Охарактеризуйте буферные свойства слюны.
Результаты опытов занесите в таблицу № 1.
Таблица № 1.
| Исследуемый раствор | Значение рН по универсальному индикатору | Вывод об изменении рН раствора | |||
| Контрольный раствор | После добавления НСl | После добавления NаОН | После добавления воды | ||
| 1. Сыворотка крови 2. Ацетатный буфер 3. Слюна |
Зависимость рН буферных растворов от соотношения компонентов
Опыт 1. В три пробирки с помощью пипетки отмерить 0,2 N Nа2НРО4 и 0,2 N NаН2РО4 в количествах, указанных в таблице № 2. добавьте в каждую пробирку по две капли универсального индикатора и определите рН по цветной шкале универсального индикатора.
Вычислите рН исследуемых растворов по формуле Гендерсона – Гассельбаха:
рН = рК + ℓg 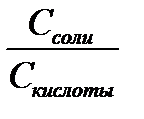 , Кд (Н2РО4-) = 1,5 · 10-7
, Кд (Н2РО4-) = 1,5 · 10-7
Сделайте вывод зависимости рН от соотношения концентраций компонентов буферной смеси.
Таблица № 2.
| № | Кол-во мл 0,2 N Nа2НРО4 | Кол-во 0,2 N NаН2РО4 | Соотношение Nа2НРО4 / NаН2РО4 | рН по индикатору | рН по формуле |
| 1. 2. 3. | 0,2 1,1 2,0 | 2,0 1,1 0,2 |
Тесты для самоконтроля.
ТЕСТ 1
1. Буферные растворы можно приготовить из:
а) HNO3 и КОН, б) СН3СООН и NaOH,
в) HCl и KNO3, г) NH4OH и H2S
2. Щелочной резерв крови определяется количеством мл СО2 в объёмных % в расчете на:
а) 1000 мл, б) 100 мл, в) 10 мл, г) 1,0 мл сыворотки крови.
3. Буферная ёмкость количественно определяется:
а) моль/экв сильной кислоты или основания, которое нужно добавить к 1 л буферного раствора, чтобы изменить его рН на единицу;
б) моль/л сильной кислоты или основания, которое нужно добавить к 1 л буферного раствора, чтобы изменить его рН на единицу;
в) числом мл слабой кислоты или основания, которое нужно добавить к 1 л буферного раствора, чтобы изменить его рН на единицу;
г) числом мл сильной кислоты или основания, которое нужно добавить к 1 л буферного раствора, чтобы изменить его рН.
4. рН буферной системы зависит от:
а) концентрации компонентов, б) объёма буфера,
в) разведения, г) соотношения концентрации компонентов.
5. При рН = 7,4 соотношение компонентов бикарбонатного буфера H2CO3/NaHCO3:
а) 1:20, б) 20:1, в) 1:1, г) 1:5
ТЕСТ 2
1. При компенсированном алкалозе:
а) рН = 7,4, щелочной резерв 55 объемных %,
б) рН = 7,2, щелочной резерв 70 объемных %,
в) рН = 7,4, щелочной резерв 70 объемных %,
г) рН = 7,4, щелочной резерв 40 объемных %.
2. рН буферной системы зависит от:
а) объёма буфера, б) концентрации компонентов,
в) разведения, г) соотношения концентраций компонентов
3. При нейтрализации ионов водорода в почечной ткани принимает участие буферная система:
а) бикарбонатная, б) фосфатная,
в) гемоглобиновая, г) ацетатная.
4. Щелочной резерв крови – это количество мл СО2, находящегося в 100 мл сыворотки крови. В норме оно равно:
а) 24%, б) 55%, в) 35%, г) 76%.
5. При разведении буферная ёмкость уменьшается, так как:
а) не изменяется соотношение компонентов,
б) увеличивается объём,
в) уменьшается концентрация,
г) изменяется соотношение компонентов.
ТЕСТ 3
1. Буферные растворы можно приготовить из:
а) HCl и KOH, б) NH4OH и HCl,
в) NH4OH и H2S, г) KOH и H2SO4
2. При добавлении к аммиачному буферу НСl рН не меняется так как, в соответствии с законом разбавления Оствальда степень диссоциации слабого электролита:
а) увеличивается б) уменьшается
в) не изменяется г) сначала увеличивается, а затем уменьшается.
3. Константа диссоциации NH4OH равна 1,8 · 10-5. Зона буферного действия будет находится в интервале рОН :
а) 3,8 – 5,8, б) 2 – 4, в) 4,8 – 5,8, г) 2,8 – 4,8
4. При разведении в 10 раз буферного раствора рН:
а) уменьшается, б) увеличивается
в) не изменяется, г) сначала уменьшается, а затем увеличивается
5. В норме парциальное давление равно:
а) 60 мм рт.ст б) 20 мм рт.ст,
в) 50 мм рт.ст г) 40 мм рт.ст
ТЕСТ 4
1. Буферные растворы можно приготовить из:
а) HNO3 и КОН, б) СН3СООН и NaOH,
в) HCl и KNO3, г) NH4OH и H2S
2. Щелочной резерв крови определяется количеством мл СО2 в объёмных % в расчете на:
а) 1000 мл, б) 100 мл, в) 10 мл, г) 1,0 мл сыворотки крови.
3. Константа диссоциации СН3СООН равна 1,8 · 10-5. Зона буферного действия будет находится в интервале рОН :
а) 3,8 – 5,8 б) 2 – 4
в) 4,8 – 5,8 г) 2,8 – 4,8
4. При нейтрализации ионов водорода в почечной ткани принимает участие буферная система:
а) бикарбонатная, б) фосфатная,
в) гемоглобиновая, г) ацетатная.
5. При компенсированном ацидозе:
а) рН = 7,4, щелочной резерв 55 объемных %,
б) рН = 7,2, щелочной резерв 70 объемных %,
в) рН = 7,4, щелочной резерв 70 объемных %,
г) рН = 7,4, щелочной резерв 40 объемных %.
ТЕСТ 5
1. При добавлении к ацетатному буферу NaOH рН не меняется так как, в соответствии с законом разбавления Оствальда степень диссоциации слабого электролита:
а) увеличивается б) уменьшается
в) не изменяется г) сначала увеличивается, а затем уменьшается
2. Буферные растворы можно приготовить из:
а) HCl и KOH, б) NaOH и H3PO4,
в) NH4OH и H2S, г) KOH и H2SO4
3. В норме парциальное давление равно:
а) 60 мм рт.ст б) 20 мм рт.ст,
в) 50 мм рт.ст г) 40 мм рт.ст
4. При разведении в 100 раз ацетатного буферного раствора рН:
а) уменьшается, б) увеличивается
в) не изменяется, г) сначала уменьшается, а затем увеличивается
5. Щелочной резерв крови – это количество мл СО2, находящегося в 100 мл сыворотки крови. В норме оно равно:
а) 24%, б) 55%, в) 35%, г) 76%.
Ответы к тестам для самоконтроля
| № теста | Номер вопроса | ||||
| б | б | а | г | а | |
| б | б | б | б | в | |
| б | б | а | в | г | |
| б | б | а | б | б | |
| б | б | г | в | б |
