Работа поперечных мостиков
Миозиновые нити имеют поперечные выступы, которые представляют собой субфрагменты миозина – тяжелый меромиозин, в котором различают шейку и головку. Эти ферменты обладают АТФ-азной активностью (способностью расщеплять АТФ), они отходят биполярно. Во время сокращения каждый поперечный мостик может связываться с актиновой нитью. В момент взаимодействия головки с актиновой нитью развивается усилие, которое сопровождается поворотом головки на 45º, т. е. она действует как рычаг, приводя в движение актиновую нить.
Биполярное расположение головок в обеих половинах саркомеров приводит к скольжению актиновых нитей в правой и левой половинах саркомера.
В момент соединения поперечного мостика с актиновой нитью происходит активация АТФ-азы этого мостика, затем расщепление АТФ. Предполагают, что энергия расщепления АТФ необходима для разделения актина и миозина.
Расщепление – обязательное условие, которое обеспечивает следующий цикл взаимодействия актина и поперечных мостиков.
Таким образом, происходит ритмическое отсоединение и присоединение головок миозина к актиновым нитям (сходство с группой людей, которая тянет длинную веревку).
Несмотря на ритмичную смену прикрепления и отсоединения поперечных мостиков с частотой от 5 до 50 Гц, сила, развиваемая мышцей, в физиологических условиях не колеблется, так как гребковые движения поперечных мостиков происходят асинхронно.
В случае уменьшения концентрации АТФ цикличность может нарушаться, а существенное снижение концентрации АТФ может привести к устойчивому прикреплению мостиков к актину.
Этим объясняется состояние трупного окоченения (расслабление будет возможно в результате аутолиза).
Электромеханическое сопряжение:
1. Генерация ПД. (Стимуляция приводит к деполяризации сарколеммы.)
2. Распространение ПД по Т-системе. (Деполяризация Т-системы и саркоплазматического ретикулума.)
3. Электрическая стимуляция зоны контакта Т-системы и саркоплазматического ретикулума, активация ферментов, образование инозитолтрифосфата, повышение внутриклеточной концентрации ионов кальция. (Выход ионов кальция из саркоплазматического ретикулума.)
Сокращение:
4. Образуется комплекс кальций + тропонин. Комплекс кальций + тропонин снимает блокаду актина тропомиозином (освобождение активных центров на актиновых филаментах), а также снимает блокаду тропонином I АТФ-азной активности миозина.
5. Взаимодействие миозиновой головки с актином, вращение головки и развитие эластической тяги.
6. Скольжение нитей актина и миозина относительно друг друга, уменьшение размера саркомера, развитие напряжения или укорочение мышечного волокна.
Расслабление:
7. Кальций отделяется от комплекса с тропонином.
8. Кальций диффундирует от тонких филаментов в саркоплазматический ретикулюм.
9. Тропомиозин возвращается на блокирующее место.
10. Тропонин I блокирует АТФ-азную активность миозина.
11. Поперечные актомиозиновые мостики разрываются и нити смещается друг относительно друга. В головках вновь накапливается АТФ.
Таким образом, в механизме сокращения скелетных мышц сократительными белками являются - актинимиозин,арегуляторными - тропонинитропомиозин.
Контрактура -в условиях целостного организма возникает при патологии и проявляется в длительном, слитном сокращении мышцы, которое не управляется корой (волей человека). Природа контрактур различна. В экспериментальных условиях ее легко получить путем воздействия на мышцы.
Гиперкалиевый раствор: вызывает длительную деполяризацию мембраны, что приводит к достаточно длительной активности мышцы (калиевая контрактура).
Кофеиновая контрактура: длительное сокращение, которое держится в течении всего времени, пока в растворе содержится кофеин. Является следствием высвобождения ионов кальция из саркоплазматического ретикулума.
СЕРДЕЧНАЯ МЫШЦА
Сердечная мышца (миокард) относится к возбудимым тканям и имеет поперечную исчерченность. Однако в области Z-линий имеются участки слияния (переплетения) волокон (в этих участках образуются вставочные диски). Благодаря этой особенности сердечная мышца представляет собой сеть волокон. Т-система кардиомиоцитов локализована в области Z-линий (а не на месте слияния А и I-дисков, как в скелетной).
В ответ на раздражение сердечная мышца сокращается в соответствии с законом «все или ничего», т.е. либо с максимальной силой, либо не сокращается вовсе. У скелетной мышцы закон «всё или ничего» выполняется применительно к отдельному мышечному волокну, а не к мышце в целом, т.к. отдельные волокна имеют разную возбудимость.
Свойства сердечной мышцы: 1) возбудимость; 2) проводимость; 3) сократимость; 4) автоматия.
Автоматия – это значит, что возбуждение возникает в сердце периодически, под влиянием процессов, протекающих в нём самом. Однако способностью к автоматии обладают лишь определённые участки миокарда, состоящие из атипичной мышечной ткани, бедной миофибриллами.
Все мышечные клетки сердца можно разделить на два больших класса:
1) миокардиоциты – осуществляют сокращение в ответ на приходящий ПД;
2) миоциты – входят в состав узлов автоматии и проводящей системы.
Для миоцитов способность к сокращению выражена слабо. Их главная функция состоит в генерации автоматического ПД и быстрого проведения возбуждения по сердцу.
Мембранный потенциал атипичных волокон не держится на стационарном уровне, происходит медленный сдвиг мембранного потенциала в сторону КУД – фаза спонтанной (или медленной) диастолической деполяризации(СДД или МДД). МДД – внутриклеточный механизм спонтанного возбуждения клеток, лежит в основе автоматии. При достижении КУД начинается генерация ПД, затем снова МДД провоцирует появление очередного потенциала действия и т.д..
Причины фазы МДД: 1) Снижение активности натрий-калиевой АТФ-азы; 2) Низкая проницаемость мембраны для ионов калия; 3) Высокая проницаемость мембраны для ионов натрия.
Проводящая система.
В норме возбуждение возникает в синоатриальном(синусно-предсердном) узле - в стенке правого предсердия у места впадения в него верхней полой вены. В атипичных клетках синоатриального узла наиболее высокая скорость МДД. Частота генерации ПД 60-80 в мин. Он навязывает ритм деятельности сердцу – является пейсмекером 1-го порядка.
От синоатриального узла возбуждение распространяется (скорость 0,8 – 0,9 м/с) по волокнам правого и левого предсердия, запуская процесс их сокращений. От предсердий возбуждение достигает перегородки между предсердиями и желудочками и попадает в атриовентрикулярный (предсердно-желудочковый) узел. В сердце теплокровных животных существуют специальные проводящие пути между синоатриальным и атриовентрикулярным узлами, а также между правым и левым предсердиями.
В атриовентрикулярном узле значительно замедляется скорость проведения возбуждения (0,02 – 0,05 м/с). Эта атриовентрикулярная задержка проведения необходима для того, чтобы отставить во времени процесс возбуждения в предсердиях и желудочках: камеры предсердий и желудочков работают поочередно.
От атриовентрикулярного узла возбуждение переходит на пучок Гиса.Благодаря атриовентрикулярной задержке возбуждение доходит до пучка Гиса тогда, когда предсердия успевают сократиться.
Пучок Гиса прободает предсердно-желудочковую перегородку и делится на правую и левую ножки. Ножки следуют в межжелудочковой перегородке, а в области верхушки сердца загибаются вверх и переходят в сеть сердечных проводящих миоцитов (волокон Пуркинье), погружённых в рабочий (сократительный) миокард желудочков. Скорость распространения возбуждения в пучке Гиса (4,5 – 5 м/с) и проводящих миоцитах в 5 раз больше скорости распространения по рабочему миокарду. Благодаря этому, миокардиоциты желудочков вовлекаются в сокращение почти одновременно.
Существует градиент автоматии, выражающийся в убывающей способности к автоматии (из-за понижения скорости МДД) различных участков проводящей системы, по мере удаления от синоатриального узла. При повреждении синоатриального узла роль водителя ритма – пейсмекера 2-го порядка берёт на себя атриовентрикулярный узел (частота разрядов 30 – 40 в мин.). Вентрикулярная проводящая система – пучок Гиса, волокна Пуркинье – пейсмекеры 3-го порядка (частота 15-20 в мин.).
Проводящая система обеспечивает: 1) ритмическую генерацию ПД; 2) координацию сокращений предсердий и желудочков; 3) синхронное вовлечение в процесс сокращения миокардиоцитов желудочков.
Отличительная особенность проведения возбуждения в миокарде – большое количество межклеточных контактов в виде специальных структурных образований – вставочных дисков. Вставочные диски имеют различную структуру. Одни участки вставочных дисков – это нексусы (электрические синапсы), другие выполняют механическую функцию, третьи – обеспечивают транспорт веществ через мембрану кардиомиоцита (креаторные связи). Нексусы благодаря низкому сопротивлению электрическому току обеспечивают быстрый переход возбуждения с одной клетки на другую. Благодаря нексусам мышечная ткань предсердий и желудочков ведёт себя как функциональный синцитий: возбуждение, возникнув в каком-либо из отделов, охватывает все без исключения невозбуждённые волокна.
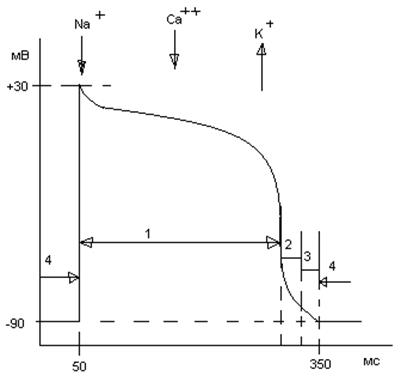
Рис. 15. ПД рабочего миокардиоцита желудочка.
1 – период абсолютной рефрактерности; 2 – период относительной рефрактерности;
3- период супернормальной возбудимости; 4 – период полного восстановления нормальной возбудимости.
Сокращение сердца, как и скелетных мышц, запускается ПД. Однако, временные соотношения этих процессов в этих двух типах мышц различны. Длительность ПД скелетных мышц составляет несколько мс, а сокращение начинается тогда, когда возбуждение уже почти заканчивается. В миокарде возбуждение и сокращение в значительной степени перекрываются во времени, ПД заканчивается после начала фазы расслабления.
В ПД рабочего (сократительного) миокардиоцита желудочка выделяют следующие фазы: фаза деполяризации (1-2 мс); фаза быстрой начальной реполяризации; фаза замедленной реполяризации (плато); фаза быстрой конечной реполяризации. МПП -90 мВ; амплитуда ПД 120 мВ; длительность ПД 100 – 400 мс (в среднем 300 мс). У ПД миокардиоцитов предсердий нет такой четко выраженной фазы плато, как у рабочих миокардиоцитов желудочков, и, соответственно, меньшая продолжительность ПД.
В отличие от ПД скелетных мышц, у миокардиоцитов во время реполяризации происходит открытие кальциевых каналов и возникает деполяризующий медленный входящий кальциевый ток. Одновременно уменьшается проводимость для калия. Эти причины формируют фазу плато, задерживают реполяризацию и удлиняют по времени ПД.
Рефрактерность во время ПД связана с инактивацией натриевых каналов. Их восстановление происходит при реполяризации до уровня - -40 мв. Т.е. рефрактерность связана с длительностью ПД. Если изменяется длительность ПД, то, соответственно, изменяется и длительность периода рефрактерности. При длительности ПД 300 мс, 270 из них приходятся на АРП.
Систола миокарда почти совпадает с рефрактерностью отдельного миокардиоцита. Этот рефрактерный период больше, чем время распространения возбуждения по предсердиям и желудочкам. Это делает невозможным возникновение тетануса в сердечной мышце.
Раздражение, нанесённое на миокард в период расслабления (диастолы), когда возбудимость восстановлена, вызывает внеочередное сокращение сердца – экстрасистолу.
ГЛАДКИЕ МЫШЦЫ
Свойства гладкой мышцы: 1) возбудимость; 2) проводимость; 3) сократимость; 4) пластичность (при растягивании напряжение мышцы сначала увеличивается, но затем уменьшается); 5) автоматия (способность к спонтанной деятельности).
Гладкие мышцы подразделяются на висцеральные(или унитарные)и мультиунитарные (ресничная мышца и мышца радужки глаза). Деление основано на различной плотности их двигательной иннервации. В висцеральных гладких мышцах (находятся во всех внутренних органах, протоках пищеварительных желез, кровеносных и лимфатических сосудах, и т.д.) двигательные нервные окончания имеются на небольшом количестве гладкомышечных клеток (ГМК). Однако возбуждение передаётся на все ГМК пучка благодаря нексусам между ними. Нексусы позволяют ПД и медленным волнам деполяризации распространяться с одной мышечной клетки на другую; обеспечивают одномоментность сокращения.
Висцеральная гладкая мышца имеет двойную иннервацию – симпатическую и парасимпатическую.
Нет концевых пластинок и отдельных нервных окончаний. По всей длине разветвлений АД- и Х-ергических нейронов имеются утолщения – варикозы. Они содержат гранулы с медиатором, который выделяется из каждой варикозы. По ходу следования нервного волокна могут возбуждаться или тормозиться многие ГМК. Скорость проведения возбуждения – несколько сантиметров в секунду.
Возбуждающее влияние проявляется в виде отдельных волн деполяризации. При повторной стимуляции потенциалы суммируются, и может возникнуть ПД.
Тормозящее влияние в виде отдельных волн гиперполяризации (ТПСП). При ритмической стимуляции ТПСП суммируются.
Строение гладких мыщц.
Состоят из клеток веретенообразной формы (длина 100 мкм, диаметр 3 мкм). Клетки располагаются в составе мышечных пучков и тесно прилегают друг к другу. Содержат миофиламенты актина и миозина, которые располагаются здесь менее упорядоченно, чем в скелетных волокнах. Саркоплазматическая сеть также менее развита.
Электрическая активность ГМК.
Нестабильный мембранный потенциал (МП). Колебания МП вызывают нерегулярные сокращения, которые поддерживают мышцу в состоянии частичного сокращения – тонуса. При уменьшении МП мышца сокращается, при увеличении – расслабляется. В период относительного покоя величина МП в среднем –50 мВ. Величина ПД может варьировать в широких пределах; продолжительность ПД 50-250 мс. В некоторых ГМК ПД имеют продолжительное плато во время реполяризации.
Ионная природа ПД ГМК определяется особенностями каналов мембраны. Основную роль играют ионы Са2+ . Кальциевые каналы пропускают и другие двухзарядные ионы (Ba2+ , Mg2+), а также ионы Na+ . Вход Са в клетку во время ПД необходим для поддержания тонуса и развития сокращения.
Автоматия.
ПД ГМК имеют авторитмический (пейсмекерный) характер. Пейсмекерные потенциалы регистрируются в различных участках ГМ. Т.е. любые клетки висцеральных ГМ способны к самопроизвольной автоматической активности. Автоматия ГМ присуща многим внутренним органам и сосудам.
Реакция на растяжение.
В ответ на растяжение ГМ сокращается. Растяжение уменьшает МП клеток, увеличивает частоту ПД и в конечном итоге – тонус ГМ. Это свойство служит одним из способов регуляции двигательной деятельности внутренних органов. Напр., увеличение тонуса стенки желудка в ответ на растяжение при наполнении способствует сохранению объема органа и лучшему контакту его стенок с поступившей пищей. В кровеносных сосудах растяжение, создаваемое колебаниями кровяного давления, является основным фактором миогенной регуляции тонуса сосудов.
Пластичность.
Если растянутую висцеральную ГМ удерживать в состоянии удлинения, то ее напряжение будет постепенно уменьшаться, иногда не только до уровня, существовавшего до растяжения, но и ниже. Эта пластичность ГМ способствует нормальному функционированию внутренних полых органов.
Связь возбуждения с сокращением.
Висцеральная ГМ находится в состоянии непрерывной активности. В условиях относительного покоя можно зарегистрировать одиночный ПД (электромеханические соотношения изучать труднее, чем в скелетной).
В основе сокращения также лежит скольжение актина по отношению к миозину, где ион Са2+ выполняет триггерную функцию.
Особенность заключается в обязательном фосфорилировании миозина перед АТФ-азной активностью. Механизм: ион Са2+ соединяется с кальмодулином (рецептивный белок для иона Са), возникающий комплекс активирует фермент – киназу легкой цепи миозина, который катализирует процесс фосфорилирования миозина. Затем происходит скольжение актина по отношению к миозину, составляющее основу сокращения. Т.е. пусковой момент для сокращения гладкой мышцы – присоединение иона Са2+ к кальмодулину, а для скелетной – к тропонину.
В гладких мышцах сократительные белки – актин, миозин; регуляторные: кальмодулин и тропомиозин.
ГЛАНДУЛОЦИТЫ
Железистая ткань также относится к возбудимым тканям. Однако, образующие ее гландулоциты обладают существенной морфофункциональной спецификой.
Секреция – процесс образования внутри клетки (гландулоцита) и выделения из нее специфического продукта (секрета).
Выделяемые секреторной клеткой вещества могут иметь различное отношение к внутриклеточным процессам. Собственно секретом принято считать продукт метаболизма данной клетки, экскретом – продукт ее катаболизма, рекретом – поглощенный клеткой из крови и затем в неизмененном виде выделенный продукт.
Секрет может выводиться из клетки через ее апикальную мембрану в просвет ацинусов, протоки желез, полость пищеварительного тракта – экзосекреция (внешняя секреция).
Выведение секрета из клетки через ее базолатеральную мембрану в интерстициальную жидкость, откуда он поступает в кровь и лимфу, называется внутренней секрецией – эндосекрецией, или инкрецией.
Секреторный цикл – периодическое изменение состояния секреторной клетки, обусловленное образованием, накоплением, выделением секрета и восстановлением ее дальнейшей секреции. Выделяют несколько фаз цикла: 1) поступление в клетку исходных веществ (диффузия, активный транспорт и эндоцитоз); 2) синтез и транспорт исходного секреторного продукта, формирование секреторных гранул; 3) выделение секрета из клетки.
Биопотенциалы гландулоцитов имеют ряд особенностей в покое и при секреции: низкую величину и скорость изменения, градуальность, различную поляризованность базальной и апикальной (верхушечной) мембран, гетерохронность изменения поляризованности мембраны при секреции.
МП гландулоцитов экзокринных желез в состоянии относительного покоя равен от –30 до –75 мВ. Стимуляция секреции меняет МП. Это изменение поляризованности мембраны называется секреторным потенциалом. У разных гландулоцитов он имеет существенные различия, влияет на секреторный цикл и сопряжение его фаз, на синхронизацию активности гландулоцитов в составе данной железы (это не исключает химического взаимодействия их через межклеточные контакты). Оптимальной для возникновения секреторных потенциалов считается поляризованность мембраны –50 мВ.
Для возбуждения большинства видов гландулоцитов характерна деполяризация их мембран (обусловлена потоком ионов натрия в клетку и выходом из нее ионов калия). У некоторых гландулоцитов мембраны при возбуждении гиперполяризуются (за счёт транспорта в клетку ионов хлора и выход из нее ионов натрия и калия).
Различие в поляризованности базальной и апикальной мембран составляет 2-3 мВ, что создает значительное электрическое поле (20-30 В/см). Его напряженность при возбуждении секреторной клетки возрастает примерно вдвое, что способствует перемещению секреторных гранул к апикальному полюсу клетки и выходу секреторного материала из клетки. Изменение МП и электрической проводимости гландулоцитов опосредовано увеличением внутриклеточной концентрации кальция (стимуляторы секреции, повышающие концентрацию кальция в гландулоцитах, влияют на калиевые и натриевые каналы и вызывают секреторный потенциал).
Секреция желез контролируется нервными, гуморальными и паракринными (выделение химических средств управления в межтканевую жидкость) механизмами.
Для синаптических окончаний на гландулоцитах характерны незамкнутые относительно широкие синаптические щели, заполненые интерстициальной жидкостью. Сюда из окончаний нейронов поступают медиаторы, из крови – гормрны, из соседних эндокринных клеток – парагормоны, от самих гландулоцитов – продукты их жизнедеятельности.
В состоянии покоя гландулоциты выделяют небольшое количество секрета, которое может градуально увеличиваться или уменьшаться. На мембранах гландулоцитов имеются возбуждающие и тормозные рецепторы, с участием которых секреторная активность гландулоцитов изменяется в широких пределах.
