Будут ли изотоническими 10%-ные растворы глюкозы и фруктозы? 9.В 5%-ном растворе глюкозы эритроциты будут:
1) да
2) нет
3) будут осмолярными
4) будут осмоляльными
9.В 5%-ном растворе глюкозы эритроциты будут:
1) находиться в равновесном состоянии
2) подвергаться гемолизу
3) подвергаться плазмолизу
4) подвергаться лизису
10.Осмотическое давление пропорционально:
1) молярной концентрации
2) молярной концентрации эквивалента
3) моляльной концентрации
4) мольной доле вещества
11.Давление паров растворителя над раствором при увеличении концентрации вещества:
1) уменьшается
2) увеличивается
3) не изменяется
4) сначала увеличивается, затем уменьшается
12.Температурой кипения жидкости является температура, при которой давление ее паров становится…
1) равным внешнему давлению
2) меньше внешнего давления
3) больше внешнего давления
4) зависит от формы сосуда
13.Криоскопические и эбуллиоскопические постоянные зависят от:
1) природы растворителя
2) температуры
3) природы растворенного вещества
4) числа частиц растворенного вещества
14.При добавлении этанола к воде температура кипения:
1) понижается
2) повысится
3) не изменится
4) зависит от формы сосуда
15.В 200 г. физиологического раствора ( 0,9% NaCl) содержится NaCl :
1) 18 г.
2) 1.8 г.
3) 0.18 г.
4. 0.018 г.
16.Гидратная теория электролитической диссоциации была предложена::
1) С.Аррениусом
2) Д.И.Менделеевым
3) О.Генри
4) Г.Льюис
17.Электролитическая диссоциация сопровождается:
1) увеличением энтропии и уменьшением энергии Гиббса
2) увеличением энтропии и увеличением энергии Гиббса
3) уменьшением энтропии и увеличением энергии Гиббса
4) энтропия и энергия Гиббса не изменяется
18.Только сильные электролиты перечислены в ряду:
1) H2S, HCl, H2SO4
2) HClO4,KCl, HNO3
3) HCN, CH3COOH, NH4OH,
4) NaOH, H2Se, HI
19.Электрический ток не проводят водные растворы:
1) ацетата Na
2) хлорид метиламмония
3) муравьиной кислоты
4) глицерина
20.Диссоциацию глюкозы описывает уравнение:
1) С6Н12О6 → 6С4++12Н+ + 6О2-
2) глюкоза не диссоциирует
3) С6Н12О6 → 12Н+ + 6СО-
4) С6Н12О6 → 6С4+ + 6Н2О
21.Количественной характеристикой процесса электролитической диссоциации электролита является:
1) степень диссоциации
2) константа растворимости
3) степень ионизации
4) константа нестойкости
22.Степень диссоциации слабого электролита увеличивается при:
1) добавлении одноименного иона
2) увеличении концентрации раствора
3) разведении раствора
4) охлаждении раствора
23.Взаимосвязь константы диссоциации и степени диссоциации слабого электролита описывается законом:
1) Гульдберга-Вааге
2) В.Оствальда
3) М.К.Сеченова
4) О.Генри
24.Константа диссоциации слабого электролита не зависит от:
1) природа электролита
2) полярности растворителя
3) температуры
4) концентрации вещества
25.Коэффициент активности иона тем больше, чем:
1) больше концентрация электролита
2) меньше концентрация электролита
3) меньше растворимость электролита
4) не зависит от концентрации электролита
26.Ионная сила раствора – это:
1) произведение концентрации иона на квадрат его заряда
2) произведение концентрации иона на его заряд
3) сумма произведения концентрации ионов на квадрат их зарядов
4) полусумма произведения концентрации ионов на квадрат их зарядов
27.Коэффициент активности ионов (fi) в очень разбавленных растворах равен:
1) 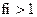
2) 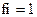
3) 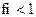
4) 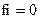
28.Ионная сила плазмы крови человека равна 0,15 м, заменителем плазмы крови является:
1) 0,7 м раствор глюкозы
2) 0,15 м раствор карбоната натрия
3) 0,9% раствор хлорида натрия
4) 1,9% раствор хлорида натрия
29.Смешали 200г 20%-ного и 300г 10%-ного растворов глюкозы. Массовая доля вещества в полученном растворе равна в %:
1)15
2)16
3)18
4)14
Сосудосуживающим действием обладает гидрохлорид адреналина. Его терапевтическая доза составляет 0,5 мл 0,1%-ного раствора. Рассчитайте массу (г) адреналина, содержащуюся в этом растворе (плотность раствора равна 1г/мл) .
1) 0,5
2) 0,0005
3) 0,005
4) 0,1
Вариант 5
Часть А
1.Рабочие «горячих» цехов должны пить подсоленную воды, так как в результате повышенного потоотделения осмотическое давление у них:
1) понижается
2) повышается
3) не меняется
4) сначала понижается, затем повышается
2.В 200 г воды растворили Х г вещества, молярная масса которого 92 г/моль. Температура замерзания понизилась на 0.279 °С. Ккр=1.86. Определить Х.
1) 2.76 г
2) 13,8 г
3) 8 г
4) 12,5 г
3.Опишите поведение эритроцитов в 5%-ном растворе NaCl. Каким будет
этот раствор по отношению к плазме крови?
1) гемолиз, гипотоническим
2) плазмолиз, гипотоническим
3) гемолиз, гипертоническим
4) плазмолиз, гипертоническим
4.Изотонический раствор - это:
1) 0,89%-ный раствор NaCl;
2) 8,9%-ный раствор NaCl;
3) 0,089%-ный раствор NaCl;
4) 1 ,00 %-ный раствор NaCl.
5.Раствор ,содержащий 11,6 г вещества в 400г воды,замерзает при температуре -0,93°С (КН2О=1,86град кг/моль).Молярная масса растворенного вещества равна ____г/моль
1)29
2) 58
3)116
4)87
6.Чем объясняется слабительный эффект сульфата магния;
1)осмосом воды в просвет кишечника;
2)диффузией соли в полости кишечника;
3)осмосом соли и воды из полости кишечника?
4)образованием осадков
7.Солевые слабительные средства (сульфаты натрия, магния, карловарская соль) в кишечнике осмотическое давление:
1) уменьшают
2) увеличивают
3) не изменяется
4) сначала уменьшают, затем увеличивают
8.При введении гипертонических растворов наблюдается:
1) осмотический шок
2) осмотический конфликт
3) флуороз
4) ацидоз
9.Температура кипения децимоляльного раствора KCL по сравнению с децимоляльным раствором сахарозы:
1) выше
2) ниже
3) их температуры одинаковы
4) зависит от давления
10.Будут ли изотоническими сантимолярные растворы глюкозы и NaCl?
1) да
2) нет
3) будут осмолярными
4) будут осмоляльными
11.В 2%-ном растворе глюкозы эритроциты будут:
1) находиться в равновесном состоянии
2) подвергаться гемолизу
3) подвергаться плазмолизу
4) подвергаться лизису
12.0,5-ный раствор NaCl является по отношению к плазме крови:
1) гипотоническим
2) гипертоническим
3) изотоническим
4) осмоляльным
13.Осмос – это направленный самопроизвольный переход молекул растворителя через мембрану из:
1) раствора с меньшей концентрацией в раствор с большой концентрацией
2) раствора с большей концентрацией в раствор с меньшей концентрацией
3) зависит от температуры
4) зависит от объема
14.В горах температура кипения воды:
1) ниже, чем на равнине
2) выше, чем на равнине
3) имеет такое же значение, как на равнине
4) зависит от формы сосуда
15.В закрытом сосуде находится 2 стакана: с чистой водой (1) и с водным раствором сахара (2) . Через некоторое время…
1) уровень жидкости в стакане (1) понизится, в стакане (2) повысится
2) уровень жидкости в стакане (1) повысится, в стакане (2) понизится
3) уровень жидкости в обоих стаканах не изменится
4) уровень жидкости в обоих стаканах понизится
16. Самопроизвольный распад вещества на ионы при растворении в воде называется:
1) ротация
2) гидратация
3) диссоциация
4) интерференция
17. Только слабые электролиты перечислены в ряду:
1) NH4OH, H2S, H2SO3
2) H2CO3, NaCl, CH3COOH
3) HClO, KOH, MgSO4
4) CaCl2, H2Te, HI
18. Электролитом не является:
1) расплав КОН
2) азотная кислота
3) раствор NaOH
4) этиловый спирт
19. Степень диссоциации в растворах слабых электролитов – это отношение:
1) количества молекул продиссоциированных к общему количеству молекул вещества
2) общего количества молекул вещества к количеству, продиссоциированных молекул
3) активной концентрации вещества к общей концентрации вещества в растворе
4) общей концентрации вещества в растворе к активной концентрации вещества
20. При увеличении концентрации электролита, степень диссоциации:
1) увеличивается
2) уменьшается
3) не зависит от концентрации
4) сначала увеличивается, затем уменьшается
21. Для сильных электролитов понятие «активность ионов» характеризует:
1) степень диссоциации
2) взаимодействие между ионами и растворителем
3) степень гидратации
4) эффективную концентрацию ионов
22. Константа диссоциации слабого электролита зависит от:
1) концентрации
2) разбавления
3) природы вещества и растворителя
4) давления
23. Способность электролита диссоциировать на ионы характеризуется:
1) степенью диссоциации
2) константой растворимости
3) константой Генри
4) константой нестойкости
24. Концентрация иона SO42- в 0,01 м растворе соли Al2(SO4)3:
1) 0,01 м
2) 0,02 м
3) 0,03 м
4) 0,05 м
25. С увеличением ионной силы раствора коэффициент активности иона в уравнении 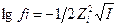 :
:
1) уменьшается
2) увеличивается
3) не изменяется
4) вначале увеличивается, затем остается постоянным
26. Ионная сила плазмы крови человека равна:
1) 0,25 м
2) 0,15 м
3) 0,9 м
4) 0,3 м
