Теоретическое введение. Хром – элемент VI В группы
Хром – элемент VI В группы. Строение его электронной оболочки 1s22s22p63s23p63d54s1. У атома хрома шесть валентных электронов: один на 4s- подуровне последнего уровня (4s1) и пять на 3d –подуровне предпоследнего энергетического уровня (3d5). В атоме 42Mo достраивается d-подуровень предпоследнего уровня. При этом у атома молибдена электронная конфигурация (n-1)d5s1, а у атома вольфрама 5d46s2. Максимальная степень окисления этих металлов +6.Для молибдена и вольфрама характерна в соединениях промежуточная степень окисления +4, для хрома +3. В химических соединениях хром проявляет различные степени окисления : +2, +3, +6; наиболее устойчивая степень окисления хрома +3. Хром – твердый блестящий металл, плавящийся при 18900С; плотность его 7,19 г/см3. При комнатной температуре хром устойчив по отношению к воде и воздуху. В ряду стандартных электродных потенциалов хром стоит между цинком и железом. Стандартный электродный потенциал хрома φ0= -0,71. В, поэтому хром растворяется в соляной и разбавленной серной кислотах с выделением водорода и образованием солей хрома Cr3+. Азотная кислота, концентрированная серная, царская водка пассивируют хром, увеличивая его потенциал до +1,2 В (по отношению к стандартному водному электроду). Пассивированный хром подобен благородным металлам. Атомные и ионные радиусы молибдена и вольфрама близки по значению, поэтому эти металлы сходны по физическим и химическим свойствам, но существенно отличаются от хрома. При переходе от хрома к вольфраму восстановительная активность металлов несколько понижается. Молибден и вольфрам отличаются слабо выраженными свойствами пассивироваться. Кислород взаимодействует с этим металлами при температуре выше 6000С. Молибден и вольфрам окисляется фтором при обычной температуре, а хром при нагревании; молибден и вольфрам растворяются только в азотной, концентрированной серной кислотах и “царской водке” при нагревании. Для молибдена и вольфрама устойчивы оксиды MoO2, WO2, MoO3 и WO3. Оксид MoO3 плохо растворим в воде; с водой он образует малорастворимую молибденовую кислоту. Оксид WO3 еще менее растворим в воде. Оба эти соединения, проявляя кислотные свойства, взаимодействуют со щелочами, образуя соли - молибдаты и вольфраматы.
Хром образует три оксида: CrO (основной), Cr2O3 (амфотерный) и CrO3 (кислотный). Соответственно этим трем оксидам известны и гидроксиды хрома. Основной гидроксид Cr(OH)2 , как и все соединения хрома со степенью окисления +2, неустойчив, в реакциях является сильным восстановителем, легко окисляется кислородом воздуха с образованием Cr(OH)3.
4Cr(OH)2↓ + O2 + 2H2O = 4Cr(OH)3
Гидроксид Cr(OH)3 имеет амфотерный характер и растворяется в кислотах с образованием солей хрома (III), а в щелочах – с образованием растворов гидроксохромитов:
Cr(OH)3↓+ 3NaOH = Na3[Cr(OH)6]
Cr(OH)3↓+ 3OH– = [Cr(OH)6]3–
или
Cr(OH)3↓ + OH–= [Cr(OH)4]–
Соли хрома (III) в водных растворах сильно гидролизованы создают кислую реакцию среды и легко превращаются в основные соли:
CrCl3 + H2O ↔ CrOHCl2 + HCl
или
Cr3+ + H2O ↔ CrOH2++ H+
Гидролиз сульфида и карбоната хрома протекает необратимо с образованием гидроксида хрома и сероводородной или угольной кислот. Хром в щелочной среде является хорошим восстановителем, в присутствии окислителей соли Cr(III) они легко переходят в хроматы:
2K3[Cr(OH)6] + 3Br2 + 4KOH= 2K2CrO4 + 6KBr + 8H2O
или
[Cr(OH)6]3-+ 2OH--3ē = CrO 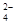 + 4Н2О
+ 4Н2О
Кислотному оксиду хрома CrO3 соответствуют две кислоты: хромовая H2CrO4и двухромовая H2Cr2O7. Обе кислоты существуют только в растворе, но соли их устойчивы. Соли хромовой кислоты называются хроматами, а двухромовой – дихроматами. Хромат-ион СrO 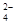 желтого цвета, а дихромат-ион Cr2O72- оранжевого цвета. Хроматы могут обратимо переходить в дихроматы:
желтого цвета, а дихромат-ион Cr2O72- оранжевого цвета. Хроматы могут обратимо переходить в дихроматы:
Н+
2CrO42-+H+ 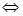 Cr2O72- + OH-
Cr2O72- + OH-
OH-
т.е хроматы устойчивы в щелочной среде, а дихроматы – в кислой.
Хроматы и дихроматы – сильные окислители. Окислительные свойства соединений хрома (VI) наиболее сильно выражены в кислой среде:
Cr2O72- + 14H+ +6ē = 2O23+ + 7H2O φ0 = + 1,33 В.
Например:
K2Cr2O7+3H2S+4H2SO4= Cr2(SO4)3+3S↓+K2SO4+7H2O
Соединения хрома со степенью окисления +3, +6 ядовиты. Они вызывают раздражения кожи и слизистой оболочки.
Выполнение опытов
Цель работы:
Ознакомление с химическими свойствами соединений хрома.
