Тема 2. Поверхностные явления и адсорбция
Любая поверхность раздела обладает свободной поверхностной энергией, так как энергетическое состояние молекул пограничного слоя отличается от энергетического состояния молекул в объёме фазы. Молекулярные силы притяжения поверхностных молекул полностью не компенсируются, что и определяет свободную энергию поверхности, равную F = s · S, где S — поверхность раздела; s — поверхностное натяжение. При S = 1 F = s. Таким образом, поверхностное натяжение — это удельная свободная поверхностная энергия, приходящаяся на единицу межфазной поверхности.
Поверхностное натяжение характеризует различия в интенсивности межмолекулярных взаимодействий граничащих фаз. Чем больше эти различия, тем больше s. Для границы «конденсированная фаза (твердая или жидкая) — воздух» можно пренебречь межмолекулярными взаимодействиями в воздухе, тогда поверхностное натяжение характеризует интенсивность межмолекулярных сил в конденсированной фазе.
Поверхностное натяжение растворов может быть больше или меньше, чем у чистого растворителя, т. к. различные растворенные вещества по-разному влияют на поверхностное натяжение растворов.
Вещества, понижающие поверхностное натяжение называются поверхостно-активными (ПАВ). Они имеют дифильное строение, т. е. полярную часть (функциональные группы) и неполярную часть (углеводородный радикал). Молекулу ПАВ принято изображать так:

Поверхостно-активными по отношению к воде являются вещества менее полярные, чем вода, такие как спирты, жирные кислоты, амины и др. Они взаимодействуют с водой слабее, чем молекулы воды между собой, поэтому, попадая на поверхность, они уменьшают поверхностное натяжение.
Вещества, повышающие поверхостное натяжение называются повеpхостно-инактивными. К ним относятся сильные элекролиты: соли, кислоты, щелочи. Зависимость поверхностного натяжения от концентрации растворенного ПАВ выражается уравнением Шишковского:
s = s0 – В ln(1 + K×c),
где s0 − поверхостное натяжение воды; с − концентрация раствора; В−костанта гомологического ряда; К−удельная капиллярная постоянная, которая увеличивается в 3-3,5 раза при удлинении углеводородного радикала на одно звено (группу −СН 2−).
Поверхостное натяжение индивидуальных веществ на границе с газом понижается с повышением температуры, так как при этом ослабляется интенсивность межмолекулярного взаимодействия в конденсированной фазе.
Адсорбцией называется самопроизвольное изменение концентрации компонента в поверхностном слое по сравнению с его концентрацией в объеме фазы.
Более плотную фазу (определяющую форму поверхности) принято называть адсорбентом, вещество молекулы которого могут адсорбироваться — адсорбтивом, уже адсорбированное вещество — адсорбатом. Процесс, обратный адсорбции, называется десорбцией.
В зависимости от природы адсорбционных сил, адсорбция может быть физической и химической.
Физическая адсорбция обусловлена силами межмолекулярного взаимодействия. Особенностью физической адсорбции является обратимость, т. е. имеет место динамическое равновесие: адсорбция ↔ десорбция.
Химическая адсорбция (хемосорбция) возникает в результате химической реакции между адсорбтивом и адсорбентом с образованием нового поверхностного соединения. Поэтому химическая адсорбция необратима. Другой особенностью хемосорбции является ее специфичность. Адсорбция происходит, только если возможна химическая реакция.
Адсорбция на границе жидкий раствор — газзаключается в том, что растворенное в жидкости вещество концентрируется на поверхности раствора на границе с газом. Процесс адсорбции обусловлен снижением поверхностного натяжения, и чем в большей степени ПАВ снижает поверхностное натяжение, тем большей будет его адсорбция.
Уравнение Гиббса связывает величину адсорбции со способностью растворенного вещества изменять поверхностное натяжение раствора:
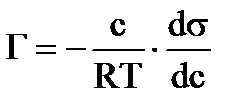 ,
,
где Г− адсорбция вещества, с − молярная концентрация его в растворе, Т – температура, R – универсальная газовая постоянная, 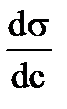 − изменение поверхностного натяжения раствора с изменением концентрации.
− изменение поверхностного натяжения раствора с изменением концентрации.
Анализ уравнения Гиббса позволяет заключить следующее:
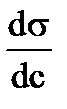 < 0, то Г > 0, т. е. наблюдается положительная адсорбция − вещество концентрируется на поверхности раствора; если
< 0, то Г > 0, т. е. наблюдается положительная адсорбция − вещество концентрируется на поверхности раствора; если 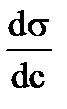 > 0, то Г < 0, т.е. адсорбция отрицательна − вещество уходит с поверхности в объем раствора.
> 0, то Г < 0, т.е. адсорбция отрицательна − вещество уходит с поверхности в объем раствора.
Выражение (– 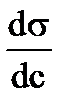 ) называют поверхностной активностью и обозначают G. Поверхностная активность возрастает с уменьшением полярности вещества. По правилу Дюкло и Траубе: поверхностная активность предельных жирных кислот в водных растворах возрастает в 3-3,5 раза на одно звено (группу —СН 2—). Правило соблюдается и для других гомологических рядов — спиртов, аминов и т.д.
) называют поверхностной активностью и обозначают G. Поверхностная активность возрастает с уменьшением полярности вещества. По правилу Дюкло и Траубе: поверхностная активность предельных жирных кислот в водных растворах возрастает в 3-3,5 раза на одно звено (группу —СН 2—). Правило соблюдается и для других гомологических рядов — спиртов, аминов и т.д.
В соответствии с теорией мономолекулярной адсорбции Лэнгмюра:
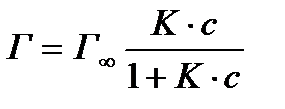 ,
,
где Г∞ − максимальная (предельная адсорбция); Г− адсорбция при концентрации c;
К − константа адсорбционного равновесия
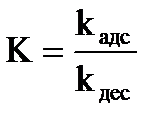 ,
,
где kадс, kдес − константы скорости адсорбции и десорбции соответственно.
Для нахождения постоянных (Г∞ и К) в уравнении Лэнгмюра, его приводят к линейной форме: 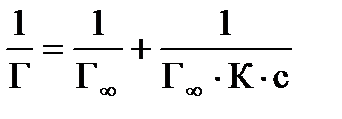
и, построив график 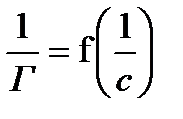 , находят предельную адсорбцию Г∞ и константу адсорбционного равновесия К.
, находят предельную адсорбцию Г∞ и константу адсорбционного равновесия К.
Рассматривая раздел «адсорбция газов и паров на поверхности твердых тел», обратите внимание на особенности этого вида адсорбции.
Для аналитического описания адсорбции используется уравнение Фрейндлиха:
а = в × р1/n ,
где а − адсорбция, р − давление газа, в и n − константы, зависящие от природы газа и температуры, которые находят из экспериментальных данных.
С повышением температуры физическая адсорбция уменьшается, так как возрастает интенсивность теплового движения молекул газа.
Необходимо рассмотреть основные допущения теории мономолекулярной адсорбции, на основании которых Лэнгмюр вывел выражение, называемое уравнением изотермы мономолекулярной адсорбции Лэнгмюра:
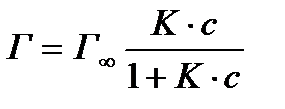 ,
,
где Г∞− емкость адсорбционного слоя или предельная адсорбция; К − константа адсорбционного равновесия; р − парциальное давление газа.
По значению Г ∞ может быть определена важная характеристика твердого адсорбента − удельная активная поверхность Sуд. Если известна S0 − площадь, занимаемая одной молекулой адсорбтива в насыщенном монослое, то
Sуд = Г ∞× S0 × NA ,
где NA ― постоянная Авогадро.
Уравнение Лэнгмюра можно использовать только при условии, что адсорбция вещества сопровождается образованием мономолекулярного слоя.
Поляни предложил теорию полимолекулярной адсорбции, которая объясняла тот факт, что после образования мономолекулярного слоя связывание адсорбтива с адсорбентом не прекращается.
Брунауэр, Эммет и Теллер разработали теорию применительно к адсорбции паров (теория БЭТ). Теория полимолекулярной адсорбции БЭТ исходит из наличия на поверхности адсорбента активных центров. В этом состоит ее сходство с теорией Лэнгмюра. Вместе с тем, подобно теории Поляни, она допускает возможность образования нескольких адсорбционных слоев.
Адсорбция на границе раздела «твёрдое тело – жидкость»— это самопроизвольное концентрирование растворенного вещества вблизи поверхности твердого адсорбента.
Различают молекулярную и ионную адсорбцию из растворов.
Молекулярная адсорбция — адсорбция из растворов неэлектролитов или слабых электролитов. Растворенные вещества адсорбируются на поверхности в виде молекул. Зависимость молекулярной адсорбции от равновесной концентрации адсорбтива описывается как уравнением Лэнгмюра, так и уравнением теории БЭТ, а в области средних концентраций — уравнением Фрейндлиха. Применимо также уравнение Гиббса.
Особенность молекулярной адсорбции состоит в том, что наряду с растворенным веществом адсорбируются молекулы растворителя. Поэтому, чем хуже адсорбируется растворитель, тем лучше будет адсорбироваться растворенное вещество. А растворитель адсорбируется тем хуже, чем больше его поверхностное натяжение. Отсюда вытекают две закономерности:
- адсорбция на твердом адсорбенте идет лучше из водных растворов и хуже из органических растворов;
- правило Шилова: чем лучше растворитель растворяет вещество, тем хуже вещество адсорбируется из раствора.
Влияние на молекулярную адсорбцию природы адсорбента проявляется в его свойствах: полярности и пористости. Неполярные твердые тела лучше адсорбируют неполярные адсорбтивы, и наоборот.
Влияние пористости зависит от соотношения размеров пор адсорбента и молекул растворенного вещества. Крупные молекулы не могут попасть в узкие поры адсорбента, и адсорбция уменьшается.
Повышение температуры приводит к уменьшению адсорбции, но в меньшей степени чем при адсорбции газов.
Ионная адсорбция — адсорбция из растворов сильных элекролитов. В этом случае вещество адсорбируется в виде ионов. Ионная адсорбция происходит только на полярных адсорбентах и при этом сопровождается образованием двойного электрического слоя. На адсорбцию ионов влияет величина радиуса иона. Чем больше радиус иона при одинаковом заряде, тем лучше он адсорбируется, так как с увеличением радиуса иона возрастает его поляризуемость, а следовательно, способность притягиваться к полярной поверхности. С другой стороны, при этом уменьшается гидратация иона, а это облегчает адсорбцию. В соответствии с указанным, ионы располагают в ряды по возрастающей способности к адсорбции, называемые лиотропными рядами или рядами Гофмейстера:
Li+<Na+<K+<Rb+<Gs+<Mg2+<Ca2+<Sr2+<Ba2+<Cl–<Br–<NO3–<I–<CNS–
адсорбционная способность возрастает
Чем больше заряд иона, тем сильнее ион притягивается противоположно заряженной поверхностью, тем сильнее адсорбция:
К+ < Cа2+ < Аl3+ < Th4+
усиление адсорбции
Для адсорбции ионов поверхностью кристалла Панет и Фаянс сформулировали правило: на кристаллической поверхности адсорбируются ионы, способные достраивать кристаллическую решетку и образующие труднорастворимое соединение с ионами, входящими в кристалл. Так, кристалл хлорида серебра nAgCl из раствора, содержащего ионы K+, Cl-, NO3 – будет адсорбировать ионы Cl-.
Для ионной адсорбции характерно явление обменной адсорбции.
Ионообменная адсорбция − это процесс, при котором твердый адсорбент обменивает свои ионы на ионы того же знака из жидкого раствора. Вещества, проявляющие способность к ионному обмену называются ионитами. Иониты, способные обменивать катионы, называют катионитами, они содержат ионообменные группы: −SO3H; −COOH; −OH (фенольные). Иониты, способные обмениваться анионами, называют анионитами, они содержат активные группы: −NH2, =NH, −N(CH3)3Cl и др.
Смачивание— это поверхностное явление, заключающееся во взаимодействии жидкости с твердыми или другими жидкими телами при наличии одновременного контакта с воздухом.
Различают три случая смачивания: полное смачивание, когда капля жидкости самопроизвольно растекается на поверхности, пока не покроет ее мономолекулярным слоем; полное несмачивание — капля жидкости на твердой поверхности самопроизвольно принимает почти сферическую форму; неполное смачивание — различные промежуточные случаи между двумя крайними. Мерой смачивания является краевой угол q, иногда его называют углом смачивания.
Краевой угол (θ) − это угол, который образует капля с поверхностью твердого тела со стороны жидкости.
Если вода на твердой поверхности образует θ < 900, то такую поверхность называют гидрофильной, если θ > 900, то поверхность называют гидрофобной. Чем больше краевой угол, тем в меньшей степени жидкость смачивает поверхность твердого тела. Степень смачивания, а значит, и краевой угол зависит от соотношения величин поверхностного натяжения на границах: воздух − твердое тело sтв-г, жидкость − твердое тело sтв-ж и воздух − жидкость sж-г. Эта зависимость выражается уравнением Юнга:
sтв-г = sтв-ж + sж-г × cos q ,
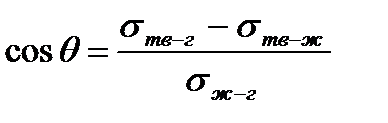 . Отсюда следует, что
. Отсюда следует, что
если s тв-г > s тв-ж, то cosθ > 0 и θ < 900 - смачивание полное или частичное,
если s тв-г < s тв-ж, то cosθ < и θ > 900 - несмачивание.
К явлению адсорбции и смачивания близки явления адгезии.
Адгезия (прилипание) − это взаимодействие между приведенными в контакт поверхностями конденсированных фаз разной природы. Адгезия обусловлена стремлением системы к уменьшению поверхностной энергии, следовательно, является самопроизвольным процессом.
Работа адгезии Wa − это работа обратимого разрыва адгезионной связи, отнесенная к единице площади.
Работа адгезии при разрыве двух контактирующих жидкостей (1 и 2) находящихся в среде (3) определяются уравнением Дюпре:
Wa = s1,3 + s2,3 - s1,2 .
Из уравнения следует, что работа адгезии Wa тем больше, чем больше поверхностное натяжение исходных компонентов и чем меньше конечное межфазное поверхностное натяжение.
Работа адгезии между жидкостью и твердым телом определяется по уравнению Юнга:
Wa = s2,3 × (1+cos θ),
где s2,3 − повехостное натяжение на границе «жидкость − воздух».
Работу адгезии между твердыми телами вычислить невозможно с помощью рассмотренных уравнений, так как поверхностное натяжение на границе «твердое тело – воздух» обычно неизвестно. Определяют ее экспериментально при непосредственном разрушении соединения.
Когезией называется притяжение молекул, атомов или ионов внутри отдельной фазы. Когезию оценивают работой когезии Wк. Это работа процесса разрыва тела по сечению равному единице. При этом образуются две новые единицы поверхности данной фазы.
Соотношение работы когезии и адгезии определяется смачиванием:
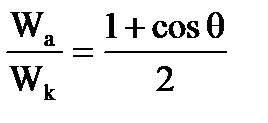 .
.
При Wa = Wк растекание становится неограниченным, т. к. θ = 0; при Wa = 0 полное несмачивание, так как θ = 1800.
Чтобы увеличить смачивание надо повысить адгезию или уменьшить когезию. Например, добавлением ПАВ.
