Экспериментальная часть. Опыт 1. Влияние концентрации реагирующих веществ на химическое равновесие
Опыт 1. Влияние концентрации реагирующих веществ на химическое равновесие
Запишите уравнение реакции:
__________________
Запишите выражение константы химического равновесия для данной реакции:
Кх.р.=
_____________________________
Заполните таблицу:
| № пробирки | Что добавлено | Изменение интенсивности окраски | Направление смещения равновесия |
Вывод:___________________________.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ФГБОУ ВПО «Уфимский государственный нефтяной технический университет»
Кафедра «Прикладная химия и физика»
Дисциплина «Химия»
ОТЧЕТ
по лабораторной работе №___
На тему: «Электролитическая диссоциация»
Выполнил
студент группы__________ ______________И.О. Фамилия
(Подпись, дата)
Принял
преподаватель кафедры ПХиФ __________________И.О. Фамилия
(Подпись, дата)
Цель работы:
-изучить электрическую проводимость растворов электролитов и зависимость её от различных факторов;
- научиться предсказывать направление обменной реакции в растворах электролитов.
Теоретическая часть
Электролиты-__
____________________.
Процесс распада молекул вещества на ионы под действием растворителя называется___________.
Основания – это электролиты, которые при диссоциации образуют только один вид анионов – ___
NaOH ______
NH4OH _____.
Кислоты – это электролиты, которые при диссоциации образуют только один вид катионов – ___________
HCl _______
HNO3 ______
H2SO4 _____
H3PO4 _____.
Амфотерные гидроксиды диссоциируют в водном растворе как по типу кислоты, так и по типу основания. При их диссоциации одновременно образуются ионы:_____________________ ____________________.
К ним относятся гидроксиды цинка Zn(OH)2, алюминия Al(OH)3, хрома (III) Cr(OH)3, свинца (II) Pb(OH)2 и др..
Например, при диссоциации Zn(OH)2 в водном растворе одновременно присутствуют:
___________⇄ H2ZnO2 º Zn(OH)2 ⇄ _____________.
Средние соли – это электролиты, при диссоциации которых в водных растворах образуются ионы ________________
Na2SO4 _____________________________
Ca3(PO)4 ___________________________.
Кислые соли при растворении в воде образуют ионы_
KHSO3 _____________________________,сложный анион диссоциирует частично:
HSO3- ________________________
Основные соли при диссоциации образуют анионы_______________________и сложные катионы, состоящие и_________:
Al(OH)2Cl ___________________________,Сложный катион диссоциирует частично:
Al(OH)2+ _____________________________
AlOH2+ _______________________________.
Двойные соли диссоциируют на два катиона__________________________и анион ________________________________:
KAl(SO4)2 _____________________________
Na2NH4PO4 ___________________________.
Сложные соли диссоциируют на катион ________________и анионы_________________
ZnClNO3 = ______________________________
AlSO4Cl = _______________________________.
Степень диссоциации (a) показывает_______________
____________________.
Степень диссоциации зависит от различных факторов:_______________________________
_____________________
____________________.
Для сильных электролитов a > 30%, для средних электролитов a_______, для слабых электролитов a_________.
Константа диссоциации для равновесия, которое устанавливается в растворе слабого электролита:
AmBn ⇄ m An+ + n Bm-
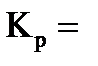
___________.
Равновесия в слабых электролитах подчиняются закону _____________________________.
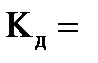
___________.
Между ионами электролитов в растворе действуют силы_____________________________. В связи с этим состояние ионов описывают активностью - условной (эффективной) концентрацией ионов:
а = ______________________________.
Экспериментальная часть
Опыт 1. Изучение электрической проводимости растворов
А. Запишите наблюдения, отмечая степень накала лампы:____________________________
____________________.
Напишите уравнение диссоциации воды:
H2O _______________.
Б. Запишите наблюдения, отмечая степень накала лампы:
1.___________________
2.___________________
3. __________________
4.___________________
5. ___________________
6. __________________.
Напишите уравнения диссоциации электролитов:
1. CH3COOH _________
2. NH4OH ____________
3. HNO3 _____________
4. HCl _______________
5. NaOH _____________
6. KOH ____________.
Вывод: (по степени накала лампы определить сильным или слабым электролитом являются вышеприведённые вещества)________________________________
___________________.
В. Напишите уравнения реакций в молекулярной и ионной формах:
1. HCl + NaOH _______
__________
2. CH3COOH + NH4OH _______________________________.
_________.
Смешайте равные объёмы растворов и запишите наблюдения:
1.___________________
2.___________________,
Вывод: (какова электрическая проводимость полученных растворов)_________________________
____________________
___________________
________.
Опыт 2. Зависимость электрической проводимости раствора (степени диссоциации электролита) от разбавления
При добавлении дистиллированной воды к концентрированной кислоте степень накала лампы ______________.
При добавлении дистиллированной воды к концентрированному раствору аммиака степень накала лампы ________.
Вывод:(как изменяется электрическая проводимость растворов от разбавления)____________________
___________________.
