Виды коррозии металлов
| Вид коррозии | Описание коррозийного процесса |
| Химическая (разрушение металла при взаимодействии его с сухими газами или жидкостями, не проводящими электрического тока) | Процесс идет с разрушающим металлы веществом (кислород воздуха, водой, H2S, SO2, и др.) Пример: Fe+H2S=FeS+H2 Fe+SO2+H2O=FeSO3+H2 |
| Электрохимическая(разрушение металла в среде электролита) | Электрохимическая коррозия железа, где железо находится в контакте с медью. В природной воде присутствуют ионы H+, OH-, HCO3-, Cl- и др. Электролиты от более активного металла железа, переходят в менее активный - медь, то есть медь становится катодом, а железо- анодом У поверхности железа (анод) образуется катионы низкой степени окисления (+1): Fe2++OH-=(FeOH)+ затем (FeOH)++Fe(OH)2+HCO3=(FeOH)2CO3+H2 Под действием Н2О и О2 идет реакция 4Fe(OH)2+O2+2H2O= 4Fe(OH)3 Если к катоду подходит кислород, то образуется вода 4H0+O2=2H2O Таким образом железо, как более активный металл разрушается, так как образуется слой рыхлой ржавчины, не защищающий железо от дальнейшей коррозии |
Типы защиты металлов от коррозии.
| Метод | Схема реализации | Область применения |
| Катодная защита | На некотором расстоянии от трубопровода в землю зарывается идущий параллельно ему металлический анод, который образует с трубопроводом гальваническую пару. | Защита подземных трубопроводов и металлических емкостей. |
| Металлургический | Введение в состав стали в процессе ее плавки легирующих элементов: Cr, N, Mn, Si, W, V | В машиностроении для создания коррозийно - стойких сталей и сплавов |
| Нанесение металлических, оксидных и органических покрытий | Анодное покрытие (цинкование). Катодное покрытие (лужение - покрытие оловом), хромирование и др. Оксидирование (погружение железа в щелочь с окислителем) Анодирование в гальванических ваннах. Покраска и лакировка. | В общем, энергитическом и химическом машино-строении, а так же в автомобилестроении, авиа - и кораблестроении. |
Примеры решения задач.
Пример.1. Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах. Составьте электронные уравнения анодного и катодного порцессов. Каков состав продуктов коррозии?
Решение. Цинк имеет более отрицательный потенциал (—0,763 В), чем кадмий (—0.403 В), поэтому он является анодом, а кадмий катодом.
анодный процесс: 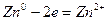
катодный процесс: в кислой среде 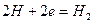
в нейтральной среде: 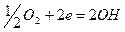

Так как ионы 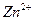 с гидроксильной группой образует нерастворимый гидроксид, то продуктом коррозии будет
с гидроксильной группой образует нерастворимый гидроксид, то продуктом коррозии будет 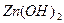 .
.
