Выполнение определений
Взятие и растворение навески. На аналитических весах взвешивают часовое стекло и записывают его вес в журнал. На тех же весах точно отвешивают около 0,3 г хлористого бария, количественно переносят в химический стакан с носиком емкостью 200–300 мл и растворяют в воде. Переносить навеску с часового стекла в стакан рекомендуется так. Сначала очень осторожно пересыпать навеску в стакан. Затем, держа стекло наклонно над стаканом, тщательно обмыть его струей дистиллированной воды из промывалки; при этом, конечно, вся жидкость с него должна стекать в стакан. После прибавления 3 – 5 мл 2н раствора соляной кислоты (для предупреждения образования коллоидного раствора BaSO4) дистиллированной водой доводят общий объем жидкости в стакане приблизительно до 100 мл.
Осаждение. Стакан закрывают часовым стеклом; полученный раствор нагревают почти до кипения. Одновременно в другой чистый химический стакан (можно в колбочку) отмеривают 3 – 4 мл 2Н Н2SO4, разбавляют ее дистиллированной водой до 30 мл, нагревают до кипения и приливают к горячему раствору хлористого бария. Серную кислоту нужно приливать очень медленно, по каплям, все время перемешивая раствор стеклянной палочкой. Во время перемешивания надо стараться не касаться палочкой стенок и дна стакана, чтобы осадок не пристал к стеклу.
Когда вся серная кислота будет прилита, стакан с полученным осадком (палочка остается в стакане) тотчас же помещают на 2-3 ч на кипящую водяную баню, чтобы сернокислый барий осел на дно стакана.
Как только осадок полностью соберется на дне стакана, берут пробу на полноту осаждения. Для этого к прозрачному раствору осторожно по стеклянной палочке приливают 1-2 капли серной кислоты. Если раствор останется прозрачным, то осаждение полное. Если же будет новое помутнение, то барий осажден не полностью и нужно снова прилить к раствору 2-3 мл серной кислоты. Дав раствору отстояться, еще раз взять пробу на полноту осаждения.
Убедившись в полноте осаждения, вынимают из раствора палочку и над стаканом тщательно смывают струей горячей воды из промывалки приставшие к палочке частицы осадка. Затем стакан с осадком накрывают часовым стеклом или фильтровальной бумагой и оставляют стоять на 3-4 ч или до следующего занятия. Медленное охлаждение способствует образованию крупнокристаллического осадка, который затем хорошо отфильтровывается.
Фильтрование и промывание осадка. Осадок BaSO4 отфильтровывают через плотный беззольный фильтр («синяя лента»). Такой фильтр вкладывают в воронку, которую помещают в кольцо штатива и подставляют под нее чистый стакан. Жидкость осторожно декантируют по стеклянной палочке на фильтр (нужно сливать жидкость с осадка так, чтобы не замутнить ее). Когда будет слита почти вся жидкость, промывают осадок 3-4 раза декантацией, прибавляя каждый раз 20-25 мл горячей, сильно разбавленной серной кислоты (примерно 0,1 %) и каждый раз как можно полнее сливая ее с осадка на фильтр. Когда декантация будет закончена, соблюдая все правила предосторожности, количественно переносят осадок на фильтр и промывают его холодной дистиллированной водой до тех пор, пока в промывной воде при помощи AgNO3 нельзя будет обнаружить присутствие ионов хлора.
Высушивание и прокаливание осадка. По окончании промывания воронку вместе с осадком сернокислого бария накрывают листочком фильтровальной бумаги и ставят в сушильный шкаф. После высушивания фильтр вместе с осадком аккуратно переносят в предварительно промытый, прокаленный и взвешенный фарфоровый тигель и приступают к прокаливанию осадка. При этой операции следят за тем, чтобы фильтр постепенно обугливался, но не вспыхивал.
Прокаливание продолжают до полного озоления фильтра, т.е. до тех пор, пока содержимое тигля не побелеет и не исчезнет черный налет как на стенках тигля, так и в само осадке. Затем переносят тигель в эксикатор, охлаждают до комнатной температуры и взвешивают. Чтобы быть уверенным в постоянстве веса осадка, прокаливают тигель еще раз 10-15 мин, охлаждают его в эксикаторе и снова взвешивают. Обычно двух прокаливаний бывает достаточно, чтобы получить постоянный вес осадка.
Вычисления (пример). Вычисления проводят следующим образом (вес в г):
Вес стекла с BaCl2∙2H2O………………………………….6,5801
Вес пустого стекла………………………………………..6,2345
навеска BaCl2∙2H2O…………… …………………...0,3456
вес тигля с BaSO4………………… …..………………12,3518
вес пустого тигля…………………………………...… .12,0230
навеска BaSO4……………………………………………..0,3288
Составляем и решаем пропорцию:
в 233,42 г BaSO4 содержится 137,36 г Ва
в 0,3288 г BaSO4 – // – Х г Ва
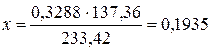 Ва
Ва
Если в навеске 0,3456 г найдено 0,1935 г бария, то содержание в процентах будет:
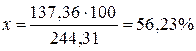
Таким образом, экспериментально найденная величина отличается от теоретически вычисленной на 0,24 %.
V. Литература.
1. Ю. Я. Харитонов. Аналитическая химия ч. II. Высшая школа, М., ч 2, с. 98-135.
2. В.П. Васильев. Аналитическая химия. Книга 1. Титриметрические и гравиметрический методы анализа. Высшее образование. М., 2004 г. С. 125-157.
3. Ю. Я. Золотов. Основы аналитической химии. Практическое руководство. Высшая школа, М., 2001. С. 233 - 234.
4. Лекции.
З А Н Я Т И Е № 16
I.Тема: Титрование в неводных средах.
II. Цель: Научиться использовать неводные растворители в кислотно-основных титриметрических методах анализа.
