Тема 12: Кислородсодержащие органические соединения
Производные углеводороды, в которых один или несколько атомов водорода замещены на гидроксогруппу, называются спиртами.
В зависимости от числа гидроксогрупп спирты делятся на: а) одноатомные, содержащие одну гидроксогруппу; б) многоатомные, содержащие две, три и более гидроксогрупп.
По правилам современной заместительной номенклатуры названия спиртов производят от названий углеводородов с добавлением окончания -ол и цифры, обозначающей номер углеродного атома, при котором стоит гидроксогруппа, определяющая начало нумерации.
Ниже приведена схема, отражающая химические свойства предельных одноатомных спиртов:
 Горение
Горение
 O2 nCO2 + (n + 1)H2O
O2 nCO2 + (n + 1)H2O
 Окисление O
Окисление O
 + [O] R — C
+ [O] R — C 
H
+ Na
 CnH2n+1ONa + H2↑
CnH2n+1ONa + H2↑
CnH2n+1OH  + HГ
+ HГ
 (H2SO4) CnH2n+1Г + H2O
(H2SO4) CnH2n+1Г + H2O
 + RCOOH
+ RCOOH  O
O
 t0, (H2SO4) R — C + H2O
t0, (H2SO4) R — C + H2O
OCnH2n+1
Дегидратация (H2SO4 (конц.))
 - H2O CnH2n + H2O
- H2O CnH2n + H2O
Отнятие от двух молекул
спирта одной молекулы воды
 - H2O (CnH2n+1)2O
- H2O (CnH2n+1)2O
 Альдегидами и кетонами называют производные углеводородов, содержащие функциональную карбонильную группу C = O (карбонил). В альдегидах карбонильная группа связана с атомом водорода и одним радикалом, а в ке
Альдегидами и кетонами называют производные углеводородов, содержащие функциональную карбонильную группу C = O (карбонил). В альдегидах карбонильная группа связана с атомом водорода и одним радикалом, а в ке  тонах — с двумя радикалами. Общие формулы:
тонах — с двумя радикалами. Общие формулы:
 O R — C —R'
O R — C —R'
 R — C ||
R — C ||
H O
альдегид кетон
Изомерия у альдегидов и кетонов обусловлена строением углеводородных радикалов, а у кетонов еще и положением кетонной группы, которая может занимать различные места внутри углеродной цепи.
Альдегиды и кетоны изомерны. Общая формула насыщенных альдегидов и кетонов CnH2nO.
По международной номенклатуре названия альдегидов производят от названий соответствующих углеводородных радикалов, включающих карбонильную группу с прибавлением окончания -аль, а у кетонов — окончания -он.
Альдегиды и кетоны, за счет имеющейся в их составе сильно поляризованной карбонильной группы, очень активны в химических реакциях. При этом альдегиды гораздо больше реакционноспособны, чем кетоны. Для них характерны реакции окисления, присоединения.
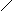 окисление [ O ] O
окисление [ O ] O


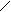
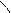 H — C
H — C
OH
H2 R — CH2 — OH

 O HCN R — CH — CN
O HCN R — CH — CN

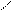
 R — C присоединение |
R — C присоединение |

 H OH OH
H OH OH
R1— OH |
 R — CH — O —R1
R — CH — O —R1
OH
NaHSO3 |
 выделение альдегидов в виде осадка R — CH — SO3Na
выделение альдегидов в виде осадка R — CH — SO3Na
 Cl
Cl
 PCl5 R — CH
PCl5 R — CH

 Cl
Cl
замещение NH3 R — CH = NH

NH2 — OH R — CH = N — OH

 Карбоновыми кислотами называются органические вещества, содержащие одну или O O
Карбоновыми кислотами называются органические вещества, содержащие одну или O O
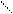
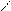
 несколько карбоксильных групп — C . Общая формула R — C , сокращенно RCOOH.
несколько карбоксильных групп — C . Общая формула R — C , сокращенно RCOOH.
OH OH
В зависимости от числа карбоксильных групп в молекуле различают кислоты одноосновные, двухосновные и т.д.
По международной номенклатуре названия присваивается кислоте по названию углеводорода с тем же числом атомов углерода, что и в кислоте, углерод в карбоксильной группе обозначается номером 1. Например, по международной номенклатуре предельная одноосновная кислота
6 5 4 3 2 1
CH3 — CH — CH — CH2 — CH2 — COOH
| | |
CH3 CH3 C2H5
будет называться 4,5-диметил-3-этилгексановая кислота.
Для карбоновых кислот характерна высокая реакционная способность.
 Na, Na2O O
Na, Na2O O

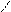
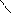 NaOH R — CH2 — C
NaOH R — CH2 — C
ONa
соли кислот
дегидратация (R — CH2 — CO)2O
 ангидриды кислот
ангидриды кислот
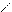
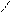
 O PCl5, SOCl2 O
O PCl5, SOCl2 O
 R — CH2 — C
R — CH2 — C 
 R — CH2 — C
R — CH2 — C
OH Cl
хлорангидриды кислот
O
R, - OH ||
 этерификация R — CH2 — C — O — R
этерификация R — CH2 — C — O — R
сложные эфиры
 NH3 O
NH3 O

 R — CH2 — C
R — CH2 — C
NH2
амиды кислот
Для карбоновых кислот, альдегидов и кетонов характерны следующие реакции за счет углеводородного радикала:
1. Замещение водорода на галоген (наиболее легко при углероде, находящемся в α — положении к карбоксильной или карбонильной группе):
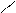 O O
O O
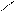
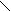
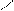
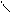 R — CH2 — C + Cl2 ® R — CHCl — C + HCl
R — CH2 — C + Cl2 ® R — CHCl — C + HCl
OH α OH
2. Присоединение соединений типа HХ к непредельным соединениям происходит с нарушением правила Морковникова:
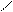
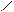 O O
O O
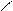
 CH2 = CH — C + HCl ® CH2 — CH2 — C
CH2 = CH — C + HCl ® CH2 — CH2 — C 
OH | OH
Cl
Сложными эфирами называют производные карбоновых кислот, у которых гидроксил в карбоксиле замещен спиртовым остатком:
 O O
O O
 R — C ® R — C
R — C ® R — C
OH OR'
кислота сложный эфир
Сложные эфиры в большинстве случаев называют по тем кислотам и спиртам, которые участвуют в их образовании, причем на первом месте в названии стоит кислота, на втором — спирт.
Например:
O O O
|| || ||
H — C — O — CH3 H3C — C — O — CH3 H3C — C — O — C2H5
муравьино-метиловый уксусно-метиловый уксусно-этиловый
эфир (метилформиат) эфир (метилацетат) эфир (этилацетат)
Употребляют также названия, образуемые от углеводородного радикала спирта и корня латинского названия кислоты с добавлением окончания -ат (в примерах, приведенных выше, эти названия даны в скобках).
Контрольные задания:
221. Напишите уравнение реакций внутримолекулярной и межмолекулярной дегидратации
2-метил-1-пропанола. Введите указанный спирт в реакции с: а) Naмет.; б) HСl; в) PСl5.
222. С какими из перечисленных веществ будет реагировать 1-пропанол:
а) Na б) CH3OH в) PCl5 г) NaOH д) CH3 — C = O
|
OH
Напишите уравнения соответствующих реакций, дайте систематические названия полученным соединениям. Что образуется при окислении 1-пропанола?
223. Составьте уравнения реакций получения соответствующих спиртов по нижеприведенной схеме:
O
||
H — C — H ? H2O ?
 | |||
 | |||
CH3 — CO — CH2 — CH3 ? H2O ?


 CH3 — CH2MgBr O
CH3 — CH2MgBr O
||
CH3 — CH2 — C — H ? H2O ?
 |  |
Для получения вторичного спирта приведите уравнения внутримолекулярной дегидратации, каталитического окисления и реакции этерификации с уксусной кислотой.
224.Приведите реакции, позволяющие отличить спирт от фенола.
225. Как из 1-пропанола получить 2-пропанол, применяя лишь неорганические реактивы?
226. Установите строение вещества C2H6O, если оно не реагирует с металлическим натрием на холоде, а при нагревании с ним дает CH3ONa и CH3Na. При нагревании с HI образуется CH3I и CH3OH.
227. Напишите схемы получения альдегида, метилэтилкетона тремя способами. Введите эти соединения в реакции с: а) PCl5; б) NaHSO3; в) HCN.
228. Напишите схемы получения ацетона из следующих исходных веществ: а) этиловый спирт; б) пропилен; в) ацетилен. Как ацетон будет взаимодействовать с: а) HCN; б) NaHSO3 ; в) PСl5.
229.С помощью каких реакций можно отличить ацетон от пропионового альдегида. Напишите реакции взаимодействия указанных веществ с: а) C2H5OH; б) HCN; в) NaHSO4; г) PСl5.
230. Напишите уравнения реакций, с помощью которых можно отличить альдегиды от кетонов. Какие соединения образуются при взаимодействии уксусного альдегида с хлористым фосфором, синильной кислотой?
231. Составьте схемы взаимодействия пропионового альдегида с веществами: а) синильной кислотой; б) этил магний бромидом; в) хлором; г) гидросульфатом натрия.
232.Какие ацетиленовые углеводороды следует взять, чтобы по реакции Кучерова получить:
а) метилэтилкетон; б) уксусный альдегид. Последний введите в реакции с: а) аммиаком;
б) гидросульфитом натрия; в) синильной кислотой.
233.Осуществите схему превращений:
HCl KCN 2H2O(H+)
CH3 — CH = CH2 ® A ® B ® C
Полученное соединение введите в реакции с NH3; PCl5; Na; Ca(OH)2; CH3OH.
234. Составьте уравнение реакций получения метилпропановой кислоты, исходя из пропилового спирта и используя все необходимые для этого неорганические вещества.
235. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения: O O
|| ||
C2H6 ® С2H5Cl ® С2H5OH ® CH3 — C — OH ® CH3 — C — O — C2H5 ® C2H5OH ® CO2
236Используя в качестве исходного соединения карбид кальция, получите уксусную кислоту, а из последней: а) хлористый ацетил; б) ангидрид уксусной кислоты; в) ацетат натрия. Как их этих веществ получить метилэтанат?
237.Напишите уравнения реакций получения масляной кислоты из: а) бромбутана; б) бромпропана. Полученную кислоту введите в реакции: а) с аммиаком при нагревании; б) с хлоридом фосфора (V); в) с этиловым спиртом.
238. Напишите уравнения получения этилацетата из ацетилена, используя его в качестве единственного органического вещества. Этилацетат введите в реакцию гидролиза.
239. Из каких кислот и спиртов могут быть получены следующие сложные эфиры:
а) HCOOC2H5; б) CH3(CH2)3COOCH3; в) C6H5COOCH(CH3)2.
Напишите уравнения реакций. В чем различие между сложными и простыми эфирами?
240. Из соответствующего альдегида получите 3-метилбутановую кислоту и напишите реакции взаимодействия этой кислоты со следующими соединениями:
а) PСl3; б) CH3 — CH — CH3; в) NaOH; г) CuO; д) Cl2.
|
ОН
