Задание 8-1 контрольной работы
Рассчитайте концентрации ионов Н+ и ОН– и рН раствора сильной кислоты или сильного основания, V мл которого содержит m г кислоты или основания ( 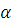 = 1).
= 1).
| Номер задания | Соеди-нение | V, мл | m, г | Номер задания | Соеди-нение | V, мл | m, г |
| HCl | 1,46 | HI | 0,0256 | ||||
| HCl | 0,365 | HBr | 1,62 | ||||
| HCl | 0,73 | HBr | 0,81 | ||||
| HCl | 0,365 | HBr | 0,81 | ||||
| NaOH | 0,04 | HBr | 0,162 | ||||
| NaOH | 0,02 | NaOH | 0,2 | ||||
| NaOH | 0,1 | NaOH | 0,4 | ||||
| NaOH | 0,40 | NaOH | 0,8 | ||||
| KOH | 0,56 | NaOH | 6,0 | ||||
| KOH | 0,112 | KOH | 8,4 | ||||
| KOH | 0,112 | KOH | 2,8 | ||||
| KOH | 1,12 | KOH | 1,68 | ||||
| HI | 2,56 | KOH | 0,28 | ||||
| HI | 0,256 | HCl | 1,46 | ||||
| HI | 1,28 | HCl | 0,73 |
Пример 3 Сравните концентрацию ионов Н+ в растворах уксусной кислоты Кдис =1,74·10–5 и соляной кислоты (α=0,8), концентрация которых См=1моль/л.
Решение
В растворе уксусной кислоты, равновесие процесса диссоциации сдвинуто в сторону недиссоциированных молекул:

 СН3СООН H+ + Н3СОО– , СH+ = √(1,7*10-5*1) =4,17*103моль/л.
СН3СООН H+ + Н3СОО– , СH+ = √(1,7*10-5*1) =4,17*103моль/л.
В растворе соляной кислоты равновесие диссоциации сдвинуто в сторону продуктов диссоциации, на ионы диссоциировано 80% молекул (α=0,8):

 HCl H+ + Cl– , СH+= α·Ск-ты = 0,8·1= 0,8 моль/л.
HCl H+ + Cl– , СH+= α·Ск-ты = 0,8·1= 0,8 моль/л.
0,8/4,17  10-3= 800/4,17=192, т.е. концентрация ионов в растворе соляной кислоты почти в 200 раз выше, чем в растворе уксусной кислоты.
10-3= 800/4,17=192, т.е. концентрация ионов в растворе соляной кислоты почти в 200 раз выше, чем в растворе уксусной кислоты.
Задание 8-2 контрольной работы
Напишите уравнение электролитической диссоциации раствора слабой кислоты и найдите концентрации ионов Н+ и кислотного остатка в моль/л в растворе нормальной концентрации с, если известна Кдисс.
| Вариант | Формула кислоты | Название кислоты | с,моль/л | Кдисс |
| HCOOH | Муравьиная | 0,005 | 1,8  10-4 10-4 | |
| CH3COOH | Уксусная | 0,005 | 1,74  10-5 10-5 | |
| HNO2 | Азотистая | 0,05 | 5,1  10-4 10-4 | |
| C6H6COOH | Бензойная | 0,05 | 6,6  10-5 10-5 | |
| HIO4 | Иодная | 0,005 | 2,8  10-2 10-2 | |
| HIO3 | Иодноватая | 0,001 | 1,6  10-1 10-1 | |
| HF | Плавиковая | 0,01 | 6,8  10-4 10-4 | |
| HCN | Синильная | 0,1 | 6,2  10-10 10-10 | |
| HBrO | Бромноватистая | 0,1 | 2,5  10-9 10-9 | |
| C2H5COOH | Пропионовая | 0,01 | 1,35  10-5 10-5 | |
| HCNS | Роданисто-водородная | 0,001 | 1,4  10-1 10-1 | |
| C6H4(OH)COOH | Салициловая | 0,001 | 1,1  10-3 10-3 | |
| HClO2 | Хлористая | 0,001 | 1,1  10-2 10-2 | |
| HClO | Хлорноватистая | 0,05 | 5,0  10-8 10-8 | |
| HCNO | Циановая | 0,01 | 3,5  10-4 10-4 | |
| HCOOH | Муравьиная | 0,02 | 1,8  10-4 10-4 | |
| CH3COOH | Уксусная | 0,01 | 1,74  10-5 10-5 | |
| HNO2 | Азотистая | 0,01 | 5,1  10-4 10-4 | |
| C6H5COOH | Бензойная | 0,01 | 6,6  10-5 10-5 | |
| HIO4 | Йодная | 1,0 | 2,8  10-2 10-2 | |
| HIO3 | Йодноватая | 2,0 | 1,6  10-1 10-1 | |
| HF | Плавиковая | 0,05 | 6,8  10-4 10-4 | |
| HCN | Синильная | 0,5 | 6,2  10-10 10-10 | |
| HBrO | Бромноватистая | 0,5 | 2,5  10-9 10-9 | |
| C2H5COOH | Пропионовая | 0,05 | 1,35  10-5 10-5 | |
| HCNS | Роданистово-дородная | 2,0 | 1,4  10-1 10-1 | |
| C6H4(OH)COOH | Салициловая | 1,0 | 1,1  10-3 10-3 | |
| HClO2 | Хлористая | 1,0 | 1,1  10-2 10-2 | |
| HClO | Хлорноватистая | 0,1 | 5,0  10-5 10-5 | |
| HCNO | Циановая | 0,05 | 3,5  10-4 10-4 |
Тема 9 Гидролиз солей
Гидролиз солей – это взаимодействие соли с водой, приводящее к образованию слабого электролита и сопровождающееся изменением кислотности среды (рН раствора). Гидролиз тем сильнее, чем меньше Кдисс образующего слабого электолита.
Возможны три типа гидролиза:
1. Гидролиз по аниону – гидролизу подвергается анион слабой кислоты,
Соль сильного основания и слабой кислоты NaF.
Молекулярное уравнение:
NaF + H2O = NaOH+ HF
Ионно-молекулярное уравнение:
F–+Na++НОН=⇄ Na++ОН–+НF
Кратное ионное уравнение:
F–+НОН= НF+ ОН–
Образующиеся при диссоциации анионы F– связываются молекулами воды в слабый электролит НF.
Ионы ОН– накапливаются, создавая в растворе щелочную среду (рН>7).
Гидролиз солей многоосновных кислот (например H2S) протекает по стадиям, преимущественно по 1 стадии с образованием кислой соли.
1 стадия: K2S + H2O = KHS + KOH
2К++S2– + HOH = К+ + HS– + К++ OH–
S2– + HOH =HS– + OH–
По 2 стадии гидролиз соли сильного основания и слабой кислоты протекает незначительно.
2 стадия: KHS + H2O = H2S + KOH
K++HS– + HOH = H2S + К++ OH–
HS-– + HOH = H2S + OH–
2.Гидролиз по катиону – гидролизу подвергается катион слабого основания.
Соль слабого основания и сильной кислоты NН4Сl.
Молекулярное уравнение:
NН4Сl + H2O = NН4OH + HСl
Ионно-молекулярное уравнение:
NН4++ Сl– + НОН = NН4+ + OH–
Кратное ионное уравнение:
NН4+ + НОН= NН4ОН+ Н+
Образующиеся при диссоциации катионы NН4+ связываются водой в слабый электролит NН4ОН.
Ионы Н+ накапливаются, создавая в растворе кислую среду (рН<7).
Гидролиз солей многокислотных оснований протекает по стадиям, преимущественно по 1 стадии с образованием основной соли.
1 стадия:
2CuSO4 + 2HOН = (CuOH)2SO4- + H2SO4
2Cu2+ + 2SO42–+ 2H2O = 2CuOH+ + SO42–+ +2H++ SO42–+
2Cu2++H2O = CuOH+ H+
2 стадия:
(CuOH)2SO4 + 2H2O = 2Cu(OH)2 + H2SO4
2(CuOH) + +SO42– + 2HOH = 2Cu(OH)2 + 2H+ + SO42–
CuOH+ + HOH = Cu(OH)2 + H+
3.Гидролиз по катиону и аниону – гидролизу подвергается катион слабого основания и анион слабой кислоты.
Соль слабого основания и слабой кислоты CH3COONH4.
NH4+ + CH3COO– + HOH = NH4OH + CH3COOH
Среда раствора близка к нейтральной (рН≈7) и в зависит от Кдисс образующихся слабых электролитов:
если Кдисс кислоты > Кдисс основания – среда слабокислая,
если Кдисс кислоты>Кдисс основания – среда слабощелочная
Соли сильных оснований и сильных кислот гидролизу не подвергаются, т.к. ни один из ионов соли не образует с ионами Н+ и ОН– воды слабых электролитов. Водные растворы таких солей имеют нейтральную среду.
Усиление гидролиза, совместный гиролиз солей слабого основания CrCl3 и слабой кислоты Na2S приводит к необратимому гидролизу каждой из солей до конца с образованием слабого основания и слабой кислоты.
Гидролиз соли CrCl3 идет по катиону: Cr3+ + HOH ⇄ CrOH2+ + H+
Гидролиз соли Na2S идет по аниону: S2– + HOH ⇄ HS– + OH–
Гидролиз усиливается, т.к. образуется слабый электролит Н2О (например, вода): H++OH–=Н2О
Молекулярное уравнение: 2CrCl3+3Na2S+6H2O=2Cr(OH)3+3H2S+6NaCl
Ионно-молекулярное уравнение: 2Cr3+ + 3S2– + 6H2O = 2Cr(OH)3¯ + 3H2S
