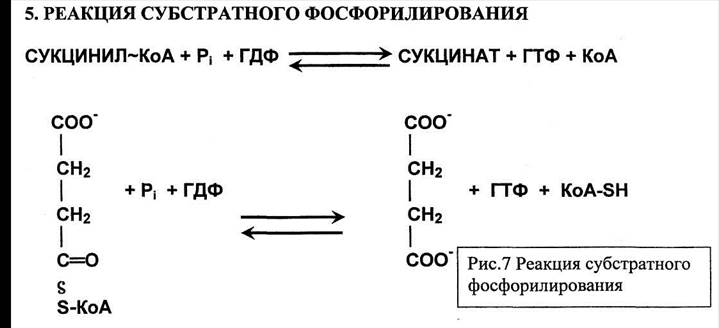
Реакции цикла трикарбоновых кислот
Цикл трикарбоновых кислот
В 1953 г. Кребсу была присуждена Нобелевская премия по физиологии и медицине «за открытие цикла лимонной кислоты» (1937г.). В поздравительной речи было сказано: «Цикл Кребса объясняет два одновременно происходящих процесса: реакции распада, при которых высвобождается энергия, и синтетические процессы, при которых эта энергия расходуется». Ученый, завершая речь «экскурсом в общую биологию», проанализировал более широкое значение этих открытий: «Наличие одного и того же механизма образования энергии у всех живых существ позволяет сделать еще два вывода, – сказал он. – Во-первых, этот механизм возник на очень ранних этапах эволюции, и, во-вторых, жизнь в ее настоящем виде зародилась лишь однажды».

Образующийся в ПВК-дегидрогеназной реакции ацетил-SКоА далее вступает в цикл трикарбоновых кислот (ЦТК, цикл лимонной кислоты, цикл Кребса). Кроме пирувата, в цикл вовлекаются кетокислоты, поступающие из катаболизма аминокислотили каких-либо иных веществ.
Цикл протекает в матриксе митохондрий и представляет собой восемь последовательных реакций: связывание ацетила и оксалоацетата (щавелевоуксусной кислоты) с образованием лимонной кислоты, изомеризация лимонной кислоты и последующие реакции окисления с сопутствующим выделением СО2. После восьми реакций цикла вновь образуется оксалоацета.
Основная роль ЦТК:
- генерации атомов водорода для работы дыхательной цепи, а именно трехмолекул НАДНи одноймолекулы ФАДН2.
Кроме этого, в ЦТК образуется
- одна молекула АТФ,
- сукцинил-SКоА, участвующий в синтезе гема,
- кетокислоты, являющиеся аналогами аминокислот – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой.
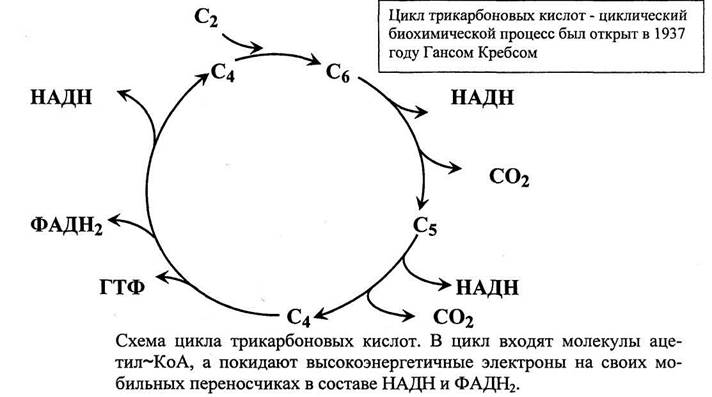
Цикл лимонной кислоты — заключительный этап катаболизма, локализованный в матриксе митохондрий. В нем 4-х углеродное соединение оксалоацетат конденсируется с 2-х углероднымацетильным компонентом, которое вносит в процесс молекула ацетил-КоА, с образованием 6-ти углеродной трикарбоновой кислоты - цитрата. Далее изомер цитрата подвергается окислительному декарбоксилированию. Образующееся при этом 5-ти углеродное соединение а-оксоглутарат (а-кетоглутарат) при окислительном декарбоксилировании превращается в 4-х углеродное соединение сукцинат. Дальнейшие превращения сукцината приводят к регенерированию 4-х углеродного оксалоацетата.
Поэтому одна молекула оксалоацетата может многократно использоваться для окисления ацетильных остатков.
2 атома углерода включаются в цикл в виде ацетильного компонента и 2 атома углерода покидают цикл в виде 2 молекул СО2.
Таким образом, двухуглеродный фрагмент молекулы ацетил-КоА подвергается полному окислению. Электроны, ранее принадлежащие молекуле ацетил~КоА, покидают цикл в связанной форме: в виде 3 молекул НАДН и
1 ФАДН2. Затем они переносятся в процесс окислительного фосфорилирования, где энергия каждой пары электронов переносимых НАДН, преобразуется в энергию макроэргических связей до 3 молекул АТФ. А энергия пары электронов переносимых ФАДН2, ведет к образованию до 2 молекул АТФ. Всего в процессе окислительного фосфорилирования при окислении этих переносчиков электронов образуется до 11 молекул АТФ.
1 макроэргическая связь генерируется в самом цикле в форме молекулы ГТФ или АТФ.
Итого, теоретически до 12 молекул АТФ может быть генеририровано при окислении 2-х углеродного фрагмента ацетил-КоА в цикле трикарбоновых кислот сопряженном с процессом окислительного фосфорилирования.
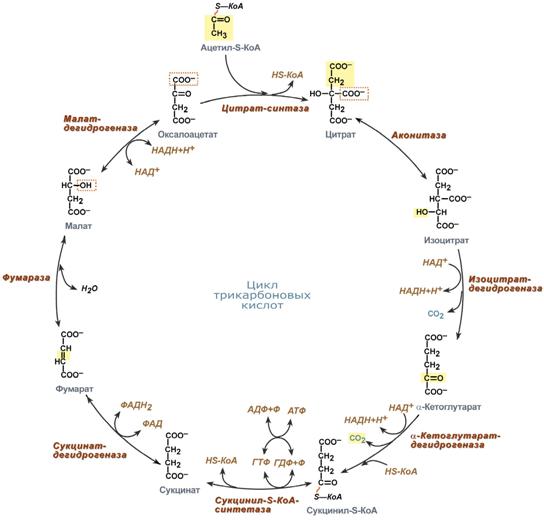
Реакции цикла трикарбоновых кислот
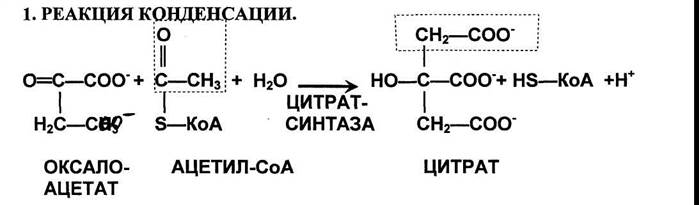 |
Реакция образования цитрата (лимонной кислоты): альдольная конденсация с последующим гидролизом, катализирует цитрат-синтаза. При расщеплении тиоэфирной связи освобождается коэнзим А, и выделяется значительная тепловая энергия. Равновесие в реакции сильно сдвинуто вправо.
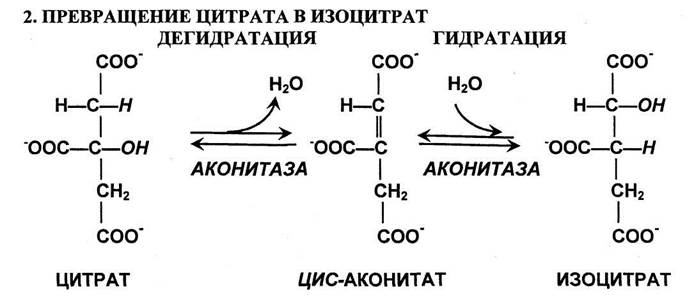
Превращение цитрата в изоцитрат. Изомеризация цитрата осуществляется
путем дегидратации с последующей гидратацией. В результате происходит
взаимоперемещение Н и ОН. Фермент назван аконитазой, поскольку промежуточное соединение цис-аконитат не покидает активный центр фермента.
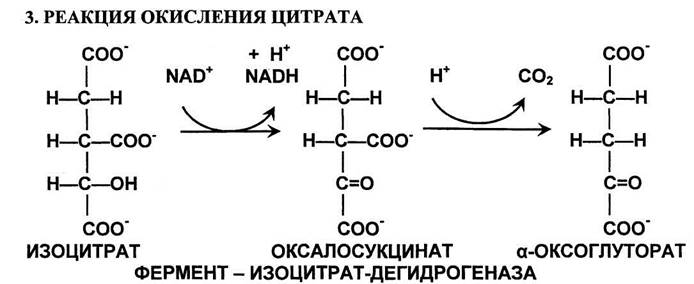 |
Реакция окислительного декарбоксилирования изоцитрата катализируется изоцитрат-дегидрогеназой и ведет к образованию а-оксоглутарата (а-кетоглутарата). НАД+ в реакции играет роль второго субстрата, захватывая пару высокоэнергетичных электронов, и в форме НАДН вовлекает их в процесс окислительного фосфорилирования. Самая медленная реакция цикла. Аллостерически активируется АДФ.
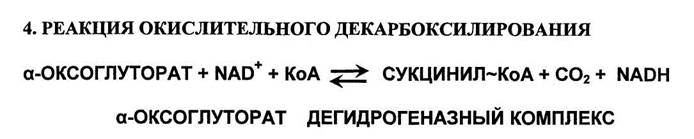
Реакция катализируется а-оксоглутарат дегидрогеназным комплексом (мультиферментный комплекс), который структурно и функционально сходен с пируват дегидрогеназным комплексом. Механизм этой реакции сходен с механизмом превращения пирувата в ацетил-КоА. В состав комплекса также входят 5 коферментов: тиаминдифосфат (ТДФ), липоевая кислота, ФАД, НАД+ и КоА. а-Оксоглутарат дегидрогеназный комплекс отличается от пируват дегидрогеназного комплекса тем, что в нем отсутствует сложная система регуляции активности. Равновесие реакции сильно сдвинуто вправо, в сторону образования сукцинил~КоА. Биохимическое значение реакции состоит в удалении карбоксильной группы (—СОО-) поскольку атом углерода в ней почти полностью окислен, и извлечь из неё электроны высокой энергии невозможно. Из неё можно извлечь всего 2е".