РН некоторых растворов
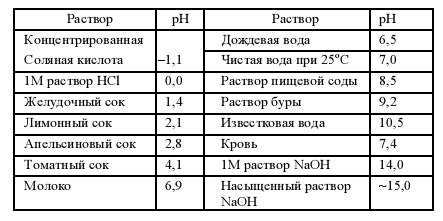
Таблица 2.
Интервали перехода окраски индикаторов
| Название индикатора | pK | Область перемены окраски,pH | Окраска | |
| Индикатор-кислота | Индикатор-основание | |||
| 1. Метиловый-оранжевый | 3,7 | 3,0-4,4 | красный | жёлтая |
| 2. Бром-феноловый синий | 4,1 | 3,0-4,6 | жёлтая | сине-фиолетовая |
| 3. Конго красный | 4,2 | 3,0-5,2 | сине-фиолетовая | красный |
| 4. Метиловый красный | 5,1 | 4,4-6,2 | красный | жёлтая |
| 5. n-Нитрофенол | 7,0 | 4,7-7,9 | бесцветная | жёлтая |
| 6. Лакмус | 7,0 | 5,0-8,0 | красный | синяя |
| 7. Бромтимоловый синий | 7,1 | 6,0-7,6 | жёлтая | синяя |
| 8. Тимоловый синий | 8,9 | 8,0-9,6 | жёлтая | синяя |
| 9. Фенолфталеин | 9,7 | 8,2-10,0 | бесцветная | малиновая |
| 10.Нейтральный красный | 7,3 | 6,8-8,0 | красный | янтарно-жёлтая |
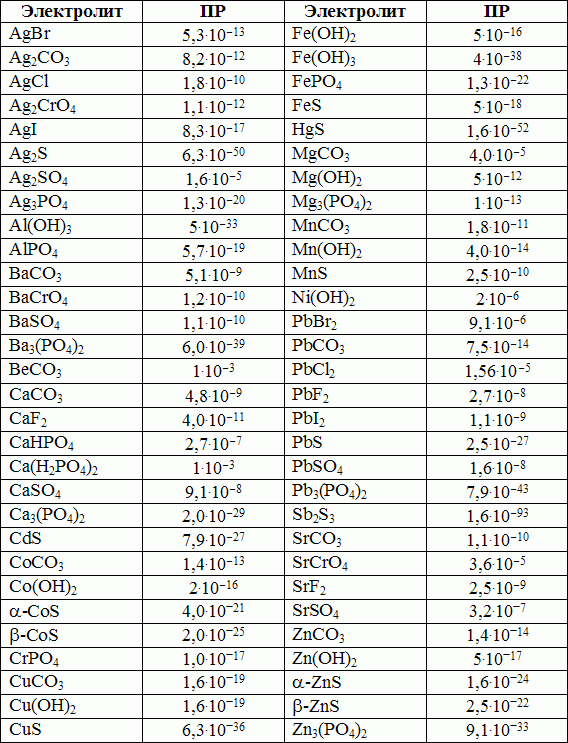
Таблица 3.
Произведение растворимости некоторых соединений
Таблице 4
Стандартные электродные потенциалы в водных растворах при 250С
| № п/п | электрод | реакция | φ0,В |
| Электроды, обратимые относительно катиона | |||
| H+,H | H+ + ē = H | –2,106 | |
| Al3+,Al | Al3+ + 3ē = Al | –1,662 | |
| Zn2+,Zn | Zn2+ + 2ē = Zn | –0,763 | |
| Fe2+,Fe | Fe2+ + 2ē = Fe | –0,440 | |
| Cd2+,Cd | Cd2+ + 2ē = Cd | –0,403 | |
| Ni2+,Ni | Ni2+ + 2ē = Ni | –0,250 | |
| Sn2+,Sn | Sn2+ + 2ē = Ni | –0,136 | |
| Pb2+,Pb | Pb2+ + 2ē = Pb | –0,126 | |
| Fe3+,Fe | Fe3+ + 3ē = Fe | –0,036 | |
| H+,H2 | H+ + ē = ½H2 | 0,000 | |
| Cu2+,Cu | Cu2+ + 2ē = Cu | 0,337 | |
| Cu+,Cu | Cu+ + ē = Cu | 0,521 | |
| Ag+,Ag | Ag+ + ē = Ag | 0,799 | |
| Hg22+,Hg | ½ Hg22+ + ē = Hg | 0,798 | |
| Электроды, обратимые относительно аниона | |||
| O2, OH– | 1/2O2 + H2O + 2ē = 2OH– | 0,401 | |
| Br2(ж),Br – | 1/2Br2 + ē = Br– | 1,065 | |
| Cl2(г ) ,Cl | 1/2Cl2 + ē = Cl– | 1,360 | |
| Электроды второго рода | |||
| Al, Al(OH)3, OH– | Al(OH)3 +3ē = Al + 3OH– | –2,30 | |
| Zn, Zn(OH)2, OH– | Zn(OH)2+ 2ē =Zn + 2OH– | –1,245 | |
| Cd, Cd(OH)2, OH– | Cd(OH)2+ 2ē =Cd + 2OH– | –0,809 | |
| Ag, AgCl, Cl– | AgCl + ē= Ag + Cl– | 0,222 | |
| Hg, Hg2Cl2, Cl– | 1/2Hg2Cl2 + ē = Hg + Cl– | 0,268 | |
| Ag, Ag2SO4, SO42– | Ag2SO4 + 2ē = Ag + SO42– | 0,654 | |
| Pb, PbSO4, SO42– | PbSO4 + 2ē = Pb + SO42– | –0,359 |
| Окислительно–восстановительные электроды | |||
| Sn4+, Sn2+(Pt) | Sn4+ + 2ē = Sn2+ | 0,15 | |
| Cu2+, Cu+(Pt) | Cu2+ + ē = Cu+ | 0,153 | |
| Fe3+, Fe2+(Pt) | Fe2+ – ē = Fe3+ | 0,771 |
Таблица 5.
Константы нестойкости комплексных ионов.
| Комплексный ион | Кн. |
| [Ag(NH3)2]+ | 9,3∙10–8 |
| [Cu(NH3)4]2+ | 2,1∙10–13 |
| [Zn(OH)4]2– | 3,6∙10–16 |
| [Fe(CN)6]3– | 1,0∙10–31 |
| [Fe(CN)6]4– | 1,0∙10–36 |
Таблица 6.
Значения констант диссоциации некоторых кислот
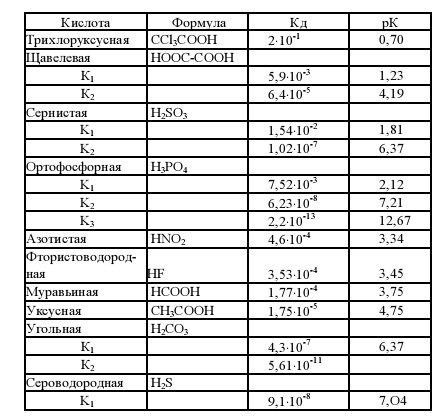
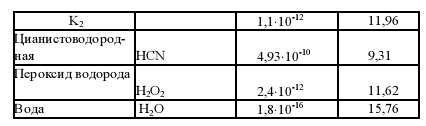
Таблица 7.
Значение рКа некоторых органических соединений
| Кислота | рКа |
| Хлорная Азотная Соляная Серная Бензолсульфокислота Тринитрометан | <0 Сильные кислоты |
| Пикриновая Трихлоруксусная Щавелевая Сернистая Фосфорная Хлоруксусная Азотистая Бензойная Уксусная Пиридиний-катион Лимонная Сероводородная Борная Аммоний-ион Фенол Нитрометан Этилмеркаптан Вода Этиловый спирт Ацетон Анилин Аммиак Толуол Метан | 0,4 0,7 1,2 1,8 2,1 2,9 3,3 4,2 4,7 5,2 5,4 7,2 9,2 9,2 9,9 11,0 12,0 14,0 18,0 20,0 27,0 30,0 35,0 40,0 |
СПИСОК ЛИТЕРАТУРЫ
- Аналитическая химия и физико-химические методы анализа [Текст]: учебник для студентов, обуч. По хим.-технол. Направлениям и спец.: в 2т. Т.1/Ю.М. Глубоков [и др.]; под ред. А.А. Ищенко. – М.: Академия, 2010.-352с.: ил.-(Высшее профессиональное образование. Химические технологии).
2. Попков В.А. Общая химия [Электронный ресурс]: учебник/ Попков В.А., Пузаков С.А. - М.: ГЭОТАР – Медиа, 2010, 976 с. – Режим доступа: http: //studmedlib.ru
3. Саенко О.Е. «Аналитическая химия» [Текст]: учебник для сред. спец. учеб. заведений/О.Е. Саенко.-Изд. 2-е допю и перераб.- Ростов. н/Д. «Феникс», 2011-288с.: ил.- (Среднее профессиональное оьразование).
4. Харитонов Ю.А., Григорьева В.Ю. Аналитическая химия.[Электронный ресурс] Практикум. Качественный химический анализ: учеб. пособие/ Ю.А. Харитонов, В.Ю. Григорьева. – М.: ГЭОТАР – Медиа, 2009. -296с. - Режим доступа: http: //studmedlib.ru
5. Харитонов Ю.А., Григорьева В.Ю. Примеры и задачи по аналитической химии [Электронный ресурс]: учеб. пособие/ Ю.А. Харитонов, В.Ю. Григорьева. – М.: ГЭОТАР – Медиа, 2009. -296с. - Режим доступа: http: //studmedlib.ru
ДЛЯ ЗАПИСЕЙ
