Свойства растворов электролитов
1. Электролиты – это вещества, которые … .
1) увеличивают скорость химических реакций
2) характеризуются отсутствием ионов в растворе
3) в воде и других полярных растворителях, а также при расплавлении, распадаются (диссоциируют) на ионы
4) способны поглощать, адсорбировать другое вещество
2. Наименьшей частицей растворённого вещества в растворах электролитов является … .
1) нейтральный атом 2) молекула
3) ион 4) электрон
3. Процесс распада веществ на ионы под действием полярных молекул растворителя называется … .
1) электролизом
2) гидролизом
3) термической диссоциацией
4) электролитической диссоциацией
4. Электролитической диссоциации подвергаются химические соединения, содержащие … .
1) ковалентные неполярные или ионные связи
2) ковалентные сильно полярные или ионные связи
3) ковалентные неполярные или ковалентные полярные связи
4) любые химические связи
5. Степенью электролитической диссоциации (α) называется отношение … .
1) количества электролита в растворе к объёму раствора
2) числа молекул электролита к числу молекул растворителя
3) числа молей электролита, распавшегося на ионы, к общему числу молей электролита в данном растворе
4) числа гидратированных молекул электролита к объёму раствора
6. Степень диссоциации электролита в растворе при данной температуре зависит от … .
1) давления
2) наличия катализатора
3) природы и концентрации электролита
4) агрегатного состояния электролита
7. Степень ионизации уксусной кислоты уменьшается при добавлении … .
1) NаСl 2) Н2О
3) СН3СООNа 4) КОН
8. При разбавлении раствора степень диссоциации электролита … .
1) увеличивается 2) уменьшается
3) не изменяется 4) изменяется неоднозначно
9. Для слабого электролита АВ закон разбавления Оствальда выражается формулой … .
1) 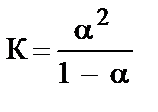 · сАВ 2) К =
· сАВ 2) К = 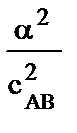
3) К = (1 + α) · с2АВ 4) К = (1 – α) · сАВ
10. Слабые электролиты … .
1) практически полностью диссоциируют
2) имеют степень диссоциации, близкую к единице
3) диссоциируют в малой степени
4) не диссоциируют
11. Величиной, которая характеризует степень диссоциации электролита и не зависит от его концентрации, является … .
1) рН раствора
2) константа диссоциации
3) ионное произведение воды
4) степень диссоциации
12. Константа диссоциации для процесса
АВ  А+ + В–
А+ + В–
определяется выражением … .
1) К = [АВ] · [А+] · [В–] 2) 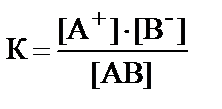
3) 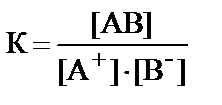 4) К = [АВ]
4) К = [АВ]
13. Для констант ступенчатой диссоциации ортофосфорной кислоты Н3РО4 соблюдается неравенство … .
1) К1 > К2 < К3 2) К1 < К2 > К3
3) К1 > К2 > К3 4) К1 < К2 < К3
14. Константа диссоциации слабого электролита не зависит от … .
1) концентрации раствора
2) температуры
3) природы электролита
4) природы растворителя
15. Сильными электролитами являются … .
1) хромат калия 2) ацетат натрия
3) уксусная кислота 4) азотистая кислота
16. Для веществ СН3СООН и СН3СООК верно, что … .
1) оба вещества – сильные электролиты
2) оба вещества – слабые электролиты
3) только второе вещество – сильный электролит
4) только первое вещество – сильный электролит
17. Лампочка прибора для испытания веществ на электрическую проводимость загорится при погружении электродов в … .
1) растворы сахарозы и глюкозы
2) растворы хлорида натрия и уксусной кислоты
3) ацетон и в крахмальный клейстер
4) глицерин и в расплав гидроксида натрия
18. Слабыми электролитами являются … .
1) хлорид натрия и этанол
2) уксусная и сероводородная кислоты
3) нитрат кальция и уксусная кислота
4) хлорид кальция и метанол
19. Концентрация ацетат-ионов наименьшая в 0,1 М растворе … .
1) СН3СООNа 2) СН3СООК
3) СН3СООН 4) СН3СООАg
20. Концентрация ионов NН4+ наименьшая в 0,1 М растворе … .
1) нитрата аммония 2) сульфата аммония
3) хлорида аммония 4) аммиака
21. Ионы водорода образуются при ионизации … .
1) КОН 2) Н2SО4 3) Са(ОН)2 4) FеОНВr
22. Ионы Мn2+ образуются при электролитической диссоциации … .
1) КМnО4 2) МnО2
3) К2МnО4 4) МnSО4
23. Многоосновные кислоты и многокислотные основания диссоциируют … .
1) быстро 2) медленно
3) ступенчато 4) необратимо
24. Электролитическая диссоциация воды описывается уравнением … .
1) Н2О  Н+ + ОН– 2) Н2О
Н+ + ОН– 2) Н2О  Н2+ + О2–
Н2+ + О2–
3) Н2О  Н– + ОН+ 4) Н2О
Н– + ОН+ 4) Н2О  2Н+ + О2–
2Н+ + О2–
