Пояснения к синтезам бензойной кислоты (2.5.2 и 2.5.3)
Конец реакции окисления определяют по исчезновению малиновой окраски перманганата калия. Для этого каплю реакционной смеси наносят на фильтровальную бумагу. Если весь перманганат прореагировал, в месте нанесения капли остается черное пятно МnО2, а растекающийся водный раствор бесцветен. Такую пробу можно проводить только в том случае, если перманганат заведомо взят в некотором недостатке по отношению к окисляемому веществу. В противном случае можно контролировать присутствие окисляемого вещества в парах, выходящих из реакционной колбы, и прекращать реакцию, как только оно в них исчезнет. Так поступают, например, при получении бензойной кислоты из бензилового спирта. Избыток перманганата удаляют, добавляя в реакционную смесь какой-либо восстановитель: сульфит или бисульфит натрия, этиловый спирт, формальдегид и т.п. Например,
2 KMnO4 + 3 C2H5OH 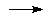 3 CH3CHO + 2 MnO2 + 2 KOH + 2 H2O
3 CH3CHO + 2 MnO2 + 2 KOH + 2 H2O
этиловый спирт ацетальдегид
Образующийся при окислении этилового спирта уксусный альдегид не загрязняет основной продукт – бензойную кислоту, так как, имея низкую температуру кипения, улетает из реакционной смеси.
На примере последней реакции можно показать, как обычно уравниваются органические реакции окисления-восстановления.
2 KMnO4 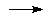 2 MnO2 + 2 KOH + 3 O 2 MnO2 + 2 KOH + 3 O | (1) |
CH3CH2OH + O 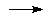 CH3CHO + H2O CH3CHO + H2O | (2) |
Полуреакция (1) отражает процесс восстановления перманганата в щелочной среде. Полуреакция (2) – процесс окисления спирта до альдегида. Умножая стехиометрические коэффициенты полуреакции (2) на три и складывая после этого уравнения (2) и (1), получают полное уравнение окисления этанола.
При проведении синтеза бензойной кислоты требуется энергичное перемешивание. По мере прохождения реакции выпадает тяжелый осадок диоксида марганца, поэтому даже при незначительных перегревах наблюдаются толчки неравномерно кипящей смеси, что может привести к растрескиванию реакционного сосуда. Чтобы избежать этого, целесообразно перед началом синтеза в колбу положить “кипелки”, например, осколки фарфора.
Следует иметь в виду, что продуктом окисления как толуола, так и бензилового спирта перманганатом калия является не свободная бензойная кислота, а ее калиевая соль, растворенная в воде. Свободную кислоту выделяют путем подкисления водного раствора калиевой соли. Малорастворимая в холодной воде бензойная кислота выпадает в осадок. Необходимо учитывать, что соляная кислота расходуется также и на нейтрализацию образовавшейся в ходе реакции щелочи. При расчете количества соляной кислоты, необходимой для нейтрализации щелочи и превращения бензоата калия в свободную бензойную кислоту, можно руководствоваться правилом: количество эквивалентов кислоты должно быть равно количеству молей взятого KMnO4.
Контрольные вопросы
1. Зачем при получении бензойной кислоты из толуола или бензилового спирта реакционный сосуд снабжают обратным холодильником? С какой целью в колбу добавляют осколки фарфора?
2. Напишите уравнения окисления марганцовокислым калием в водной среде: а) сульфита натрия; б) формальдегида.
3. Рассчитайте, сколько миллилитров соляной кислоты с плотностью 1,18 г/см3 требуется добавить к реакционной смеси для осаждения бензойной кислоты при синтезе ее по применяемой методике?
4. Проведите сравнительную характеристику физических свойств толуола или бензилового спирта и бензойной кислоты (в зависимости от используемой методики).
5. Почему конечный продукт промывают ледяной водой?
6. Какая кислота более сильная: уксусная или бензойная? Как влияет строение кислоты на ее силу?
7. Как зависит сила бензойных кислот от наличия в их молекулах электроноакцепторных или электронодонорных заместителей?
