Задание 2. Приготовление аншлифа. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СВОБОДНОЙ ИЗВЕСТИ В КЛИНКЕРЕ
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СВОБОДНОЙ ИЗВЕСТИ В КЛИНКЕРЕ.
ДОПУСК______________________
ВЫПОЛНЕНИЕ________________
ЗАЩИТА______________________
Цель работы: освоить метод определения СаОсв в клинкере, (цементе), по содержанию СаО оценить качество клинкера.
Влияние свободной извести на качество цемента
Для получения цемента высокого качества необходимо, чтобы оксид кальция находился в нём не в свободном виде, а в химическом соединении с кислотными оксидами SiO2, Al203, Fe203 в виде клинкерных минералов 3CaO·SiO2, 2СаО·SiO2, ЗСа0·Аl203, 4СаО·Al203·Fe203.
При обжиге цементного клинкера иногда в силу ряда причин часть оксида кальция не усваивается и остается в виде так называемой свободной извести. Полнота усвоения СаО зависит от состава и качества приготовления сырьевой смеси и режима обжига. Так, при высоком коэффициенте насыщения обжигаемого материала (КН = 0,94), повышенном содержании щелочных соединений в нем, грубом помоле и плохом смешивании сырья, а также при недостаточно высокой температуре и малой продолжительности обжига в клинкере может оставаться свободная несвязанная известь (СаОсв).
В промышленных условиях клинкер обжигают при температуре 1450°С с выдержкой 20 - 40 мин, при этом в клинкере образуется крупнокристаллическая "намертво" обожжённая свободная известь, которая гасится в течение длительного времени. При гидратации по уравнению CaO + H2O = Ca(OH)2 известь увеличивается в объеме почти в два раза. Если содержание такой извести в цементе более 1-2%, она реагирует с водой уже после того, как цементное тесто схватилось и затвердело. Возникающие в этих условиях большие внутренние напряжения могут разрушить бетонные сооружения из-за неравномерности изменения объема цемента.
В отличие от СаОсв в клинкере строительная известь, обожженная в известковых печах при 1000-1100°С гасится в течение 15-20 мин.
Определение содержания свободной извести имеет большое значение для контроля качества обжига клинкера.
Приборы и реактивы
Клинкер; мел; известь; реактив Уайта; ступка с пестиком; микроскоп с осветителем; предметное стекло; покровные стекла; микрошпатель; фильтровальная бумага; цемент; 0,1н. спиртовой раствор бензойной кислоты; безводный глицерин; хлористый барий; абсолютный этиловый спирт; 12-ный спиртовой раствор фенолфталеина; сито ЖЗО63; колба коническая 150 мл сухая; обратный холодильник; электроплитка; бюретка с раствором бензойной кислоты для титрования; капельница с фенолфталеином; часовое стекло и кисточка для перенесения навески в колбу.
Порядок выполнения работы.
Задание 1. Качественное определение СаОсв реактивом Уайта под микроскопом.
Реактив Уайта представляет собой смесь фенола с нитробензолом в соотношении 1:1, содержащую несколько капель дистиллированной води. Нитробензол не участвует в реакции, являясь лишь растворителем фенола, так как последний при комнатной температуре может находиться только в кристаллическом состоянии. Несколько капель воды, добавленные при приготовлении реактива Уайта, ускоряют реакцию образования фенолята кальция.
Тонко растертый порошок клинкера (мела, извести) помещают на предметное стекло микрошпателем, закрывают тонким покровным стеклом, под которое вводят одну каплю реактива Уайта. Осторожным круговым движением порошок, смоченный реактивом, равномерно распределяют под стеклом. Избыток реактива Уайта можно отсосать фильтровальной бумагой. Подготовленный препарат помещают на столик микроскопа. Наблюдения ведут в проходящем свете в темном поле.
Через несколько минут вокруг зерен свободного оксида кальция появляются длинные перистые кристаллики фенолята кальция, хорошо различимые при скрещенных николях микроскопа по их интерференционной окраске.
Микрохимическая реакция на свободную известь имеет качественный характер, т.е. позволяет определить, есть или нет свободная неусвоенная известь.
В условиях проведения систематических наблюдений над клинкером возможно произвести градуировку микрохимической реакции. Для этой цели необходимо изготовлять микрохимические препараты таким образом, чтобы в поле зрения получалось одинаковое количество зерен цементного порошка. Путем подсчёта числа гнезд фенолята кальция в различных препаратах, изготовленных из цементов с различным (определенным другими методами) содержанием СаОсв .можно установить соотношение между количеством оксида кальция и числом возникших гнезд фенолята кальция.
В образцах с содержанием СаОсв меньше 1...2% можно подсчитать количество гнезд фенолята кальция. В пробах же с большим содержанием свободной извести фенолята кальция так много, что он закрывает все поле зрения и дифференцировать, а следовательно, и подсчитать гнезда фенолята кальция не представляется возможным.
В лабораторный журнал зарисовать изображения, наблюдаемые под микроскопом, и дать характеристику исследуемых материалов по содержанию свободной извести.
Задание 2. Приготовление аншлифа.
Этилово-глицератный метод, разработанный Э.И.Нагеровой, Н.И. Колендзян, пригоден для определения суммарного содержания свободной извести как в виде СаО, так и в виде Са(ОН)2. Метод основан наобработке цементов горячей смесью безводного глицерина и абсолютного спирта. При взаимодействии с содержащейся в цементе несвязанной извести с безводным глицерином образуется глицерат кальция (1). Этот глицерат титруют спиртовым раствором бензойной кислоты (2), образуется бензокислый кальций:
 СН2ОН СН2ОН  СНОН + СаО = СН2ОН СНОН + СаО = СН2ОН |   СН2О СН2О 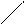  СНОН Са + Н2О ; (1) СН2О СНОН Са + Н2О ; (1) СН2О | |
  СН2О СН2О 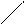  СНОН Са + 2С6Н5СООН = СН2О СНОН Са + 2С6Н5СООН = СН2О | СН2ОН СНОН + Са(С6Н5СОО)2 ; (2) СН2ОН | |
В раствор переходит лишь глицерат кальция. Свободный оксид магния не вступает в реакцию с глицерином. Затруднения при определении свободной извести вызваны невозможностью применения водных растворов, вступающих во взаимодействие с клинкером, так как в этом случае в результате гидролиза алита по реакции
C3S + Н O →CSH + Ca(0H)2
выделяется гидроксид кальция, который может быть оттитрован.
Из всех количественных методом определения свободной извести этилово-глицератный метод принят в общественном стандарте и получил наибольшее распространение.
В сухую коническую колбу объемом 150 мл, содержащую 10 мл раствора глицерина, хлористого бария, фенолфталеина, Решенную на аналитических весах навеску 0,1 г клинкера; цемента, свежеизмельченного и пропущенного через сито 0063 (10000 отв./см2). Колбу присоединяют с помощью пробки к обратному холодильнику. Содержимое колбы, периодически встряхивая, кипятят в течение 10 мин над электрической плиткой. Появление окраски зависит от количества содержащейся в цементе свободной извести. Если после получасового непрерывного кипячения окраска не появилась, можно считать, что свободный СаО в пробе отсутствует.
При появлении розовой окраски кипящую жидкость через каждые 10...15 мин титруют раствором бензойной кислоты. Нагревание и титрование повторяют до тех пор, пока не прекратится появление розовой окраски после 15...20 мин кипячения. Тогда титрование можно считать законченным. Содержание свободной извести в процентах подсчитывают по следующей формуле:
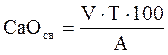
где v - объем раствора бензойной кислоты, пошедшей на титрование, мл; А - сухая навеска, г; Т - титр бензойной кислоты, т.е. количество СаО, которое связывается в 1 мл раствора бензойной кислоты по реакции (2).
________________________
________________
