Рубеановодородная кислота (дитиооксамид)

Оранжевые кристаллы; умеренно растворяется в воде и этиловом спирте, растворяется в концентрированной серной кислоте с образованием красного раствора.
Применяют для количественного осаждения меди, никеля и кобальта.
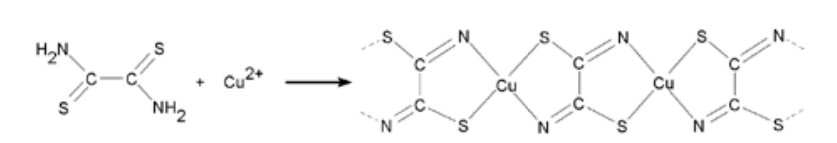 Медный комплекс окрашен в зеленый цвет (уравнение 4):
Медный комплекс окрашен в зеленый цвет (уравнение 4):
(4)
Комплекс кобальта – в буровато-красный, а никеля – в фиолетовый. Из-за исключительной прочности и яркой окраски комплексов реакции их образования обладают высокой аналитической чувствительностью. Самый прочный из них комплекс меди; он выпадает в осадок даже из умеренно кислого раствора, а для осаждения комплексов кобальта и никеля требуется буферная среда. Палладий, платина и серебро дают осадок с рубеановодородной кислотой в сильно кислом растворе. Однако вместо комплексов с рубеановодородной кислотой получаются сульфиды платины и некоторых других металлов (цинк, кадмий, серебро, свинец, медь).
С рутением рубеановодородная кислота образует синий, растворимый в воде комплекс, который используется для спектрофотометрического определения этого металла.
Подобным образом использовали этот реагент для спектрофотометрического определения осмия.
Реагент пригоден для экстракционного отделения и определения таллия. Установлено, что талий существует в органической фазе в виде комплекса состава Tl(dto)Hdto, где dto означает анион рубеановодородной кислоты с одним отрицательным зарядом.[2,3]
2.3 Тионалид ( β-аминонафталид тиогликолевой кислоты)
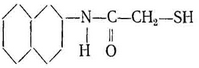
Белые или светло-желтые иглы; умеренно растворим в воде, легко растворяется в органических растворителях. Растворимость в воде значительно увеличивается при добавлении небольших количеств этилового спирта или уксусной кислоты.
Тионалид взаимодействует с различными ионами металлов, давая хелатные комплексы, умеренно растворимые в воде. Различия в прочности комплексов в некоторых случаях позволяют проводить избирательные аналитические реакции.
1) Медь (II), серебро (I), ртуть (II), висмут (III), мышьяк (III), олово (IV), золото (I), платина (IV) и палладий (II) осаждаются реагентом в кислой среде.
2) Ртуть (II), кадмий (II), таллий (I) и золото (I) осаждаются из щелочных растворов, содержащих тартрат.
3) Комплексы таллия (I), сурьмы (III) и висмута (III) осаждаются реагентом из растворов, содержащих цианид и тартрат.
4) Комплекс таллия (I) осаждается также из щелочного раствора (едкий натр), содержащего цианид и тартрат.
Из этого подразделения на группы видно, что реакция может быть специфической для таллия при установлении подходящего значения pH раствора и применении маскирующих реагентов. Таким же образом можно повысить избирательность реакции в отношении других ионов, применяя другие маскирующие реагенты. Например, олово (IV) избирательно маскируют в присутствии мышьяка (III) и сурьмы (III) фосфорной кислотой, а эти ионы осаждают трионалидом.
Аналитическое применение тионалида обуславливается тем, что комплексы его с металлами имеют стехиометрический состав, их можно сушить при 105°-110°С и непосредственно взвешивать.[2]
