Определение активности липазы
В растениях липазы широко распространены. Особенно их много в семенах масличных культур. У каждого вида растений есть свои липазы, проявляющие свою активность при различных значениях рН, потому иногда различают кислую, нейтральную и щелочную липазы, которые проявляют свою максимальную активность соответственно в кислой, нейтральной или щелочной среде. В семенах масличных культур содержатся в основном кислые и щелочные липазы.
Принцип метода. Основан на определении количества жирных кислот, образующихся при действии липаз на растительный жир. В качестве источника липаз используют семена масличных культур. Титрование образовавшихся кислот щелочью происходит по схеме:
RСООН + NаОН ¾¾¾® RСООNа + Н2О
Активность липаз определяют в слабокислой или щелочной среде.
Ход работы. 2–3 г масличных культур растирают в ступке, в растертую массу добавляют 50 мл кислого или щелочного буфера и смесь тщательно перемешивают. Кислый ацетатный буфер (рН = 4,7) готовят смешиванием разных объемов растворов 1 н. уксусной кислоты и 1 н. уксусного натрия или уксусного аммония и 2 объемов воды. Для приготовления щелочного боратного буфера (рН = 8,5) растворяют в воде 12,404 г борной кислоты, прибавляют 100 мл 1 н NаОН и доводят общий объем раствора до 1 л. Из этого раствора берут 650 мл, прибавляют к нему 350 мл, 0,1 н раствора НСl и тщательно перемешивают. Полученные смеси переносят в центрифужные пробирки и центрифугируют 10–15 мин 5 тыс. об/мин. Для определения ферментативной активности из каждой пробирки берут 2 пробы по 20 мл и переносят их в конические колбы на 100 мл с притертыми пробками. Содержимое одной из колб кипятят 3 минуты для инактивации ферментов. Затем в колбы вносят по 1 мл чистого подсолнечного масла, которое служит субстратом для действия липаз, добавляют по 5 капель толуола, перемешивают и ставят в термостат при 30 °С на 20–24 ч.
После инкубации в термостате во все колбы приливают по 50 мл смеси этилового спирта с эфиром (4:1) и взбалтывают. После отстаивания титруют 0,1 н спиртовым раствором NаОН в присутствии нескольких капель тимолфталеина.
Вычисление результатов. Активность кислых и щелочных липаз выражают в миллилитрах 0,1 н. NаОН, пошедшей на нейтрализацию жирных кислот, образовавшихся в результате действия липаз на 1 г семян. Расчеты проводят по формуле:
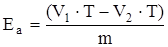 , (18)
, (18)
где Еа – активность липазы, мл/г;
V1 – количество 0,1 н. NаОН, израсходованное для титрования опытного образца, мл;
V2 – количество 0,1 н NаОН, израсходованное для титрования контрольного (предварительно прокипяченного) образца, мл;
Т– поправка к титру 0,1 н. NаОН;
m – навеска семян, соответствующая объему вытяжки (20 мл), взятому для определения ферментативной активности, г.
Материалы и реактивы. Ацетатный буфер рН 4,7 (см. Приложение 1, п.10);
0,2 М боратный буфер рН 8,5; 0,1 н. NаОН; этиловый спирт; эфир; подсолнечное масло; толуол; 1 %–ный спиртовой раствор тимолфталеина.
Оборудование. Автоматическая мешалка; термостат; ступки фарфоровые; конические колбы на 100 мл с притертыми пробками; пипетки.
Приложение 1
1. В нескольких мл воды растворяют 1 г йодистого калия, затем растворяют 1 г йода и доливают водой до 300 мл; 3 г йодистого калия растворяют в 70 мл воды в мерной колбе емкостью 100 мл добавляют 0,3 г. растертого в ступке йода и после растворения йода доводят водой до метки. Раствор хранят в темной склянке.
2. Фосфатный буфер, 0,1 М раствор, рН = 5,6. Состоит из двух растворов:
а) 0,1 М раствор двухзамещенного фосфорнокислого натрия (17,8 г Na2НРО4 ×2Н2О или 35,82 Na2НРО4 × 12 Н2О в 1 л);
б) 0,1 М раствор однозамещенного фосфорнокислого натрия (18,8 г NaН2РО4 × Н2О или 31,21 г NaН2РО4 .2Н2О в 1 л). При смешивании 4,0 мл раствора "а" и 96 мл раствора "б" получают буферную смесь м рН 5,6.
3. Фелинг II. 200 г сегенетовой соли растворяют в 500 мл воды, 150 г гидроксида натрия растворяют в 300 мл воды, затем раствор щелочи осторожно приливают к раствору соли и объем доводят водой до 1 л.
4. Железоаммиачные квасцы, раствор. 86 г железоаммиачных квасцов растворяют в 500 мл воды и осторожно по стенкам приливают 200 г (108 мл) концентрированной серной кислоты, объем доводят водой до 1 л.
5. (9,077 г/л КН2РО4 и 23,283 г/л Nа2РО4×12Н2О); для приготовления буфера смешивают 5,5 мл первого раствора и 94,5 мл второго раствора.
6. Приготовление 0,1 %–ного раствора казеина. 3,8 г Nа3РО4 ×12Н2О растворяют в 80 мл дистиллированной воды при 40 °С, добавляют 100 мг казеина и после полного растворения последнего устанавливают рН смеси 1 н. НСI на уровне 6.5; объем раствора доводят дистиллированной водой.
7. Реактив Фолина. В круглодонную колбу на 1,5–2,0 л вносят 100 г вольфрамовокислого натрия–гидрата (NaWО4 .2Н2О), 25 г молибденовокислого натрия–гидрата (NaМоО4 ×2Н2О), 750 мл дистиллированной воды, 50 мл 85% фосфорной кислоты Н3РО4 и 100 мл концентрированной соляной кислоты, после чего смесь нагревают при умеренном кипячении с обратным холодильником. После кипячения прибавляют 150 г сернокислого лития 50 мл дистиллированоой воды, 5 капель бромной воды. Избыток удаляют кипячением под тягой без холодильника в течении 30 минут,после чего жидкость охлаждают и разводят дистиллированной водой до 1 литра. Хранят в темной склянке. Перед употреблением реактив разводят водой в отношении: реактива: 3 части дистиллированной воды.???
8. 1 г казеина растворяют при нагревании на водяной бане в 10 мл 10 %–ной НСI и прибавляют воды до объема 1000 мл;
9. Ацетатный буфер, 0,3 М раствор, рН 4,7. Состоит из двух растворов в соотношении 1:1:
а) 0,3 М раствор уксусной кислоты;
б) 0,3 М раствор уксуснокислого натрия.
10. Крахмал индикатор. 1 г. растворимого крахмала размешивают с 10 мл холодной воды и постепенно вливают в 90 мл кипящего насыщенного раствора хлорида натрия, нагревают до кипения и охлаждают.
11. Фосфорнокислые соли, раствор. (6 г Na2НРО4×2Н2О смешивают с 2 г КН2РО4× Н2О в 1,0 л воды).
12. 50 г (по сухому веществу) технического измельченного казеина помещают в стакан, добавляют для набухания 50 мл дистиллированной воды и оставляют на 30 мин, затем стакан помещают на водяную баню с температурой 65–70°С. Постепенно при тщательном перемешивании стеклянной палочкой прибавляют 50 мл 1 н. раствора NаОН. В процессе растворения казеина прибавляют небольшими порциями воду (5–6 раз по 50–80 мл.), нагретую до 65–70 °С, и выдерживают на бане до полного исчезновения комочков. После полного растворения казеина и охлаждения объем раствора доводят в мерной колбе до 1 л; фильтруют через четыре слоя марли.
13. Раствор фермента.
а) для технического ферментного препарата (культура гриба) из тщательно измельченной воздушно–сухой средней пробы берут в колбу на 300–200 мл навеску 1 г (с точностью до 0,01), приливают пипеткой 50–100 мл дистиллированной воды и настаивают 1 ч при комнатной температуре, перемешивая через каждые 10 мин; по истечении 1 ч раствор фильтруют через складчатый фильтр;
б) для очищенных ферментных препаратов: на аналитических весах берут навеску средней пробы тонко измельченного препарата 0,1 г (с точностью до 0,0001), препарат тщательно растирают стеклянной палочкой в небольшом количестве воды, затем переводят в мерную колбочку на 100 мл и доводят дистиллированной раствор до метки, раствор фильтруют.
14. 2 г растительного материала растирают в ступке с песком с 5 мл фосфорного буфера, рН 7,0; переносят в коническую колбу вместимостью 50 мл, смывают ступку 20 мл буфера, настаивают 30 мин и центрифугируют 10–15 мин при 4000 об/мин.
15. На аналитических весах отвешивают по разности в мерную колбу (вместимостью 50 мл) 2 г муки или хорошо измельченного растительного продукта. В колбу приливают дистиллированную воду, содержимое ее хорошо перемешивают, добавляют 2–3 капли толуола, доводят водой до метки и смесь настаивают 2 ч при комнатной температуре. Затем жидкость отфильтровывают через сухой складчатый фильтр или центрифугируют. В фильтрате или центрифугате тот час же определяют каталазу.
16. Реактив А: (2 г NaOH и 10 г Na2CO3 в 500 мл дистиллированной воды); реактив В: (5 мл 1,1 %–ного раствора калия–натрия виннокислого + 0,5 мл 5,5 %–ного раствора CuSO4×5Н2О); реактив С (50 мл реактива А + 1 мл реактива В) готовится перед каждой работой заново;
17. Раствор ферментов: 250 мкг глюкозооксидазы из плесневого гриба и 41,7 мкг пероксидазы из корней хрена растворяют в 10 мл 0,1 М Nа–фосфатного буфера, рН 7,0.
18. 1 %– ный раствор казеина рН 8,0: 1 г казеина заливают 100 мл 1/5 М фосфатного буфера рН 8,0 и нагревают на водяной бане до полного растворения. Проверяют рН раствора и доводят его точно до 8,0. Раствор казеина можно хранить в холодильнике не более трех суток.
19. 1 %–ный раствор гемоглобина рН 3,0 готовят растиранием в ступке 1,0 г гемоглобина с небольшим количеством воды. Содержимое ступки переносят в мерную колбу на 100 мл, подкисляют 0,3 н. НСl до рН 3,0 и доводят водой до метки. Полученный раствор неустойчив, его следует готовить ежедневно.
Для приготовления растворов гемоглобина с рН 6,0 и 8,0 растворяют в 100 мл 1/15 М фосфатного буфера с соответствующим значением рН 1,1 г гемоглобина, затем в раствор добавляют 36 г мочевины и оставляют при комнатной температуре. После этого растворы доводят до нужного значения рН 1 н. NаОН или 1 н. НСl
Приложение 2
Таблица 5 – Международная классификация ферментов
| № | Класс | Тип катализируемой реакции | Пример реакций |
| 1. | Оксидоре-дуктазы | Перенос электронов и протонов | |
| 2. | Трансфе-разы | Перенос групп атомов (исключая Н) | |
| 3. | Гидро-лазы | Гидролиз различных связей (с участием молекул воды) | |
| 4. | Лиазы | Оброзование двойных связей за счет удаления групп или добавления групп за счет разрыва двойных связей | |
| 5. | Изомера-зы | Внутримолекулярный перенос групп с образо– ванием изомерных форм | |
| 6. | Лигазы (синтета-зы) | Соединение двух молекул и образование связей С¾С, С¾О, С¾N, сопряженных с разрывом пирофосфатной связи АТФ |
Приложение 3
Таблица 6
Ер на воздушно–сухое вещество
| 0,1 н. NаОН, мл на 10мл фильтрата | Единицы протеолитической активности, е | ПС при введении 10мл раствора при разведении | |
| 1:100 | 1:50 | ||
| 0.30 | 0.0123 | 0.615 | 0.300 |
| 0.35 | 0.0167 | 0.835 | 0.418 |
| 0.40 | 0.0203 | 1.015 | 0.508 |
| 0.45 | 0.0243 | 1.215 | 0.608 |
| 0.50 | 0.0283 | 1.415 | 0.708 |
| 0.55 | 0.0320 | 1.600 | 0.800 |
| 0.60 | 0.0360 | 1.800 | 0.900 |
| 0.65 | 0.0393 | 1.965 | 0.982 |
| 0.70 | 0.0433 | 2.165 | 1.082 |
| 0.75 | 0.0473 | 2.365 | 1.182 |
| 0.80 | 0.0513 | 2.565 | 1.282 |
| 0.85 | 0.0550 | 2.750 | 1.375 |
| 0.90 | 0.0590 | 2.950 | 1.475 |
| 0.95 | 0.0627 | 3.135 | 1.573 |
| 1.00 | 0.0667 | 3.335 | 1.663 |
| 1.05 | 0.0700 | 3.500 | 1.750 |
| 1.10 | 0.0747 | 3.735 | 1.868 |
| 1.15 | 0.0787 | 3.935 | 1.968 |
| 1.20 | 0.0827 | 4.135 | 2.068 |
| 1.25 | 0.0867 | 4.335 | 2.168 |
| 1.30 | 0.0907 | 4.535 | 0.375 |
| 1.35 | 0.0950 | 4.750 | 2.268 |
| 1.40 | 0.0990 | 4.950 | 2.475 |
| 1.45 | 0.1033 | 5.165 | 2.582 |
| 1.50 | 0.1080 | 5.400 | 2.700 |
| 1.55 | 0.1123 | 5.616 | 2.808 |
| 1.60 | 0.1167 | 5.835 | 2.918 |
| 1.65 | 0.1213 | 6.065 | 3.032 |
| 1.70 | 0.1260 | 6.300 | 3.150 |
| 1.75 | 0.1307 | 6.535 | 3.266 |
| 1.80 | 0.1353 | 6.765 | 3.382 |
| 1.85 | 0.1400 | 7.000 | 3.500 |
| 1.90 | 0.1453 | 7.265 | 3.632 |
| 1.95 | 0.1500 | 7.500 | 3.750 |
| 2.00 | 0.1556 | 7.780 | 3.890 |
| 2.05 | 0.1603 | 8.015 | 4.008 |
| 2.10 | 0.1653 | 8.265 | 4.132 |
| 2.15 | 0.1707 | 8.035 | 4.268 |
| 2.20 | 0.1760 | 8.800 | 4.400 |
| 2.25 | 0.1817 | 9.085 | 4.542 |
| 2.30 | 0.1873 | 9.365 | 4.632 |
| 2.35 | 0.1933 | 9.665 | 4.832 |
| 2.40 | 0.1993 | 9.965 | 4.932 |
| 2.45 | 0.2053 | 10.265 | 5.182 |
| 2.50 | 0.2113 | 10.565 | 5.232 |
Приложение 4
Таблица 7
