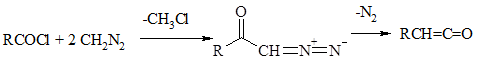Получение диазосоединений алифатического ряда
 |
Различия между алифатическими и ароматическими диазосоединениями выражены как в отношении свойств, так и строения. У алифатических диазосоединений формы, аналогичные солям диазония, отсутствуют.
Из двух классических формул диазометана только линейная соответствует измерениям её физических констант. Однако в её классической форме она не может быть принята электронной теорией. Поэтому строение диазометана изображается предельными структурами, как, например, Iа и Iб или II.
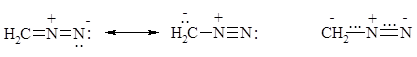 |
Ia Iб II
При обработке простых алифатических первичных аминов, например метиламина CH3NH2 азотистой кислотой диазосоединения не получаются даже, если работают при температуре -80°С. Непосредственно продиазотировать можно только те алифатические амины, в которых группа NH2 связана с атомом углерода, несущим кроме водорода карбэтоксигруппу
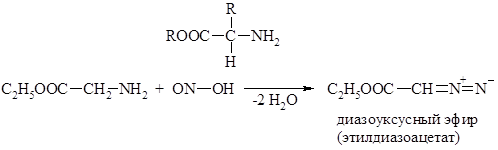 |
или карбонильную группу С = О.
К числу подобных веществ относятся эфиры a-аминокислот.
Простые диазоалканы, которые не могут быть получены непосредственным диазотированием, получают из алкилуретанов или алкилмочевин.
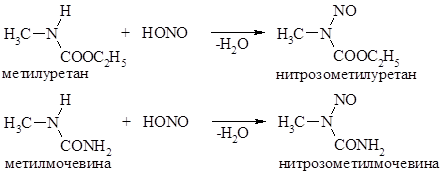 |
Нитрозоалкилуретан и нитрозометилмочевина превращаются в результате гидролиза концентрированным едким кали на холоду в диазоалкан, в данном случае в диазометан. Крайне неустойчивая промежуточно образующаяся кислота декарбоксилируется, а затем отщепляет воду.
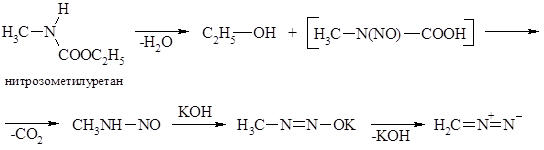 |
Промежуточные продукты, написанные в квадратных скобках, не могут быть выделены. Метилдиазотат калия можно выделить, работая осторожно на холоду. Он самопроизвольно превращается в диазометан.
N-метилтолуолсульфамид даёт при нитрозировании устойчивое N-нит-розосоединение CH3C6H4SO2-N(CH3)NO, сохраняющееся без разложения. При обработке концентрированным раствором КОН выделяется диазометан, который экстрагируют эфиром, охлаждённым до 0°С.
Специальный метод получения диазометана состоит в обработке смеси хлороформа и гидразина конц. КОН.
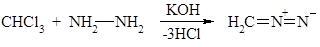 |
Диазометан представляет собой очень токсичный газ жёлтого цвета
(т. кип. -24°С). Эфирный раствор диазометана менее опасен в обращении при 20°С, чем чистый газ, который при этой температуре взрывается на воздухе. Он разлагается медленно и может храниться при температуре 0°С несколько дней.
Реакции диазометана
Циклоприсоединение.
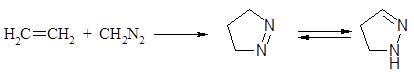 |
Диазометан происоединяется к олефинам, образуя пиразолины по схеме 1,3 – диполярного [3+2] циклоприсоединения (см. граничные структуры диазометана):
Другое направление этой реакции приводит к образованию производных циклопропана (циклопропанирование) через стадию образования чрезвычайно реакционноспособного соединения двухвалентного углерода – карбена, обладающего двумя неспаренными электронами.
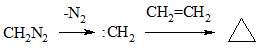 |
К этой же группе процессов можно отнести взаимодействие диазометана с кетеном протекает с образованием циклобутанона:
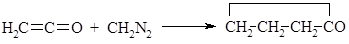 |
Реакции внедрения.
Кроме циклоприсоединения, карбены, в том числе генерированные из диазометана, могут вступать в реакции внедрения по различным связям. Широко применяется открытая Пехманом реакция, который показал, что диазометан является эффективным реагентом для метилирования соединений, содержащих подвижный атом водорода – карбоновых кислот, фенолов, минеральных и сульфокислоткислот.
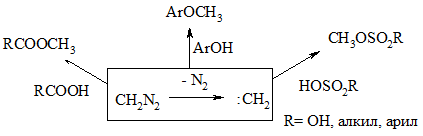 |
Нейтральные спирты индифферентны в этих реакциях, что позволяет предположить возможное каталитическое действие протона кислых соединений (по типу реакции этерификации).
Метилирование спиртов с образованием простых метиловых эфиров проводят в присутствие трифторида бора (или его комплекса с диэтиловым эфиром):
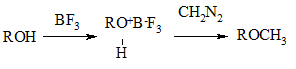
Хлорангидриды карбоновых кислот с диазометаном дают диазокетоны, которые при разложении превращаются в кетены – ценные высокореакционноспособные реагенты для органического синтеза.