Физические свойства алкенов
Физические свойства алкенов, по существу, такие же, как и свойства алканов. Они нерастворимы в воде, но хорошо растворимы в неполярных растворителях, таких как бензол, эфир, хлороформ или лигроин. Их плотность ниже плотности воды. Алкены с разветвленной цепью кипят при более низкой температуре, чем линейные соединения с тем же числом углеродных атомов.
Большинство алкенов неполярны, только некоторые олефины вследствие определенной геометрии молекулы имеют небольшие дипольные моменты.
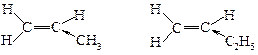
| μ = 0,35D | μ = 0,37 D |
Связь алкильной группы с атомом углерода двойной связи мало полярна, и ее направление указано на рисунке: алкильная группа подает электроны к углероду двойной связи.
Цис-бутен-2 с двумя метильными группами по одну сторону двойной связи и двумя атомами водорода по другую должен иметь небольшой дипольный момент. В транс-бутене-2 с каждой стороны двойной связи в молекуле находятся метильная группа и водород. В этом случае дипольный момент равен нулю, т.к. индукционные эффекты метильных групп направлены навстречу друг другу. Хотя дипольные моменты непосредственно не были измерены, небольшое различие в полярности находит отражение в более высокой температуре кипения цис-изомера.

| цис-изомер, т. кип. 4 ºС | транс-изомер μ=0; т. кип. 1 ºС |
Цис-изомер менее симметричен, и поэтому его упаковка в кристаллической решетке менее плотная, что обуславливает, как правило, более низкую температуру кипения данного изомера.
Различия в полярности и, следовательно, различия в температурах плавления и кипения больше для алкенов с заместителями, электроотрицательность которых сильно отличается от электроотрицательности углерода. Это может быть проиллюстрировано следующими примерами:
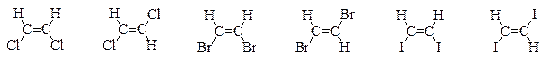
| Конфигурация | цис- | транс- | цис- | транс- | цис- | транс- |
| m (D) | 1,85 | 1,35 | 0,75 | |||
| т. пл. (°С) | -80 | -50 | -53 | -6 | -14 | -72 |
| т. кип. (°С) |
Связь между конфигурацией и температурами кипения и плавления является эмпирическим правилом, из которого имеется много исключений. В то же время измерение дипольных моментов часто позволяет приписать цис- или транс-строение определенному изомеру.
8.2.1. Спектроскопия алкенов
Алкены легко обнаружить с помощью спектральных методов.
· В УФ-спектрах алкены проявляют полосу поглощения соответствующую p→p*-переходу с максимумом при 180-205 нм.
· В ИК-спектрах валентные колебания νС=С проявляются в виде полосы 1640-1680 см-1, а деформационные колебания dС-Н – в диапазоне 790-990 см-1. Кроме того, цис- и транс-изомерам отвечают деформационные колебания: 650-750 см-1 для цис- и 960-980 см-1 для транс-конфигурации.
· В масс-спектрах алкенов отмечают характерные интенсивные пики молекулярных ионов, а также группу пиков с m/z 41(C3H5), 55; 69; 83 и т.д., образующихся в результате аллильного расщепления. К сожалению, двойная связь под электронным ударом мигрирует, поэтому масс-спектрометрию нельзя использовать для определения места положения двойной связи в алкенах.
· В спектрах ПМР протоны у двойной связи имеют химический сдвиг около 4,5-6,5 м.д. – т.е. они значительно сдвинуты в более слабое поле, чем протоны у насыщенных атомов углерода. Примеры значений химических сдвигов протонов для некоторых олефинов:
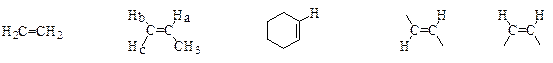
| d 5,33 | d 5,70 (a), 4,88 м.д. (b), 4,96 (с) | d 5,57 м.д. | Jвиц 12-18 Гц Jвиц 6-12 Гц |
Геометрические изомеры существенно различаются по вицинальным константам спин-спинового взаимодействия, что позволяет их интерпретировать.
