Факторы, влияющие на состояние равновесия
Принцип Ле-Шателье
На положение равновесия влияют: температура, давление, концентрация реагирующих веществ, инертный разбавитель. Качественно влияние изменения внешних условий на положение равновесия можно определить, пользуясь принципом Ле-Шателье:
если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-нибудь из условий, определяющих положение равновесия, то в системе усилится то направление процесса, течение которого ослабляет влияние произведенного воздействия, и положение равновесия сместится в том же направлении.
Например, рассмотрим реакцию синтеза аммиака в смеси идеальных газов:
N2 + 3H2 <==> 2NH3 – DrH°
Если повысить температуру, то равновесие сдвинется справа налево, так как обратная реакция протекает с поглощением тепла, что вызовет снижение температуры, т.е. ослабление внешнего воздействия.
Если увеличим давление, то равновесие сдвинется слева направо, так как эта реакция протекает с уменьшением объема, что вызовет снижение давления, ослабление внешнего воздействия.
Для количественной оценки состояния равновесия используют значения констант равновесия, равновесных концентраций с*i(или p*i) и равновесных степеней превращения х*.
Влияние температуры. Уравнение Вант-Гоффа
Численные значения КС и КP не зависят ни от концентрации реагентов и их соотношений, наличия или отсутствия примесей или разбавителей, ни от давления (если газы идеальные, а давление не очень велико). Константы химического равновесия зависят лишь от природы реагентов и температуры.
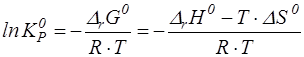 (4)
(4)
Для определения влияния температуры продифференцируем уравнение (4) по температуре и определим знак производной.
Это уравнение изобары Вант-Гоффа.
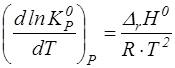 (5)
(5)
где: 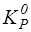 – стандартная константа равновесия;
– стандартная константа равновесия;
DrH° – изменение энтальпии при стандартных условиях (тепловой эффект реакции).
Из уравнения (5) следует, что влияние температуры на состояние равновесия определяется знаком теплового эффекта реакции:
- при DrH°> 0 (эндотермическая реакция) 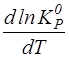 > 0 и
> 0 и 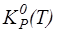 – возрастающая функция;
– возрастающая функция;
- при DrH°< 0 (экзотермическая реакция) 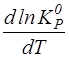 < 0 и
< 0 и 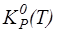 – убывающая функция.
– убывающая функция.
Зависимости равновесной степени превращения х* от температуры для экзо- и эндотермических реакций представлены на рис.1,а.
Если численные значения констант равновесия зависят только от природы реагентов и температуры, то на равновесные составы, степени превращения и выходы продуктов влияет не только температура, но и давление, концентрация исходных веществ, наличие примесей, разбавителей.
