Реакции обнаружения анионов первой группы
Групповым реагентом на анионы первой аналитической группы является, как было указано выше, водный раствор хлорида бария ВаС12, с которым анионы данной группы образуют осадки соответствующих бариевых солей, малорастворимые в нейтральных или слабо щелочных водных растворах. Поэтому реакции с групповым реагентом и проводят в нейтральной или слабо щелочной среде. Осадки бариевых солей рассматриваемых анионов растворяются в минеральных кислотах, за исключением сульфата бария BaS04.
Карбонат ВаС03, тетраборат ВаВ407, ортофосфат, Ва3(Р04)2 и арсенат Ba3(As04)2 растворимы и в уксусной кислоте.
Катионы серебра Ag+ также дают осадки солей серебра с анионами первой группы, за исключением фторид-аниона F-, поскольку фторид серебра AgF растворим в воде. Эти осадки растворяются в азотнокислом растворе, в отличие от солей серебра анионов второй аналитической группы. Соли свинца анионов первой группы также нерастворимы в воде, за исключением тетрабората и периодата.
Анионы первой аналитической группы в водных растворах бесцветны. Первая группа включает как анионы-окислители (As04, иногда также СrO42-, Сг2O72-), так и восстановители (AsO33-,S2O32-, SO32-, С2О42-). Под действием минеральных кислот анионы «летучих» кислот (СО32-, SO32- и S2O32-) разрушаются с выделением газообразных С02 или S02.
Аналитические реакции сульфат-иона S042-.
Сульфат-ион - анион сильной двухосновной серной кислоты H2S04 (рК2 = 1,94). В водных растворах бесцветен, практически не гидролизуется, обладает окислительными свойствами, которые, однако, в разбавленных растворах обычно не реализуются. Сульфат-ион как лиганд образует сравнительно малостойкие сульфатные комплексы металлов.
Сульфаты аммония и многих металлов хорошо растворяются в воде. Сульфата кальция, стронция, бария, свинца(II) малорастворимы в воде, что широко используется в химическом анализе.
Реакция с катионами бария (фармакопейная). Сульфат-ионы при взаимодействии с катионами бария Ва2+ образуют белый мелкокристаллический осадок сульфата бария BaS04:
Ba2++S02- ->BaS04
Осадок не растворяется в минеральных кислотах, за исключением концентрированной H2S04, в которой он частично растворим с образованием Ba(HS04)2:
BaS04 +H2S04 -> Ba(HS04)2
Если в растворе присутствует перманганат калия КМп04, то осадок сульфата бария окрашивается в фиолетово-красный цвет за счет адсорбции перманганат-ионов Мп04- на осадке.
Методика. В пробирку вносят 3-4 капли раствора сульфата натрия Na2S04 (или другого растворимого сульфата), прибавляют каплю разбавленного раствора НС1 и 2-3 капли раствора ВаС12. Выпадает белый осадок сульфата бария.
Реакция с катионами свинца. Сульфат-ион дает с катионами свинца РЬ2+ белый кристаллический осадок сульфата свинца PbS04:
Pb2++S042- =PbS04
Осадок частично растворяется в минеральных кислотах; растворяется в щелочах и в водных растворах ацетатов натрия CH3COONa или аммония CH3COONH4,с образованием комплексных соединений.
Растворение в щелочах:
PbS04 + 4NaOH = Na2[Pb(OH)4] + Na2S04
Комплексам, образующимся при растворении сульфата свинца в растворах ацетатов натрия и аммония, различные исследователи приписывают неодинаковый состав.
Методика. В пробирку вносят 3-4 капли раствора сульфата натрия и прибавляют 2—3 капли раствора нитрата свинца Pb(N03)2. Выпадает белый осадок сульфата свинца.
Реакция с родизонатом бария. Сульфат-ионы при взаимодействии с красным родизонатом бария разрушают его с образованием сульфата бария, вследствие чего красный родизонат бария обесцвечивается:
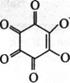 Ва2+ + SO42- = BaS04 +
Ва2+ + SO42- = BaS04 + 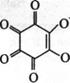
родизонат бария родизонат-анион — остаток
родизоновой кислоты H2C6H6
Реакция высокочувствительна: предел обнаружения 5 мкг. Реакцию обычно проводят капельным методом на фильтровальной бумаге.
Методика. На листок фильтровальной бумаги наносят каплю раствора хлорида бария ВаС12 и 1 каплю раствора родизоната натрия Na2C606 или родизоновой кислоты Н2С606. На бумаге возникает красное пятно родизоната бария. На это пятно наносят 1-2 капли раствора, содержащего сульфат-ионы (разбавленной серной кислота или растворимых сульфатов). Пятно обесцвечивается.
Некоторые другие реакции сульфат-ионов. Сульфат-ион открывают также реакциями с некоторыми органическими реагентами - сульфанозо III и солями бария, с карбонатом бария и фенолфталеином в нейтральной среде и т. д.
Аналитические реакции сульфит-иона SO32-.
Сульфит-ион SO32- и гидросульфит-ион HSO3- - анионы двухосновной нестабильной в водных растворах сернистой кислоты H2S03, которая при ионизации по первой стадии является кислотой средней силы (рК1 = 1,85), а по второй - очень слабой (рК2 = 7,20). В водных растворах сульфит-ионы бесцветны, подвергаются гидролизу, являются сильными восстановителями (уже в водных растворах они медленно окисляются кислородом воздуха до сульфатов). Однако некоторые сильные восстановители, например, металлический цинк в кислой среде, могут восстанавливать сульфиты до сероводорода H2S. Сульфит-ион обладает довольно эффективными комплексообразующими свойствами как лиганд.
Средние сульфиты натрия и калия хорошо растворяются в воде, средние сульфиты других металлов, как правило, малорастворимы в воде.
При действии кислот на сульфиты они разлагаются.
Реакция с хлоридом бария (фармакопейная). Сульфит-ионы при взаимодействии с катионами бария образуют белый кристаллический осадок сульфита бария BaS03:
Ba2++S032- = BaS03
Осадок растворяется в разбавленных НСI и HN03 с выделением газообразного диоксида серы S02, например:
BaS03 + 2НС1 -> S02 + ВаС12 + Н20
Аналогично протекает реакция сульфит-ионов и с хлоридом стронция SrCl2.
Методика. В пробирку вносят 2-3 капли раствора сульфита натрия Na2S03 и прибавляют 2-3 капли раствора ВаС12. Выпадает белый осадок сульфита бария.
К полученной смеси прибавляют по каплям раствор НС1. Осадок растворяется.
Реакция разложения сульфитов кислотами (фармакопейная). Все сульфиты разлагаются минеральными кислотами с выделением газообразного диоксида серы S02:
S032-+2H+ ->S02+H20
Выделяющийся диоксид серы обнаруживают по характерному запаху, а также по обесцвечиванию водного раствора иода или перманганата калия:
 S02 +12 + 2Н20 -> H2S04 + 2HI
S02 +12 + 2Н20 -> H2S04 + 2HI
5S02 + 2KMn04 + 2Н20 -> K2S04 + 2MnS04 + 2H2S04
Разложение сульфитов под действием кислот ускоряется при нагревании и при понижении рН среды.
Реакцию обычно проводят в приборе для обнаружения газов (рис. 16.1), состоящем из двух пробирок (7 и 2). Одна пробирка 1 снабжена пробкой с газоотводной изогнутой стеклянной трубкой, свободный конец которой погружают в раствор (для поглощения выделяющегося газа), которым заполняется другая пробирка-приемник 2. Методика.
Первый вариант. В пробирку 1 с пробкой вносят 6-8 капель раствора сульфита натрия, быстро прибавляют 6-8 капель разбавленной H2S04, сразу же закрывают пробирку пробкой с газоотводной трубкой, свободный конец которой погружают в пробирку-приемник 2, заполненную сильно разбавленным (светло-розового цвета) раствором перманганата калия, подкисленным серной кислотой. Розовый раствор в пробирке-приемнике обесцвечивается.
Второй вариант. В пробирку вносят 5-6 капель раствора сульфита натрия, прибавляют столько же капель раствора НС1 или H2S04 и встряхивают пробирку с раствором. Постепенно выделяется газообразный диоксид серы с характерным запахом.
Реакция с нитратом серебра. Сульфит-ионы дают с нитратом серебра AgN03 белый осадок сульфита серебра Ag2S03, растворимый при избытке сульфит-ионов с образованием растворимых комплексных
дисульфитоаргентат(I)-ионов [Ag(S203)2]3-:
2Ag++S032- ->Ag2S03
Ag2S03 +3S032- -> 2[Ag(S03)2]3-
При кипячении смеси белый осадок сульфита серебра темнеет за счет выделения оксида серебра Ag20:
Ag2S03 -> Ag20 + S02
Методика. В пробирку вносят 2-3 капли раствора сульфита натрия и по каплям прибавляют раствор нитрата серебра до выпадения белого осадка сульфита серебра. К образовавшейся смеси по каплям при перемешивании прибавляют раствор сульфита натрия до растворения осадка.
В другой пробирке аналогично получают белый осадок сульфита серебра и кипятят смесь осадка с раствором. Осадок постепенно становится бурым.
Реакция с перманганатом калия. Сульфит-ион при реакции с пер-манганатом калия КМn04 в кислой среде окисляется до сульфат-ионов:
5S032- +2МnО4- +6Н+ = 2Mn2+ +5S042- +3Н20
При этом розовый раствор перманганата калия обесцвечивается.
В нейтральной среде сульфит-ион при реакции с перманганат-ионом также окисляется до сульфат-иона. Одновременно образуется темный хлопьевидный осадок МпО(ОН)2:
3S032- + 2МnО4- + 3Н20 -> 2МnО(ОН)2 + 3S042- + 20Н-
Методика. В каждую из двух пробирок вносят по 2-3 капли раствора сульфита натрия.
В одну пробирку прибавляют 2-3 капли раствора H2S04 и по каплям - сильно разбавленный (до светло-розовой окраски) раствор перманганата калия. Раствор обесцвечивается.
В другую пробирку добавляют по каплям такой же раствор перманганата калия. Выпадает темный хлопьевидный осадок МnО(ОН)2.
Реакция с раствором иода (фармакопейная). Сульфит-ионы в нейтральных или слабо кислых растворах окисляются иодом до сульфат-ионов. При этом желтый раствор иода обесцвечивается вследствие восстановления иода до иодид-ионов:
SO32- +12 + Н20 = SO42- + 2I- + 2Н+
Аналогично протекает реакция сульфит-иона с бромной водой.
Методика.
а) В пробирку вносят 2-3 капли раствора сульфита натрия, прибав-
ляют по каплям раствор уксусной кислоты до нейтральной реакции (по
лакмусовой бумажке), затем также по каплям добавляют разбавленный
раствор иода (бледно-желтого цвета), который обесцвечивается.
б) В пробирку вносят 2-3 капли раствора сульфита натрия и добав-
ляют 2-3 капли раствора иода, который обесцвечивается.
Реакция восстановления сульфит-иона металлическим цинком в кислой среде. Сульфит-ион восстанавливается металлическим цинком в кислой среде до сероводорода H2S. Реакцию можно описать схемой:
S032- +2H+ = S02+H20
S02 +3Zn + 6H+ = H2S+3Zn2+ +2H20
Выделяющийся газообразный сероводород можно обнаружить по почернению фильтровальной бумаги, смоченной раствором соли свинца(II), вследствие образования черного сульфида свинца PbS:
H2S + Pb2+ = PbS+2H+
Методика. В пробирку вносят 3-4 капли раствора сульфита натрия, прибавляют 2 капли раствора НС1 и немного металлического цинка. В верхнюю часть пробирки помещают полоску фильтровальной бумаги, смоченной раствором соли свинца. Бумага чернеет.
Другие реакции сульфит-иона. Для открытия сульфит-иона в растворах используют также реакции с красителями - фуксином, малахитовым зеленым (обесцвечивание красителя), с дихроматом калия (раствор обесцвечивается), с нитропруссидом натрия Na2[Fe(CN)5NO] (образуются продукты реакции розово-красного цвета), с ацетатом меди(Н) и уксуснокислым раствором бензидина на фильтровальной бумаге (возникает темное пятно) и др.
Аналитические реакции тиосульфат-иона S2O32-
Тиосульфат-ион S2O32- - анион неустойчивой двухосновной тиосерной кислоты H2S203 средней силы (рК1 = 0,60, рК2 = 1,72), которая в водных растворах разлагается с выделением элементной серы:
H2S203 = S + S02 + H20
В водных растворах тиосульфат-ион бесцветен, практически не гидроли-зуется, является сильным восстановителем и достаточно эффективным лигандом-комплексообразователем.
Тиосульфаты щелочных металлов, стронция, цинка, кадмия, марган-ца(II), железа(II), кобальта(II), никеля(II) растворимы в воде. Тиосульфаты других металлов малорастворимы в воде.
Реакция с хлоридом бария. Тиосульфат-ион при взаимодействии с катионами бария образует белый мелкокристаллический осадок тиосульфата бария:
Ba2++S2032- = BaS203
осадок растворяется в кислотах с разложением:
BaS203 +2h+ = Ba2++S+S02+h20
Методика. В пробирку вносят 2-3 капли раствора тиосульфата натрия Na2S203 и прибавляют 2-3 капли раствора хлорида бария. Выпадает белый осадок тиосульфата бария.
Осадок образуется медленно. Для ускорения выделения осадка можно потереть внутреннюю стенку пробирки стеклянной палочкой.
Реакция разложения тиосульфатов кислотами (фармакопейная). При действии минеральных кислот на тиосульфаты вначале образуется нестабильная тиосерная (серноватистая) кислота H2S203, быстро разлагающаяся с выделением газообразного диоксида серы S02 и элементной серы S, которая вызывает помутнение раствора:
S2032-+2h+ = H2S203
H2S2O3 = S+SO2+Н20
Выделяющийся газообразный диоксид серы обнаруживают либо по характерному запаху, либо по обесцвечиванию им растворов перманганата калия или иода.
Методика
а) В пробирку вносят 3-4 капли раствора тиосульфата натрия и
столько же капель разбавленного раствора хлороводородной кислоты
НС1. Раствор мутнеет вследствие выделения элементной серы и ощуща-
ется характерный запах диоксида серы.
б) Реакцию проводят с использованием прибора для обнаружения га-
зов, описанного выше (см. рис. 16.1).
В пробирку 1 вносят 6-8 капель раствора тиосульфата натрия и 6-8 капель разбавленного раствора НС1. Пробирку сразу же закрывают пробкой с газоотводной трубкой, свободный конец которой погружают в сильно разбавленный раствор КМn04 (бледно-розового цвета) или в сильно разбавленный раствор иода (бледно-желтого цвета), находящийся в пробирке-приемнике 2. Раствор в первой пробирке мутнеет вследствие выделения элементной серы. Раствор в пробирке-приемнике обесцвечивается.
Реакция с иодом. Тиосульфат-ион обесцвечивает нейтральные или слабо щелочные растворы иода, восстанавливая иод до иодид-ионов I- с одновременным образованием тетратионат-иона S4062-:
2S2032- + I2 = S4062- + 2I-
Эта реакция имеет большое значение в количественном титриметри-ческом анализе.
Методика. В пробирку вносят 3-4 капли разбавленного раствора иода, имеющего желтую окраску, и прибавляют по каплям раствор тиосульфата натрия до обесцвечивания раствора иода.
Реакция с нитратом серебра (фармакопейная). Тиосульфат-ион с катионами серебра Ag+ образует белый осадок тиосульфата серебра Ag2S203:
2Ag++S2032- = Ag2S203
Осадок тиосульфата серебра быстро разлагается до черного сульфида серебра(1) Ag2S. Цвет осадка последовательно изменяется на желтый, бурый и под конец - на черный. Реакция протекает по схеме:
Ag2S203 + Н20 = Ag2S + H2S04
При избытке тиосульфат-ионов осадок тиосульфата серебра растворяется с образованием комплексных дитиосульфатоаргентат(1)-ионов [Ag(S20)2]3-:
Ag2S203 + 3S2032- = 2[Ag(S203)2]3-
Методика. В пробирку вносят 2-3 капли раствора тиосульфата натрия и прибавляют 2-3 капли раствора нитрата серебра AgN03. Выделяется белый осадок тиосульфата серебра, постепенно изменяющий окраску на буро-черную.
В другой пробирке аналогично получают белый осадок тиосульфата серебра и сразу же прибавляют к нему при перемешивании избыток раствора тиосульфата натрия до растворения осадка.
Реакция с сульфатом меди(II). Тиосульфат-ион при взаимодействии с катионами меди (II) Сu2+ образует черный осадок сульфида меди(I) Cu2S:
2Cu2+ + 3S2032- = Cu2S203 + S4062-
Cu2S203 + H20 = Cu2S + H2S04
Методика. В пробирку вносят 2-3 капли раствора тиосульфата натрия, прибавляют 2-3 капли раствора сульфата меди(II) CuS04 и осторожно нагревают пробирку. Выпадает черный осадок сульфата меди(I).
Некоторые другие реакции тиосульфат-иона. Тиосульфат-ион легко окисляется различными окислителями (Н202, КМn04, К2Сг207 и др.); при реакциях с хлоридом железа(III) FeCl3, образует тиосульфатный комплекс [Fe(S203)2]- фиолетового цвета (постепенно разлагающийся в водном растворе), с солями ртути(II) - черный осадок сульфида ртути(II) HgS и т. д.
Аналитические реакции оксалат-иона С2042-
Оксалат-ион С2042- — анион двухосновной щавелевой кислоты Н2С204 средней силы (рК1 = 1,25; рК2 = 4,27), сравнительно хорошо растворимой в воде. Оксалат-ион в водных растворах бесцветен, частично гидролизуется, сильный восстановитель, эффективный лиганд — образует устойчивые оксалатные комплексы с катионами многих металлов.
Оксалаты щелочных металлов, магния и аммония растворяются в воде. Оксалаты других катионов, как правило, малорастворимы в воде.
Реакция с хлоридом бария. Соли бария осаждают из водных растворов оксалат-ион в виде белого осадка оксалата бария ВаС204:
Ва2++С2O42- = ВаС204
Осадок оксалата бария растворяется в минеральных кислотах, а при кипячении — ив уксусной кислоте.
Методика. В каждую из двух пробирок вносят по 2—3 капли раствора оксалата аммония (NH4)2C204 и прибавляют по 2—3 капли раствора бария хлорида. В обеих пробирках выпадает белый осадок оксалата бария.
В одну пробирку прибавляют по каплям при перемешивании раствор НСl до полного растворения осадка.
В другую пробирку прибавляют 6—7 капель раствора уксусной кислоты и осторожно нагревают смесь до кипения. При кипячении смеси осадок постепенно растворяется.
Аналогично протекает реакция оксалат-ионов с катионами кальция (фармакопейная) с образованием белого осадка оксалата кальция СаС204, который растворяется в минеральных кислотах, но не растворяется в уксусной кислоте.
Реакция с нитратом серебра. Оксалат-ионы при взаимодействии с катионами серебра Ag+ образуют белый творожистый осадок оксалата серебра Ag2C204:
2Ag++C2O42- = Ag2C204
Осадок оксалата серебра растворяется в азотной кислоте, в концентрированном растворе аммиака. Действие раствора НС1 на оксалат серебра приводит к образованию хлорида серебра:
Ag2C204+2HCl = 2AgCl + H2C204
Методика В каждую из трех пробирок вносят по 2—3 капли раствора оксалата аммония (NH4)2C204 и прибавляют по 2—3 капли раствора AgN03. В каждой пробирке выпадает белый осадок оксалата серебра.
В одну пробирку прибавляют по каплям при перемешивании раствор HN03 до растворения осадка.
В другую пробирку также по каплям при перемешивании добавляют концентрированный раствор аммиака до растворения осадка.
В третью пробирку прибавляют 4—5 капель раствора НС1; в пробирке остается белый осадок хлорида серебра.
Реакция с перманганатом калия. Оксалат-ионы при взаимодействии с перманганатом калия КМnO4 в кислой среде при нагревании окисляются с выделением газообразного диоксида углерода С02; раствор перманганата калия при этом обесцвечивается вследствие восстановления марганца(VII) до марганца(II):
5С2O42-+ 2МnО4- + 16Н+ = 10СО2 + 2Мn2+ +8Н20
При проведении этой реакции можно использовать прибор для обнаружения газов, аналогичный тому, который применяется при изучении реакции разложения сульфитов кислотами (см. рис. 16.1).
Методика.
а) В пробирку вносят 2—3 капли раствора оксалата аммония,
прибавляют 3—5 капель раствора серной кислоты, нагревают смесь до
~70—80°С (не выше) и медленно, по каплям прибавляют разбавленный
раствор перманганата калия. Последний обесцвечивается; наблюдается
выделение пузырьков газа — диоксида углерода.
б) В пробирку 1 (см. рис. 16.1) вносят 6—8 капель раствора оксалата
натрия Na2C204 (или другого растворимого оксалата), прибавляют столь-
ко же капель раствора H2S04 и 5—6 капель разбавленного раствора
КМnO4. Раствор в пробирке 1 окрашивается в бледно-розовый цвет
перманганат-ионов.
Пробирку 1 закрывают пробкой с газоотводной трубкой, погружая ее свободный конец в раствор баритовой воды (насыщенный раствор гидро-ксида бария Ва(ОН)2) или известковой воды (насыщенный раствор гид-роксида кальция Са(ОН)2), находящийся в другой пробирке-приемнике 2.
Осторожно нагревают раствор в первой пробирке до ~70—80 °С. При нагревании раствор обесцвечивается и из него выделяются пузырьки газа (С02), который через газоотводную трубку попадает в пробирку-приемник 2 и вызывает помутнение известковой воды вследствие образования малорастворимого карбоната кальция СаС03:
Са2+ + 20Н- + С02 = СаС03 + Н20
Некоторые другие реакции оксалат-ионов. Оксалат-ионы дают с α-нафтиламином и n-толуидином в присутствии ацетата меди(II) осадки комплексов соответственно желтого и зеленого цвета. При проведении капельной реакции на фильтровальной бумаге с уксуснокислым раствором бензидина и ацетатом меди оксалат-ионы образуют комплекс коричневого цвета (на фильтровальной бумаге наблюдается возникновение коричневого пятна).
Аналитические реакции карбонат-иона СО32-
Карбонаты — соли нестабильной очень слабой угольной кислоты Н2С03 (pK1= 6,35, рК2 = 10,32), которая в свободном состоянии в водных растворах неустойчива и разлагается с выделением диоксида углерода С02:
Н2СО3 = СО2+Н2О
Угольная кислота образует два ряда солей: средние карбонаты (или просто карбонаты), содержащие анион СО3 2-, и гидрокарбонаты, содержащие анион HCO3- . Карбонаты аммония, натрия, калия, рубидия, цезия растворимы в воде. Карбонат лития в воде малорастворим. Карбонаты других металлов, как правило, также малорастворимы в воде. Гидрокарбонаты растворяются в воде.
Карбонат-ионы в водных растворах бесцветны, не обладают ни окислительными, ни восстановительными свойствами, способны как ли-ганды к образованию различных по устойчивости карбонатных комплексов с катионами ряда металлов.
Карбонат-ионы в водных растворах подвергаются гидролизу. Водные растворы гидрокарбонатов щелочных металлов не окрашиваются при прибавлении к ним капли раствора фенолфталеина, что позволяет отличать растворы карбонатов от растворов гидрокарбонатов (фармакопейный тест).
Реакция с хлоридом бария. Карбонат-ион при взаимодействии с катионами бария образует белый мелкокристаллический осадок карбоната бария ВаС03:
Ва2++СО32- = ВаС03
Осадок растворяется в минеральных кислотах (в растворе H2S04 образуется белый осадок BaS04) и в уксусной кислоте.
Аналогичные осадки карбонатов дают катионы кальция (СаС03) и стронция (SrC03).
Методика. В пробирку вносят 2—3 капли раствора карбоната натрия Na2C03 и прибавляют 2—3 капли раствора хлорида бария. Выпадает белый осадок карбоната бария.
К осадку медленно, по каплям прибавляют раствор НС1 до полного растворения осадка.
Реакция с сульфатом магния (фармакопейная). Карбонат-ион СО32- с сульфатом магния образует белый осадок карбоната магния MgC03:
Mg2++C032- = MgC03
Осадок карбоната магния растворяется в кислотах.
Гидрокарбонат-ион НС03 образует с сульфатом магния осадок MgC03 только при кипячении:
Mg2+ + 2НСО3- = MgC03 + С02 + Н2О
Методика. В пробирку вносят 3—5 капель раствора карбоната натрия Na2C03 и прибавляют столько же капель насыщенного раствора сульфата магния MgS04. Выпадает белый осадок карбоната магния.
Реакция с минеральными кислотами (фармакопейная). Карбонат-ионы и гидрокарбонат-ионы при взаимодействии с кислотами образуют слабую нестабильную угольную кислоту, быстро разлагающуюся в кислой среде с выделением газообразного диоксида углерода СO2:
СО32- + 2Н30+ = Н2С03 + 2Н2O
HCO- + Н3О+ = Н2СО3 + Н2O
Н2С03 ->С02+Н20
Выделяющийся газообразный диоксид углерода обнаруживают по помутнению баритовой или известковой воды в приборе для обнаружения газов (см. рис. 16.1).
Методика. В пробирку 1 вносят 8—10 капель раствора карбоната натрия Na2C03 или гидрокарбоната натрия NaHC03, прибавляют столько же капель раствора НС1 или H2S04 и сразу же закрывают пробирку 1 пробкой с газоотводной трубкой, свободный конец которой быстро погружают в баритовую или известковую воду, находящуюся в пробирке-приемнике 2. В первой пробирке наблюдается выделение пузырьков газа (С02), в пробирке-приемнике — помутнение раствора.
Реакция с гексацианоферратом(II) уранила. Карбонат-ионы обесцвечивают коричневый раствор гексацианоферрата(II) уранила (U02)2[Fe(CN)6], разлагая его на бесцветный карбонат уранила U02C03 (или
на карбонатные комплексы уранила) и ферроцианид-ионы [Fe(CN)6]4-, которые в малых концентрациях не придают раствору интенсивной окраски. Реакция протекает по схеме:
2С032- + (U02)2[Fe(CN)6] -> 2U02C03 +[Fe(CN)6]4-
Коричневый раствор тексацианоферрата(П) уранила получают, смешивая раствор ацетата уранила (CH3COO)2U02 с раствором гексацианоферрата(II) калия:
2(CH3COO)2U02+K4[Fe(CN)6] = (U02)2[Fe(CN)6] + 4CH3COOK
Реакция — высокочувствительная: предел обнаружения равен 0,4 мкг.
Методика. В пробирку вносят 3—4 капли раствора ацетата уранила и прибавляют 2—3 капли раствора гексацианоферрата(II) калия. Раствор окрашивается в коричневый цвет вследствие образования гексациано-феррата(II) уранила. К полученному раствору прибавляют по каплям раствор Na2C03 или К2С03 при перемешивании до исчезновения коричневой окраски.
Раздельное открытие карбонат-ионов и гидрокарбонат-ионов реакциями с катионами кальция и с аммиаком. Если в растворе одновременно присутствуют карбонат-ионы СО32- и гидрокарбонат-ионы HCO3-, то каждый из этих анионов можно открыть раздельно. Для этого вначале к анализируемому раствору прибавляют избыток раствора хлорида кальция. При этом карбонат-анионы СО32- осаждаются в виде карбоната кальция СаС03:
СО2 +Са2+ = СаС03
Гидрокарбонат-анионы НС03 остаются в растворе, так как Са(НС03)2
растворим в воде.
Осадок СаС03 отделяют от раствора и к последнему прибавляют раствор аммиака. Гидрокарбонат-анионы с аммиаком и катионами кальция дают снова осадок карбоната кальция:
HCO3- + Са2+ +NH3 = СаС03 + NH4+
Методика. В пробирку вносят 6—8 капель раствора гидрокарбоната натрия NaHC03, одну каплю раствора карбоната натрия Na2C03 и прибавляют 4—5 капель раствора СаС12. Выпадает белый осадок карбоната кальция СаС03, который отделяют от раствора центрифугированием.
К центрифугату добавляют по каплям раствор аммиака до прекращения выделения белого осадка карбоната кальция.
Другие реакции карбонат-иона. Карбонат-ион вступает во многие реакции, однако лишь некоторые из них имеют аналитическое значение.
Карбонат-ионы при реакции с хлоридом железа(III) FeCl3 образуют бурый осадок гидрокарбоната железа(III) Fe(OH)C03, с нитратом серебра — белый осадок карбоната серебра Ag2C03, растворимый в HN03 и разлагающийся при кипячении в воде до темного осадка Ag20 и С02:
Ag2C03 ->Ag2O + CO2
