Опыт 5. Электролиз раствора сульфата меди
В электролизёр налить 0,5 М раствор сульфата меди (II). Опустить в оба колена электролизёра угольные электроды, присоединить их к источнику постоянного тока и пропускать ток в течение 5-10 мин. К раствору на анодном участке добавить раствор лакмуса. Отметить окраску раствора. Составить уравнения реакций, протекающих на электродах. Промыть электроды и электролизёр.
Опыт 6. Электролиз раствора сульфата натрия
В электролизёр налить 0,5 М раствор сульфата натрия, прибавить в оба колена сосуда по 3-4 капли раствора лакмуса и пропускать ток в течение 5-10 минут. Как изменится окраска раствора на катодном и анодном участках? Какие газы выделяются на электродах? Написать уравнения электродных процессов.
Лабораторная работа: Гальванический элемент
Цель работы: Определение ЭДС гальванических элементов и расчет работы, изменения свободной энергии Гиббса и константы равновесия реакций, протекающих в гальванических элементах.
Реактивы и лабораторное оборудование: Милливольтметр. U – образный электролитический мостик, заполненный насыщенным раствором хлорида калия. Химические стаканы. Пробирки. Пластинки меди, цинка, железа (можно проволоку). Растворы: сульфата меди (1М), сульфата цинка (1 М; 0,1 М; 0,01 М), сульфата железа (II) (1 М), хлорида олова (II), (1 М), хлорида кадмия (1 М), нитрата серебра (1 М).
Опыт 1. Сравнительная активность металлов
В пробирки налить по 1 мл растворов солей цинка, железа (II), кадмия, олова (II), меди (II), свинца (II) и серебра (I). Поочередно опускать в растворы полоски цинка, очищенные железные и медные проволоки. Какие металлы может вытеснять цинк, железо, медь? Заполнить таблицу, поставив «+» под каждым металлом, который вытесняется из раствора его соли цинком, железом, медью.
| Соли | Zn2+ | Fe2+ | Cd2+ | Sn2+ | Cu2+ | Ag+ | Pb2+ |
| Металл Zn | |||||||
| Металл Fe | |||||||
| Металл Cu |
Расположить испытуемые металлы по активности в ряд и сравнить их расположение с положением в ряду напряжений. Написать уравнения реакций. Для реакций взаимодействия железа с солями цинка (II) и меди (II) рассчитать DG и указать направленность процессов.
Опыт 2. Измерение ЭДС гальванического элемента и определение ∆G в окислительно-восстановительной реакции
В два стакана налить равные объемы 1 М растворов сульфата цинка и сульфата меди (II). Растворы соединить жидкостным мостиком, заполненным насыщенным раствором хлорида калия в смеси с агар-агаром. Пластинки меди и цинка опустить в растворы ZnSO4 и CuSO4 соответственно. Проволочки от меди и цинка присоединить к милливольтметру. Измерить ЭДС после установления стационарного значения напряжения по шкале прибора. Записать схему гальванического элемента, написать реакции, идущие на электродах, указать анод и катод. Указать направление перехода электронов во внешней цепи, а ионов - во внутренней. Рассчитать теоретическое значение ЭДС с учетом концентрации электролита и сравнить ее с измеренной. Рассчитать DG источника тока и сделать вывод о возможности его работы с термодинамической точки зрения.
Опыт 3. Исследование зависимости ЭДС гальванического элемента от концентрации соли
Работу проводят с медно-цинковым гальваническим элементом (см. опыт 2).
В стакан налить 20 мл 1 М раствора сульфата меди, концентрация которого в ходе измерений не изменяется. В остальные стаканы налить растворы сульфата цинка в порядке возрастания концентрации (0,01, 0,1 и 1 М). В раствор сульфата меди опустить медный электрод, цинковый электрод опустить в раствор сульфата цинка наименьшей концентрации. Полуэлементы соединить солевым мостиком и измерить ЭДС гальванического элемента с помощью милливольтметра.
Не отключая милливольтметр, перенести цинковый электрод в 0,1 М раствор сульфата цинка и снова измерить ЭДС, затем то же проделать с 1 М раствором ZnSO4.
Результаты измерений и рассчитанные значения записать в таблицу по форме:
| СCu, моль/л | СZn, моль/л | ∆Eэксп., В | ∆Gэксп., В | ∆Eтеор., В | ∆Gтеор., В | Погреш-ность, % |
| 0,1 0,01 |
В какой мере концентрация ионов металла в растворе влияет на значение электродного потенциала металла и, следовательно, на ЭДС гальванического элемента?
Лабораторная работа: Электролиз
Цель работы: Ознакомление с процессами, протекающими на растворимых и нерастворимых электродах при электролизе водных растворов электролитов.
Реактивы и лабораторное оборудование: Источник постоянного тока. Электролизеры. Электроды: угольные, медный, алюминиевый. Растворы: иодида калия (0,5 М), сульфата натрия (0,5 М), сульфата меди (2 М), серной кислоты (2 М). Индикатор: фенолфталеин
Опыт 1. Электролиз растворов солей с нерастворимым анодом
Опыт проводится в электролизере, представляющем собой U-образную стеклянную трубку с раствором электролита, в который погружено два электрода, один из которых подключен к положительному, другой – к отрицательному полюсам источника постоянного тока.
А. Электролиз раствора сульфата натрия
В электролизер налить 0,5 М раствор сульфата натрия. К раствору прибавить 1-2 капли фенолфталеина. Угольные электроды погрузить в электролизер, через выпрямитель соединить с электросетью и пропускать ток в течение 3-5 минут. Наблюдать изменение окраски раствора, а также выделение пузырьков газа на электродах. Написать уравнение электролиза.
Б. Электролиз раствора иодида калия
Опыт проводится аналогично предыдущему. Электроды угольные.
В электролизер налить 0,5 М раствор иодида калия, прибавить 1-2 капли фенолфталеина. Пропускать ток в течение 3-5 минут. Наблюдать, что происходит на электродах. Ответить на вопрос: почему в растворе у катода обнаруживается щелочная реакция? Написать суммарное уравнение электролиза.
Опыт 2. Электролиз растворов солей с растворимым анодом
А. Электролиз раствора сульфата меди (II)
В электролизер (U-образную трубку) налить 15-20 мл 2 М раствора сульфата меди (II) и подкислить 2 каплями 2 М раствора серной кислоты. Погрузить в раствор электроды (анод – небольшая медная полоска, катод – полоска алюминия). Электроды соединить через выпрямитель с электросетью. Наблюдать, что происходит с электродами. Написать схему электролиза.
Лабораторная работа: Коррозия металлов. Методы защиты
Цель работы: Изучение условий возникновения коррозионных микроэлементов, их моделей, а также влияние различных факторов на скорость электрохимической коррозии металлов. Ознакомление с наиболее важными методами защиты металлов от коррозии.
Реактивы и лабораторное оборудование: Наждачная бумага. Химические стаканы. Пробирки. Стеклянная палочка. Цинк (гранулированный). Алюминий (гранулированный). Свинец (гранулированный). Медная проволока. Полоска оцинкованного железа. Полоска луженого железа. Стальная пластинка. Бихромат калия (кристаллический). Цинковая пыль. Растворы: серной кислоты (2 М), сульфата меди (II) (0,5 М), гексацианоферрата (III) калия (0,1 М), хлорида меди (II) (0,5 М), соляной кислоты (10%), гидроксида натрия (20%)
Опыт 1. Образование микрогальванопар
В две пробирки налить по 10 капель 2 М раствора серной кислоты и внести примерно равные кусочки цинка. Наблюдать медленное выделение водорода в пробирках. В одну пробирку добавить 1-2 капли раствора сульфата меди. Обратить внимание: что происходит? Почему возросла скорость выделения водорода при добавлении раствора сульфата меди?
Опыт 2. Коррозия при контакте различных металлов
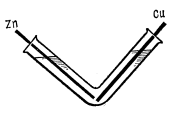 Стеклянную трубку, согнутую под углом, укрепить в штативе (см. рис. 1) и заполнить 0,01 н раствором серной кислоты. С противоположных сторон трубки вставить медную и цинковую проволочки, не допуская соприкосновения. Наблюдать выделение водорода на
Стеклянную трубку, согнутую под углом, укрепить в штативе (см. рис. 1) и заполнить 0,01 н раствором серной кислоты. С противоположных сторон трубки вставить медную и цинковую проволочки, не допуская соприкосновения. Наблюдать выделение водорода на
поверхности цинка. Ответить на вопрос: почему не Рис. 1. Схема опыта
выделяется водород на поверхности меди? Привести
медную проволоку в контакт с цинковой. При контакте водород начинает выделяться на меди. Ответить на вопрос: как влияет контакт с медью на коррозию цинка? Написать схему действия возникшей гальванопары.
Опыт 3. Электрохимическая коррозия оцинкованного и луженого железа
Две железные проволоки очистить наждачной бумагой. К одной из них прикрепить тонкую пластинку олова, к другой – цинка. Проволоки опустить в пробирки с водой, подкисленной несколькими каплями серной кислоты. В обе пробирки прилить по две капли гексацианоферрата (III) калия K3[Fe(CN)6] (при взаимодействии данной соли с ионами Fe2+ наблюдается образование синего осадка Fe3[Fe(CN)6]2). Указать, в какой пробирке синее окрашивание появляется раньше, и объяснить, чем это обусловлено. Составить схему коррозии оцинкованного и луженого железа.
Опыт 4. Разрушение оксидной пленки
Две гранулы алюминия опустить в пробирки с растворами солей хлорида меди (II) и сульфата меди (II). Наблюдать вытеснение меди в пробирке с раствором хлорида меди (II). Ответить на вопрос: какой газ выделяется? Написать уравнения происходящих процессов.
Обратить внимание: хлорид-ионы быстро разрушают защитную пленку алюминия; сульфат-ионы производят подобное действие значительно медленнее и лишь при большой концентрации данных ионов в растворе.
Опыт 5. Нанесение катодного покрытия на цинк
В пробирку внести 30 капель 10%-ного раствора соляной кислоты и гранулу цинка. После начала выделения водорода опустить несколько кристаллов бихромата калия. Выделение водорода прекращается, а поверхность покрывается хромом. Написать уравнения реакций, происходящих при этом.
Опыт 6. Нанесение анодного покрытия на медь
В пробирку внести 6 капель 20%-ного раствора гидроксида натрия, микрошпатель цинковой пыли и медную проволоку, предварительно зачищенную. Содержимое пробирки кипятить 2-3 мин. Наблюдать покрытие меди цинком. Написать уравнения происходящих реакций.
Контрольные вопросы и упражнения
Объясните возникновение скачка потенциала на границе раздела «металл– электролит».
Для чего служит гальванический элемент? Какой электрод называется катодом, какой анодом?
Пользуясь таблицей, определите, будет ли металлический кобальт растворяться в растворе сульфата цинка ?
Что такое электродный потенциал? На чём основан ряд напряжений?
Что такое электролиз? Чем отличаются электрохимические процессы, протекающие в электролизёре и гальванических элементах?
Написать уравнения электродных процессов электролиза разбавленных растворов: а) хлорида магния; б) сульфата меди; в) нитрата калия, протекающих на угольных электродах.
Составить схемы электролиза водного раствора хлорида цинка, если: а) анод цинковый; б) анод угольный.
Раствор содержит ионы Fe²⁺, Ag⁺, Bi³⁺, Pb²⁺ одинаковой концентрации. В какой последовательности эти ионы будут выделяться при электролизе, если напряжение достаточное для выделения любого металла?
Составьте схему электролиза расплава хлорида калия и рассчитайте объём хлора, выделившегося в процессе, если было взято вещество массой 149 г.
277. Составьте схему электролиза раствора хлорида калия и вычислите объём водорода, выделившегося при нормальных условиях в случае, когда растворено вещество количеством 2 моль.
278. Вычислите массу газа, выделившегося у анода при электролизе раствора серной кислоты, проводившегося 5 мин при силе тока равной 2 А.
279. Вычислите объём газа, выделившийся при электролизе раствора сульфата меди (II), если при этом образовалось 16 г меди на катоде.
280. При пропускании постоянного тока силой 6,4 А в течение 30 мин через расплав хлорида трёхвалентного металла на катоде выделилось 1,07 г металла. Определите состав соли, подвергшийся электролизу.
281. Напишите схему электролиза расплава хлорида натрия. Сколько молей хлора получится на аноде, если подвергнуть электролизу 1 моль хлорида натрия?
282. Вычислите время, необходимое для выделения железа массой 2,8 г из раствора сульфата железа (II) силой тока в 10 А.
283. Раствор хлорида никеля (II), содержащий соль массой 130 г, подвергался электролизу силой тока 5 А в течение 5,36 ч. Вычислите массу соли, оставшейся в растворе после электролиза.
284. Вычислите массу серебра, выделившуюся при пропускании через раствор нитрата серебра тока в 8 А в течение 15 мин.
285. Следующие пары металлов, находящиеся в тесном контакте, погружены в раствор серной кислоты. Укажите пару, где цинк не будет разрушаться: Zn/Ag, Zn/Cu, Zn/Al, Zn/Fe.
286. Какой из предложенных металлов: 1) Рb, 2) Сu, 3) Ni, 4)Na, 5) Li первым осадится на катоде при электролизе раствора смеси солей: Pb(NO3)2, Cu(NO3)2, Ni(NO3)2, NaNO3, LiNO3?
287. Следующие пары металлов, находящиеся в тесном контакте, погружены в раствор серной кислоты. Укажите пару, где железо не будет разрушаться: Fe/Cu, Fe/Ag, Fe/Zn, Fe/Au.
288. Имеются пары металлов (Fe/Cu, Fe/Ag, Fe/Sn, Fe/Al), погружённые в раствор соляной кислоты. В каком случае не будет протекать коррозия железа?
289. Вычислите ЭДС и определите направление тока во внешней цепи данного гальванического элемента Fe | Fe2+ || Ag+| Ag, учитывая, что концентрация ионов Fe2+ и Ag+ соответственно равна 0,1 моль/л и 0,01 моль/л.
290. Определить ЭДС гальванического элемента Ag | AgNO3 (0,001 М) || AgNO3 (0,1 М) |Ag. В каком направлении будут перемещаться электроны во внешней цепи при работе этого элемента?
291. Гальванический элемент состоит из металлического цинка, погружённого в 0,1 М раствор нитрата цинка, и металлического свинца, погружённого в 0,02 М
раствор нитрата свинца. Вычислить ЭДС элемента, написать уравнения
электродных процессов, составить схему элемента.
292. Составьте схему гальванического элемента, составленного из железа и кадмия, опущенных в растворы их солей с концентрациями ионов [Fe 2+] = 1 моль/л, а ионов кадмия [Cd 2+] = 0,0001 моль/л. Рассчитайте ЭДС гальванического элемента, напишите уравнения катодного и анодного процессов.
293. Составьте схему, напишите уравнения анодного и катодного процессов и рассчитайте ЭДС гальванического элемента, в котором один медный электрод находится в 0,0025 М растворе, а другой в 2 М растворе сульфата меди.
294. Какие продукты получаются при электролизе: а) расплава КI с инертным анодом: б) водного раствора КI с инертным анодом: в) водного раствора КI с никелевым анодом? Напишите уравнения анодного и катодного процессов и суммарное уравнение электролиза.
295. Алюминий находится в контакте с хромом. Напишите уравнения анодного и катодного процессов коррозии во влажном воздухе.
296. Цинк покрыт свинцом. Напишите уравнения коррозии во влажном воздухе при нарушении покрытия.
297. Алюминий склепан с медью. Какой из металлов будет коррозировать в кислоте, содержащей растворенный кислород? Напишите уравнения анодного и катодного процессов.
298. Свинец спаян с серебром и находится во влажном воздухе, насыщенном сероводородом. Напишите уравнения коррозии. Каков будет продукт коррозии?
299. Две алюминиевые пластинки склепаны одна с медью, другая со свинцом. В каком случае коррозия идет быстрее? Почему? Составьте уравнения электродных процессов в кислой среде.
300. Какое покрытие - цинковое или медное надежней защитит кадмиевое изделие от коррозии? Почему? Напишите уравнения коррозии в кислой среде для обоих случаев.
Приложение
Номенклатура кислот
Кислоты можно разделить на бескислородные (HCl, HBr, HCN, H2S) и кислородсодержащие (HNO3, H2SO4, H3PO4).
В названиях бескислородных кислот к наименованию элемента добавляют слово водородная. Например, HCl - хлороводородная, H2S - сероводородная.
Названия кислородсодержащих кислот зависят от степени окисления кислотообразующего элемента. Максимальной степени окисления элемента соответствует суффикс –н или -ов (-ев) и окончание –ая. Например, HN+5O3 - азот-н-ая кислота, H2S+6O3 – серная кислота, HCl+7O4 - хлорная кислота, H3As+5O4 - мышьяковая кислота, H2Si+4O3 - кремниевая кислота. По мере понижения степени окисления центрального атома суффиксы изменяются в следующей последовательности: -оват-, -ист-, -оватист-. Например, HCl+5O3 - хлорн-оват-ая, HCl+3O2 - хлористая, HCl+1O - хлорноватистая кислоты. Если элемент образует кислоты только в двух степенях окисления, то для названия кислоты, соответствующей низшей степени окисления элемента, используется суффикс –ист; например HN+3O2 – азотистая кислота. Если элемент, находясь в одной и той же степени окисления, образует несколько кислот, содержащих по одному атому данного элемента в молекуле (например, HPO3 и H3PO4), то название кислоты, содержащей наименьшее число атомов кислорода, снабжается приставкой мета-, а название кислоты с наибольшим числом атомов кислорода - приставкой орто- (HPO3 - метафосфорная кислота, H3PO4 - ортофосфорная кислота). Если молекула кислоты содержит два атома кислотообразующего элемента, то перед её названием помещается числительная приставка дву- или ди-, например: H4P2O7 - двуфосфорная кислота, H2S2O7 – двусерная кислота.
Названия некоторых кислот и их солей
| Кислота | Названия | |
| кислоты | соли | |
| НАlO2 | метаалюминиевая | метаалюминаты |
| Н3АlOз | ортоалюминиевая | ортоалюминаты |
| H2ZnO2 | цинковая | цинкаты |
| Н3ВО3 | ортоборная | ортобораты |
| НВr | бромоводородная | бромиды |
| НСООН | муравьиная | формиаты |
| СН3СООН | уксусная | ацетаты |
| HCN | циановодородная (синильная) | цианиды |
| Н2СО3 | угольная | карбонаты |
| HCI | хлороводородная (соляная) | хлориды |
| HClO | хлорноватистая | гипохлориты |
| НСlO2 | хлористая | хлориты |
| НСlО3 | хлорноватая | хлораты |
| НСlO4 | хлорная | перхлораты |
| НСrО2 | метахромистая | метахромиты |
| Н2СrО4 | хромовая | хроматы |
| Н2Сr2O7 | дихромовая | дихроматы |
| HI | йодоводородная | йодиды |
| НМnО4 | марганцевая | перманганаты |
| Н2МnО4 | марганцоватая | манганаты |
| HNO2 | азотистая | нитриты |
| HNO3 | азотная | нитраты |
| HF | фтороводородная (плавиковая) | фториды |
| НРО3 | метафосфорная | метафосфаты |
| Н3РO2 | фосфорноватистая | гипофосфиты |
| Н3РОз | фосфористая | фосфиты |
| Н3РO4 | ортофосфорная | ортофосфаты |
| H2S | сероводородная | сульфиды |
| HSCN | роданистая | роданиды |
| H2SO3 | сернистая | сульфиты |
| H2SO4 | серная | сульфаты |
| H2S2O3 | тиосерная | тиосульфаты |
| H2SiO3 | метакремниевая | метасиликаты |
Приложение
Номенклатура солей
По современной номенклатуре название соли образуется из названия аниона (кислотного остатка) и названия катиона (металла или остатка основания) с указанием его степени окисления, если она непостоянна. Например, CaCO3 - карбонат кальция; MgCl2 - хлорид магния; Cr2(SO4)3 - сульфат хрома(III).
Названия кислых солей образуются добавлением к названию аниона приставки гидро-, указывающей на наличие атомов водорода в кислотном остатке, а при необходимости, если атомов водорода два и более, с соответствующими числительными (ди-, три-, тетра- и т.д.): NaHSO3 - гидросульфит натрия; Ca(H2PO4)2 - дигидрофосфат кальция.
Наличие гидроксид-ионов в составе основной соли обозначается приставкой гидроксо- перед названием катиона: (CuOH)2CO3 - гидроксокарбонат меди; Al(OH)2Cl - дигидроксохлорид алюминия.
Названия некоторых средних, кислых и основных солей
| Формула | Название |
| Средние соли | Содержат в своём составе катионы металлов и кислотные остатки |
| NaCl | хлорид натрия |
| K2SO4 | сульфат калия |
| K2CrO4 | хромат калия |
| Fe2(SO4)3 | сульфат железа (III) |
| (NH4)3PO4 | ортофосфат аммония |
| A1(NO3)3 | нитрат алюминия |
| Кислые соли | Содержат кислотные остатки с незамещёнными атомами водорода |
| NaHCO3 | гидрокарбонат натрия |
| K2HPO4 | гидроортофосфат калия |
| KH2PO4 | дигидроортофосфат калия |
| Ca(HS)2 | гидросульфид кальция |
| Fe(HCO3)2 | гидрокарбонат железа (II) |
| Ba(H2PO4)2 | дигидроортофосфат бария |
| Основные соли | Содержат в своём составе гидроксогруппы |
| (CaOH)2SO4 | гидроксосульфат кальция (сульфат гидроксокальция) |
| (CoOH)NO3 | гидроксонитрат кобальта (II) |
| FeOHCl | гидроксохлорид железа (II) (хлорид гидроксожелеза (II)) |
| FeOHCl2 | гидроксохлорид железа (III) (дихлорид гидроксожелеза (III)) |
| Fe(OH)2Cl | дигидроксохлорид железа (III) |
| Fe(OH)2NO3 | дигидроксонитрат железа (III) |
| [Fe(OH)2]2SO4 | дигидроксосульфат железа (III) |
| (AlOH)2SiO4 | ортосиликат гидроксоалюминия |
Электрохимический ряд напряжений металлов
Li Rb К Ва Sr Ca Na Mg Al Mn Zn Cr Fe Cd Co Ni Sn Pb H Sb Bi Cu Hg Ag Pd Pt
Au
Анионы по способности окисляться располагаются в следующем порядке: I-; Br-; S2-; Сl-; OH-; SO42-; NO3-; CO32-; РО43-; F- восстановительная активность уменьшается
Электродные процессы в водных растворах при электролизе солей:
| Li+ Rb+ K+ Ba2+ Sr2+ Ca2+ Na+ Mg2+ A13+ | Mn2+ Zn2+ Cr3+ Fe2+ Fe3+ Cd2+ Со2+ Ni2+ Sn2+ Pb2+ | Sb3+Bi3+Cu2+Hg2+Ag+Pd2+ Pt2+Au3+ |
| На катоде | ||
| При электролизе водных растворов не восстанав ливаются. На катоде восстанавливаются ионы водорода: 2Н+ + 2е- = Н2 или 2Н2О + 2е- = Н2 + 2OH- | При электролизе растворов восстанавливаются на катоде одновременно с молекулами воды: Меn⁺ + nē = Me° 2Н2О + 2e- = Н2 + 2ОН- | При электролизе растворов практически полностью восстанавливаются на катоде: Men⁺ + nē = Me° |
| На аноде В случае растворимого анода (Cu, Ag, Zn, Cd, Hg, Ni и др.) при электролизе водного раствора окисляется анод, и металл переходит в раствор в виде ионов: Ме° – nē = Men⁺. Например, Сu - 2е- = Сu2+ | ||
| В случае с инертным (нерастворимым) анодом (уголь, графит, платина, золото): 1) при электролизе водных растворов солей бескислородных кислот (Сl-, Вr-, I-, S2- и др.) окисляются анионы бескислородных кислот: 2Сl- - 2е- = С12 (кроме F⁻) ; 2) при электролизе водных растворов солей кислородсодержащих кислот окисляются молекулы воды или гидроксид-ионы: 2Н2О - 4е- = О2 + 4Н+ или 4ОН- - 4е- = О2 + 2Н2О. |
Например, в процессе электролиза NaCl в водном растворе в электролитической ванне накапливается NaOH, а у электродов выделяются H₂ и Cl₂. Суммарное уравнение электролиза 2 NaCl + 2 H₂O = H₂ + Cl₂ + NaOH.
Коэффициенты активности ¦ ионов при ионных силах раствора
| Ионная сила раствора I | Заряд иона z | Ионная сила раствора I | Заряд иона z | ||||
| ±1 | ±2 | ±3 | ±1 | ±2 | ±3 | ||
| 0,001 | 0,98 | 0,78 | 0,73 | 0,1 | 0,81 | 0,44 | 0,16 |
| 0,002 | 0,97 | 0,74 | 0,66 | 0,2 | 0,80 | 0,41 | 0,14 |
| 0,005 | 0,95 | 0,66 | 0,55 | 0,3 | 0,81 | 0,42 | 0,14 |
| 0,01 | 0,92 | 0,60 | 0,47 | 0,4 | 0,82 | 0,45 | 0,17 |
| 0,02 | 0,90 | 0,53 | 0,37 | 0,5 | 0,84 | 0,50 | 0,21 |
| 0,05 | 0,84 | 0,50 | 0,21 |
Приложение 2
Термодинамическая константа растворимости (произведение растворимости) труднорастворимых в воде электролитов при 25 0С
| Электролит | К0S (ПР) | Электролит | К0S (ПР) |
| AgBr | 6,3×10-13 | Cu(OH)2 | 2,2×10-20 |
| AgCl | 1,8×10-10 | CuS | 6,0×10-36 |
| Ag2CrO4 | 4,0×10-12 | Fe(OH)2 | 1,0×10-15 |
| AgJ | 1,1×10-16 | Fe(OH)3 | 3,8×10-38 |
| Ag2S | 5,9×10-50 | FeS | 5,0×10-18 |
| Ag2SO4 | 2,0×10-5 | HgS | 1,6×10-52 |
| BaCO3 | 4,9×10-9 | MnS | 2,5×10-10 |
| BaSO4 | 1,1×10-10 | PbCl2 | 2,0×10-5 |
| CaCO3 | 5,0×10-9 | PbBr2 | 9,1×10-6 |
| CaC2O4 | 1,8×10-9 | PbCrO4 | 1,8×10-14 |
| CaF2 | 4,0×10-11 | PbI2 | 8,0×10-9 |
| CaSO4 | 1,1×10-5 | PbS | 1,0×10-27 |
| Ca(OH)2 | 3,1×10-5 | PbSO4 | 1,6×10-8 |
| Ca3(PO4)2 | 1,0×10-29 | SrSO4 | 3,2×10-7 |
| Cd(OH)2 | 2,6×10-14 | Zn(OH)2 | 1,0×10-17 |
| CdS | 7,9×10-27 | ZnS | 1,6×10-24 |
Константы диссоциации некоторых слабых электролитов (при 25 0С)
| Формула | К*i | Ka | Формула | К*i | Ka | |
| H3BO3 | K1 | 7,1× 10-10 | H2S2O6 | K1 | 6,3× 10-1 | |
| H2B4O7 | K1 | 1,8× 10-4 | K2 | 4,0× 10-4 | ||
| K2 | 2,0× 10-8 | H2SO3 | K1 | 1,4× 10-2 | ||
| CO2 (aq)+H2O | K1 | 4,5× 10-7 | K2 | 6,2× 10-8 | ||
| K2 | 4,8× 10-11 | H2SO4 | K1 | - | ||
| HCOOH | K1 | 1,8× 10-4 | K2 | 1,15× 10-2 | ||
| CH3COOH | K1 | 1,74× 10-5 | H2Se | K1 | 1,3× 10-4 | |
| CH2ClCOOH | K1 | 1,4× 10-3 | K2 | 1,0× 10-11 | ||
| CCl3COOH | K1 | 2,0× 10-1 | H2SeO3 | K1 | 1,8× 10-3 | |
| H2C2O4 | K1 | 5,6× 10-2 | K2 | 3,2× 10-9 | ||
| K2 | 5,4× 10-5 | H2SeO4 | K1 | - | ||
| HCN | K1 | 5,0× 10-10 | K2 | 1,2× 10-2 | ||
| H2SiO3 | K1 | 1,3× 10-10 | H2Te | K1 | 2,3× 10-3 | |
| H4GeO4 | K1 | 7,9× 10-10 | K2 | 6,9× 10-13 | ||
| K2 | 2,0× 10-13 | H2TeO3 | K1 | 2,7× 10-3 | ||
| HN3 | K1 | 2,0× 10-5 | K2 | 1,8× 10-8 | ||
| HNO2 | K1 | 5,1× 10-4 | H6TeO6 | K1 | 2,45× 10-8 | |
| H3PO2 | K1 | 5,9× 10-2 | K2 | 1,1× 10-11 | ||
| H3PO3 | K1 | 3,1× 10-2 | K3 | 1,1× 10-15 | ||
| K2 | 1,6× 10-7 | HF | K1 | 6,2× 10-1 | ||
| H3PO4 | K1 | 7,1× 10-3 | HCl | - | - | |
| K2 | 6,2× 10-8 | HBr | - | - | ||
| K3 | 5,0× 10-13 | HI | - | - | ||
| H3BO3 | K1 | 6,3× 10-3 | HNO3 | - | - | |
| K2 | 1,6× 10-3 | HClO | - | 2,95× 10-8 | ||
| K3 | 5,4× 10-8 | HClO2 | - | 1,1× 10-2 | ||
| K4 | 9,3× 10-11 | HClO3 | - | - | ||
| H3AsO3 | K1 | 5,9× 10-10 | HClO4 | - | - | |
| H3AsO4 | K1 | 5,6× 10-3 | HBrO | - | 2,2× 10-9 | |
| K2 | 1,7× 10-7 | HBrO3 | - | 2,0× 10-1 | ||
| K3 | 2,95× 10-12 | HIO | - | 2,3× 10-11 | ||
| H2O2 | K1 | 2,0× 10-12 | HIO3 | - | 1,7× 10-1 | |
| H2S | K1 | 1,0× 10-7 | H5IO6 | K1 | 2,45× 10-2 | |
| K2 | 2,5× 10-13 | K2 | 4,3× 10-9 | |||
| H3S2O3 | K1 | 2,5× 10-1 | K3 | 1,0× 10-15 | ||
| K2 | 1,9× 10-2 | H2Cr2O7 | K2 | 2,3× 10-2 | ||
| H2MnO4 | K1 | ~10-1 | H2CrO4 | K1 | 1,6× 10-1 | |
| K2 | 7,1× 10-11 | K2 | 3,2× 10-7 | |||
| NH4OH | K1 | 1,8× 10-5 |
Взаимодействие серной и азотной кислот с некоторыми металлами
| Кислота (окислитель) | ||||
| Металл | H2SO4 | HNO3 | ||
| разб. | конц. | разб. | конц. | |
| К, Ва, Са, | соль + H2S + Н2О | соль + NH3 (NH4NO3) | соль + N2O+ Н2О | |
| Na, Mg | соль + H2 | + Н2O | ||
| Al, Cr, Fe | соль + H2 | пассивация (на холоде); | соль + NO+ Н2О | пассивация |
| при нагревании | ||||
| с А1 (соль + H2S+ Н2О), | ||||
| с Cr, Fe (соль + SO2+ Н2O) | ||||
| Zn, Sn | соль + H2 | соль + SO2+ Н2О | соль + NO+ Н2О | соль + NO2+ Н2О |
| Ni, Pb, | соль + SO2+ Н2О | соль + NO+ Н2О | соль + NO2+ H2O | |
| Cu, Hg, Ag | - | |||
