Горение газовых смесей
Исследование процесса горения горючих смесей отечественными и зарубежными учеными дало возможность теоретически обосновать многие явления, сопровождающие процесс горения, в том числе и скорость распространения пламени. Изучение скорости распространения пламени в газовых смесях позволяет определять безопасные скорости газо-воздушных потоков в трубопроводах вентиляционных, рекуперационных, аспирационных и других установок, где транспортируются газо- и пыле-воздушные смеси.
В 1889 г. русским ученым В.А Михельсоном в диссертации «О нормальной скорости воспламенения гремучих газовых смесей» были даны отчетливые физические представления о двух предельных случаях распространения пламени при нормальном или медленном горении и детонации.
Дальнейшее развитие теория нормального распространения пламени и детонации получила в работах советских ученых: Н. Н. Семенова, К. И. Щелкина, Д. А. Франк-Каменецкого, Л. Н. Хитрина, А. С. Соколика, В. И. Скобелкина и др., а также зарубежных ученых: Б. Льюиса, Г. Эльбе и др. В результате была создана теория воспламенения взрывоопасных смесей. Однако, попытки истолкования явлений распространения пламени как диффузии активных центров или объяснение пределов распространения пламени условиями обрыва цепей недостаточно убедительны.
В 1942 г. советский ученый Я. Б. Зельдович сформулировал положения теории горения и детонации газов. Теория горения дает ответ на основные вопросы: будет ли смесь данного состава горючей, какова будет скорость горения взрывоопасной смеси, каких особенностей и форм пламени следует ожидать. При горении происходит химическое взаимодействие горючего с окислителем, сопровождающееся выделением тепла и перемещением фронта пламени. Рассмотрим распространение пламени в трубе (рисунок 1.7), заполненной газо-воздушной смесью.
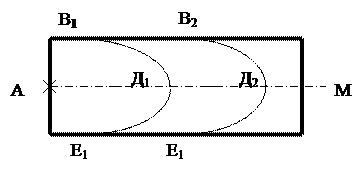
Рисунок 1.7 - Схема перемещения фронта пламени в цилиндрической трубе
После воспламенения смеси электрической искрой в точке А горение, возникшее в одной точке, начинает распространяться по трубе, образовав фронт пламени. К некоторому моменту времени 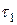 пламя находится в сечении B1Д1E1, а к моменту
пламя находится в сечении B1Д1E1, а к моменту 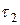 - в сечении В2Д2Е2, перемещаясь к стенке трубы
- в сечении В2Д2Е2, перемещаясь к стенке трубы 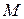 . Распространяющийся по взрывоопасной смеси фронт пламени представляет собой тонкую зону, отделяющую холодную непрореагировавшую смесь в ее исходном состоянии от продуктов горения. Ширина этой зоны, по вычислениям Зельдовича, равна от 10-2 до 10-4 см. Хотя зона пламени имеет незначительную ширину, в нем успевает протекать реакция горения из-за высокой температуры. Температура фронта пламени в зависимости от состава смеси колеблется от 1000 °С до 2800 °С. При перемещении фронта пламени температура несгоревшей части горючей смеси растет вследствие повышения давления смеси. Вблизи фронта пламени температура смеси также повышается вследствие передачи тепла из-за теплопроводности, диффузии нагретых молекул и излучения и на передней поверхности фронта (Д1 и Д2) пламени она равна температуре горючей смеси. Температуры смеси по оси трубы в моменты времени
. Распространяющийся по взрывоопасной смеси фронт пламени представляет собой тонкую зону, отделяющую холодную непрореагировавшую смесь в ее исходном состоянии от продуктов горения. Ширина этой зоны, по вычислениям Зельдовича, равна от 10-2 до 10-4 см. Хотя зона пламени имеет незначительную ширину, в нем успевает протекать реакция горения из-за высокой температуры. Температура фронта пламени в зависимости от состава смеси колеблется от 1000 °С до 2800 °С. При перемещении фронта пламени температура несгоревшей части горючей смеси растет вследствие повышения давления смеси. Вблизи фронта пламени температура смеси также повышается вследствие передачи тепла из-за теплопроводности, диффузии нагретых молекул и излучения и на передней поверхности фронта (Д1 и Д2) пламени она равна температуре горючей смеси. Температуры смеси по оси трубы в моменты времени 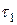 и
и 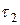 графически представлены на рисунке 1.8. Слой газа KK1, где повышается температура смеси, представляет собой фронт пламени. При повышении температуры фронт пламени расширяется (до K1K2) в стороны концевых стенок трубы А и М, смещая с некоторой скоростью несгоревшую смесь в сторону стенки М, а сгоревший газ в сторону стенки А.
графически представлены на рисунке 1.8. Слой газа KK1, где повышается температура смеси, представляет собой фронт пламени. При повышении температуры фронт пламени расширяется (до K1K2) в стороны концевых стенок трубы А и М, смещая с некоторой скоростью несгоревшую смесь в сторону стенки М, а сгоревший газ в сторону стенки А.
После воспламенения горючей смеси сферическая форма пламени очень быстро искажается и все более вытягивается в сторону еще не воспламененной смеси. Вытягивание фронта пламени и быстрое увеличение его поверхности сопровождается увеличением скорости движения центральной части пламени.
Это ускорение длится до тех пор, пока пламя не коснется стенок трубы или, во всяком случае, не подойдет очень близко к стенке трубы. В этот момент размер пламени резко уменьшается, и от пламени остается только небольшая его часть, перекрывающая все сечения трубы. Вытягивание фронта пламени и его интенсивное ускорение непосредственно после зажигания искрой, когда пламя еще не дошло до стенок трубы, вызываются увеличением объема продуктов сгорания.
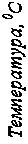
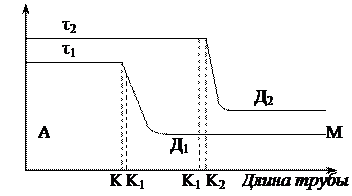
Рисунок 1.8 - Изменение температуры смеси на оси трубы во времени
Таким образом, в начальной стадии процесса образования фронта пламени, независимо от степени горючести газовой смеси, возникает ускорение и последующее торможение пламени, причем это торможение будет тем большим, чем больше скорость пламени.
На процесс развития последующих стадий горения оказывает влияние длина трубы. Удлинение трубы приводит к появлению вибраций с образованием ячеистой структуры пламени, ударной и детонационных волн.
Рассмотрим ширину зоны прогрева перед фронтом пламени. В указанной зоне химическая реакция не протекает и тепло не выделяется. Ширину зоны прогрева 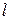 , м можно определить из зависимости:
, м можно определить из зависимости:
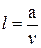 ,
,
где а — коэффициент температуропроводности, м2 /с;
v — скорость распространения пламени, м/с.
Для метано-воздушной смеси ширина зоны прогрева равна 6·10-4 м, для водородо-воздушной смеси она значительно меньше - 3·10-6 м.
Последующее горение происходит в смеси, состояние которой уже изменилось за счет теплопроводности и диффузии из соседних слоев. Перемешивание продуктов реакции никакого специфического каталитического влияния на скорость перемещения пламени не оказывает.
Рассмотрим теперь скорость перемещения фронта пламени по газовой смеси. Линейную скорость перемещения 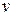 , м/с можно определить по формуле:
, м/с можно определить по формуле:
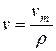 ,
,
где 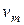 - массовая скорость горения, кг/(с · м2 );
- массовая скорость горения, кг/(с · м2 );
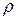 - плотность исходной горючей смеси, кг/м3.
- плотность исходной горючей смеси, кг/м3.
Линейная скорость перемещения фронта пламени не постоянна, она изменяется в зависимости от состава смеси, примеси инертных (негорючих) газов, температуры смеси, диаметра труб и др. Максимальная скорость распространения пламени наблюдается не при стехиометрической концентрации смеси, а в смеси с избытком горючего. При введении в горючую смесь инертных газов скорость распространения пламени снижается. Объясняется это снижением температуры горения смеси, так как часть тепла расходуется на нагрев не участвующих в реакции инертных примесей. На скорость распространения пламени влияет теплоемкость инертного газа. Чем больше теплоемкость инертного газа, тем больше он снижает температуру горения и тем сильнее уменьшает скорость распространения пламени. Так, в смеси метана с воздухом, разбавленной двуокисью углерода, скорость распространения пламени оказывается приблизительно в три раза меньше, чем в смеси, разбавленной аргоном.
Предварительный подогрев смеси увеличивает скорость распространения пламени. Установлено, что скорость распространения пламени пропорциональна квадрату начальной температуры смеси.
С увеличением диаметра труб скорость распространения пламени растет неравномерно. При увеличении диаметра труб от 10-1 до 1,5·10-1 м скорость растет довольно быстро, при дальнейшем увеличении диаметра труб она хотя и увеличивается, но до тех пор, пока диаметр не достигнет некоторого предельного диаметра, выше которого увеличение скорости не происходит.
При уменьшении диаметра трубы скорость распространения пламени уменьшается, и при некотором «малом» диаметре пламя в трубе не распространяется. Это явление можно объяснить увеличением наблюдающихся тепловых потерь через стенки трубы.
Следовательно, чтобы прекратить распространение пламени в горючей смеси, необходимо тем или иным способом понизить температуру смеси, охлаждая сосуд (в нашем примере трубу) извне или разбавляя смесь холодным инертным газом.
К газообразному топливу, которое широко применяется в промышленности и быту, относится природный газ газовых и газоконденсатных месторождений.
Углеводороды метанового ряда, входящие в состав природного газа, склонны к термическому разложению. Температура термического разложения углеводородных газов несколько выше температуры воспламенения газа. Поэтому при хорошем смесеобразовании, когда все молекулы горючего вступают в контакт с необходимыми для полного горения молекул окислителя, горение протекает до начала термического разложения углеводородных соединений и пиролиз их не происходит.
Если же количества окислителя недостаточно для полного окисления газа ( 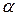 <1) или смесеобразование организовано плохо, то часть молекул газа, не имея контакта с молекулами окислителя, в зоне высоких температур подвергается термическому разложению с образованием более легких соединений и атомов углерода.
<1) или смесеобразование организовано плохо, то часть молекул газа, не имея контакта с молекулами окислителя, в зоне высоких температур подвергается термическому разложению с образованием более легких соединений и атомов углерода.
Например, разложение метана происходит по реакции:
СН4 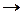 С+2Н2
С+2Н2
Атомы углерода, имея четыре свободные связи (валентности), отдельно не существуют и соединяются между собой, образуя твердые кристаллы графито-сажистые частицы (хлопья сажи).
Горение жидкостей
Процесс горения жидкостей начинается с воспламенения паро-воздушной смеси. Однако, не все жидкости при обычных условиях имеют над своей поверхностью достаточную концентрацию паров и такую скорость их образования, чтобы после воспламенения установился процесс горения. Стационарный процесс горения устанавливается только при определенной температуре жидкости, однако, и при более низких температурах жидкости уже могут представлять пожарную опасность, так как над поверхностью их может создаться взрывоопасная концентрация паров.
Горение жидкостей характеризуется двумя взаимосвязанными явлениями: испарением и сгоранием паро-воздушной смеси над поверхностью жидкости.
Испарению принадлежит исключительно важная роль, поскольку в конечном итоге оно определяет скорость сгорания жидкости.
Испарение - это переход жидкости в пар со свободной поверхности при температурах ниже точки кипения жидкости. Испарение происходит в результате теплового движения молекул жидкости. Скорость движения молекул колеблется в широких пределах, сильно отклоняясь в обе стороны от ее среднего значения. Часть молекул, имеющих достаточно большую кинетическую энергию, вырывается из поверхностного слоя жидкости в газовую (воздушную) среду. Избыточная энергия теряемых жидкостью молекул затрачивается на преодоление сил взаимодействия между молекулами и работу расширения (увеличения объема) при переходе жидкости в пар.
Испарение является эндотермическим процессом. Если к жидкости не подводится извне тепло, то в результате испарения она охлаждается. Скорость испарения определяется количеством пара, образующегося за единицу времени на единице поверхности жидкости. Она выражается в кг/(с·м2) или моль/(с·м2). Скорость испарения зависит от температуры жидкости. Это необходимо учитывать в производствах, связанных с применением, получением или переработкой легковоспламеняющихся жидкостей. Увеличение скорости испарения при повышении температуры приводит к более быстрому образованию взрывоопасных концентраций паров. Максимальная скорость испарения наблюдается при испарении в вакуум и в неограниченный объем.
Жидкость, находящаяся в закрытом сосуде, испаряясь, образует насыщенный пар. Насыщенным называется пар, находящийся в динамическом равновесии с жидкостью. Динамическое равновесие при данной температуре наступает, когда число испаряющихся молекул жидкости равно числу конденсирующихся молекул. Насыщенный пар, выходя из открытого сосуда в воздух, разбавляется им и становится ненасыщенным. Следовательно, в воздухе помещений, где находятся емкости с горючими жидкостями, имеется ненасыщенный пар этих жидкостей.
Насыщенные и ненасыщенные пары оказывают давление на стенки сосудов. Давлением насыщенного пара называют давление пара, находящегося в равновесии с жидкостью при данной температуре.
Давление насыщенного пара всегда выше, чем ненасыщенного. Оно не зависит от количества жидкости, величины ее поверхности, формы сосуда, а зависит только от температуры и природы жидкости. С повышением температуры давление насыщенного пара жидкости увеличивается; при температуре кипения давление пара равно атмосферному. Для каждого значения температуры давление насыщенного пара индивидуальной (чистой) жидкости постоянно. Давление насыщенного пара смесей жидкостей (нефть, бензин, керосин и др.) при одной и той же температуре зависит от состава смеси. Оно увеличивается с увеличением содержания в жидкости низкокипящих продуктов.
Для большинства жидкостей давление насыщенного пара при различной температуре известно. Давление насыщенных паров некоторых жидкостей при различных температурах приведено в таблице 1.3.
Таблица 1.3 - Давление насыщенных паров веществ при различных температурах
| Вещество | Давление насыщенных паров в Па при температуре | ||||||
| -20 oС | -10 oС | -0 oС | +10 oС | +20 oС | +30 oС | +40 oС | |
| Ацетон | - | 5159,6 | 8439,3 | 14705,4 | 24531,2 | 37330,2 | 55901,9 |
| Бензол | 986,6 | 1946,5 | 3546,4 | 5959,5 | 9865,8 | 15785,3 | 24197,9 |
| Бутилацетат | - | 480,0 | 933,3 | 1853,2 | 3333,1 | 5692,8 | 9452,5 |
| Бакинский авиационный бензин | - | - | 11732,3 | 15198,7 | 20531,6 | 20531,6 | 37730,1 |
| Метиловый спирт | 826,6 | 1786,5 | 3573,0 | 6692,8 | 11812,3 | 19998,3 | 32463,9 |
| Сероуглерод | 6466,1 | 10799,1 | 18531,8 | 27064,4 | 40236,6 | 58261,7 | 82259,7 |
| Скипидар | - | - | 266,6 | 386,6 | 586,6 | 919,9 | 1439,9 |
| Толуол | 226,6 | 453,3 | 893,3 | 1693,2 | 2973,1 | 4959,5 | 7906,0 |
| Этиловый спирт | 333,3 | 746,6 | 1626,5 | 3173,1 | 5866,2 | 10412,4 | 17785,2 |
| Этиловый эфир | 8932,6 | 14972,1 | 24584,6 | 38236,7 | 57688,4 | 84632,8 | |
| Этилацетат | 866,6 | 1719,9 | 3226,4 | 5706,2 | 9705,8 | 15825,3 | 24491,3 |
Давление насыщенного пара жидкостей обусловлено числом молекул, ударяющихся о стенки сосуда, или концентрацией паров над поверхностью жидкости. Чем выше концентрация насыщенного пара, тем больше будет его давление. Связь между концентрацией насыщенного пара и его парциальным давлением можно найти следующим образом.
Допустим, что удалось бы отделить пар от воздуха, причем давление в той и другой части осталось бы равным общему давлению 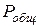 . Тогда объемы, занимаемые паром и воздухом, соответственно уменьшились бы. Согласно закону Бойля - Мариотта, произведение давления газа на его объем при постоянной температуре есть величина постоянная, т. е. для нашего гипотетического случая получим:
. Тогда объемы, занимаемые паром и воздухом, соответственно уменьшились бы. Согласно закону Бойля - Мариотта, произведение давления газа на его объем при постоянной температуре есть величина постоянная, т. е. для нашего гипотетического случая получим:
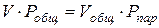 , (1.18)
, (1.18)
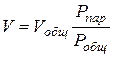 (1.19)
(1.19)
Если объем смеси принять за 100 %, то содержание пара в объемных процентах может быть найдено из пропорции:
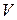 - 100 %
- 100 %
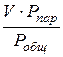 - С
- С
Откуда:
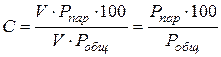 , (1.20)
, (1.20)
С помощью этой формулы (1.20) можно определять концентрацию паров жидкости в резервуарах, бочках, цистернах и других емкостях.
Основными видами жидкого топлива являются продукты переработки нефти: бензин, керосин, соляровое масло, мазут. Температура кипения отдельных фракций, входящих в состав жидких углеводородных топлив, ниже температуры термического разложения.
Интенсификация испарения жидкостей достигается путем увеличения площади удельной поверхности. Общепринятым способом увеличения площади поверхности испарения является дробление жидкого топлива на мельчайшие частицы (капли), называемое распылением. При распылении образуются частицы размером от нескольких микрометров до десятых долей миллиметра. Для распыления жидких топлив применяют различной конструкции форсунки.
Первой стадией горения жидкого вещества является нагревание и испарение горючего. Затем образовавшиеся пары горючего смешиваются с воздухом, и происходит нагревание, воспламенение и горение горючей смеси.
При горении жидкостей происходит не только химическая реакция (взаимодействие горючего вещества с кислородом воздуха), но и наблюдаются физические явления, без которых горение невозможно.
Взаимодействие горючих паров с кислородом воздуха происходит в зоне горения, в которую непрерывно должны поступать горючие пары и воздух. Это возможно, если жидкость будет получать определенное количество тепла, необходимое для испарения. Тепло в процессе горения поступает только из зоны горения (пламени), где оно непрерывно выделяется. Тепло от зоны горения к поверхности жидкости передается посредством излучения. Передача тепла путем теплопроводности невозможна, так как скорость движения паров от поверхности жидкости к зоне горения больше скорости передачи тепла по ним от зоны горения к жидкости. Передача тепла конвекцией также невозможна, так как поток паров в объеме пламени направлен от поверхности менее нагретой (жидкость) к поверхности более нагретой.
Количество тепла, излучаемое пламенем, зависит от степени черноты пламени и его температуры. Степень черноты пламени определяется концентрацией углерода, выделяющегося в пламени жидкости. Например, степень черноты пламени при горении нефти и нефтепродуктов в больших резервуарах близка к единице.
Количество тепла, поступающего от факела ( 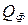 ) в единицу времени на единицу поверхности жидкости, может быть определено по формуле:
) в единицу времени на единицу поверхности жидкости, может быть определено по формуле:
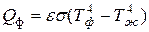 , (1.21)
, (1.21)
где 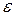 - степень черноты;
- степень черноты;
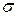 - постоянная Стефана-Больцмана, равная 5,67·10-8 Вт/(м2·К4);
- постоянная Стефана-Больцмана, равная 5,67·10-8 Вт/(м2·К4);
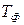 - температура пламени факела, К;
- температура пламени факела, К;
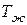 - температура поверхности жидкости, К.
- температура поверхности жидкости, К.
Это тепло расходуется на испарение жидкости ( 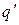 ), ее нагревание от начальной температуры до температуры поверхности (
), ее нагревание от начальной температуры до температуры поверхности ( 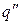 ), т. е. прогрев жидкости в глубину:
), т. е. прогрев жидкости в глубину:
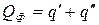 , (1.22)
, (1.22)
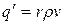 , (1.23)
, (1.23)
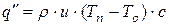 , (1.24)
, (1.24)
где 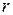 - удельное количество теплоты испарения, Дж/кг;
- удельное количество теплоты испарения, Дж/кг;
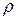 - плотность, кг/м3;
- плотность, кг/м3;
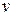 - линейная скорость горения, м/с;
- линейная скорость горения, м/с;
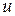 - скорость прогрева жидкости в глубину, м/с;
- скорость прогрева жидкости в глубину, м/с;
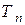 - температура поверхности жидкости, К;
- температура поверхности жидкости, К;
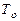 - начальная температура жидкости, К;
- начальная температура жидкости, К;
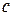 - удельная теплоемкость жидкости, Дж/(кг · К).
- удельная теплоемкость жидкости, Дж/(кг · К).
Таким образом:
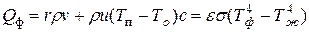 . (1.25)
. (1.25)
В установившемся процессе горения (т.е. при постоянной температуре пламени) наблюдается равновесие между количеством сгоревшего в зоне горения (пламени) вещества и массой пара, поступающего в пламя. Это определяет постоянную скорость испарения и, следовательно, выгорания жидкости в течение всего процесса горения.
Различают две скорости горения жидкостей: весовую (массовую) и линейную.
Весовой скоростью называется масса жидкости, выгорающей в единицу времени с единицы поверхности (1.26):
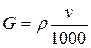 , (1.26)
, (1.26)
Под линейной скоростью горения жидкости понимается высота ее слоя, выгорающего в единицу времени (1.27):
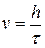 , (1.27)
, (1.27)
где 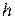 - высота слоя сгоревшей жидкости, м;
- высота слоя сгоревшей жидкости, м;
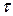 - время горения, с.
- время горения, с.
Зная или определив линейную скорость выгорания, можно вычислить весовую и наоборот.
Скорость горения жидкостей непостоянна и изменяется в зависимости от начальной температуры, диаметра резервуара, уровня жидкости в резервуаре, скорости ветра и других факторов. Для горелок малых диаметров скорость сгорания сравнительно велика. С увеличением диаметра скорость сгорания сначала уменьшается, а затем возрастает, пока не достигнет определенного постоянного значения для данной жидкости. Такая зависимость обусловлена различными причинами. На скорость горения в малых горелках существенно влияют стенки, так как пламя, соприкасаясь с ними, нагревает верхнюю кромку до высокой температуры. От верхней кромки тепло благодаря теплопроводности распространяется по всей стенке и передается жидкости. Этот дополнительный приток тепла со стороны стенки увеличивает скорость испарения жидкости. Увеличение скорости горения с увеличением диаметра связано с переходом от ламинарного режима горения к турбулентному. Этот переход сопровождается уменьшением полноты сгорания, а большое количество выделяющейся сажи способствует увеличению степени черноты пламени, что приводит к увеличению теплового потока от пламени. При турбулентном горении обеспечивается наиболее быстрый отвод паров от поверхности жидкости, увеличивается скорость испарения.
Скорость горения в больших резервуарах увеличивается с ростом диаметра незначительно. Считают, что скорость горения в резервуарах диаметром больше 2 мпрактически одинакова.
Сильный ветер способствует смешиванию паров с воздухом, повышению температуры пламени, в результате чего интенсивность горения увеличивается.
По мере снижения уровня жидкости в резервуаре увеличивается расстояние от пламени до поверхности жидкости, вследствие чего уменьшается приток тепла к жидкости. При этом скорость сгорания постепенно уменьшается и при некотором критическом расстоянии поверхности жидкости от кромки борта может наступить самотушение. Это расстояние называется критической высотой; она увеличивается с увеличением диаметра резервуара. Для больших резервуаров зависимость скорости горения от высоты свободного борта практического значения не имеет, так как высота стандартных резервуаров всегда значительно меньше критической высоты. Так, расчет показывает, что самотушение в резервуаре диаметром 23 м может наступить при высоте его более 1000 м. Действительная высота резервуара 12 м.
