Понятие об оптической активности и оптической изомерии
Под оптической активностью вещества понимают его способность отклонять плоскость поляризованного луча света вправо или влево на определенный угол.
Явление оптической активности было открыто в 1815 году физиком Ж.Б. Био (Франция).
В 1848 году Луи Пастер, изучая кристаллы винной кислоты, заметил, что оптически неактивный Na-аммоний тартрат существовал в виде двух типов кристаллов, которые были зеркальными отражениями друг друга. Пастер разделил правоориентированные и левоориентированные кристаллы. Их водные растворы оказались оптически активными. Удельное вращение двух растворов было одинаковым по величине, но разным по знаку. Поскольку различное оптическое вращение наблюдалось для растворов, Пастер сделал вывод, что это свойство характеризует молекулы, а не кристаллы, и предположил, что молекулы этих веществ являются зеркальными отображениями друг друга. Это предположение легло в основу стереохимии, изучающей пространственное строение молекул и его влияние на химические и физические свойства веществ.
Первая стереохимическая теория, объясняющая причины оптической активности веществ, была создана в 1874 году одновременно двумя учеными – голландским химиком Я.Х. Вант-Гоффом и французом Ж. Ле Бель. Основой этой теории явилось представление о тетраэдрической модели атома углерода, т.е. все четыре валентности углеродного атома лежат не в одной плоскости, а направлены к углам тетраедра.
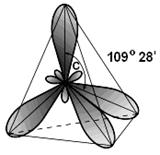
Как было установлено, чаще всего оптическая активность обусловлена наличием в молекуле асимметрического углеродного атома, т.е. С-атома, все валентности которого, направленные к углам тетраэдра, заполнены различными атомами или группами атомов (радикалами или заместителями). Асимметрические С-атомы в химии обозначают *. Например:
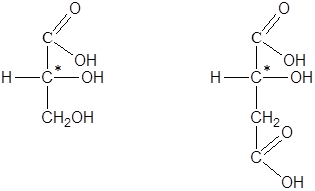
глицериновый альдегид яблочная кислота
Явление оптической активности связано с наличием оптических изомеров – веществ, имеющих одинаковый порядок связей атомов в молекуле, но различное их пространственное расположение. Оптические изомеры по пространственному строению представляют собой как зеркальные отображения друг друга, т.е. зеркальные антиподы или энантиомеры. Энантиомеры относятся друг к другу как правая и левая рука. Все константы энантиомеров, кроме удельного вращения (α) одинаковы.
Две формы вещества, имеющие зеркально-противоположные конформации, вращают поляризованный луч света в противоположные стороны: (+) – вправо, (-) – влево на один и тот же угол, называют оптическими антиподами или энантиомерами.
Какую же пространственную конформацию считать правовращающей, а какую левовращающей?
Общепринятый в настоящее время условный способ обозначения был впервые предложен Э. Фишером (1891г.), затем несколько видоизменен М.А. Розановым (1906г.) и подробно обсужден Хадсоном (1949г.). В качестве стандарта используется глицериновый альдегид:

D(+) - глицериновый L(-) - глицериновый
альдегид альдегид
Однако оказалось, что принадлежность к D(d) –или L(l) – типу конфигурации не всегда означает, что направление вращения идет (+) вправо или (-) влево. Возможны ситуации, что Д – конформация, а вращает плоскость поляризованного луча влево (-), или L – конформация, а вращает вправо (+). Поэтому буквенные обозначения D(d) или L(l) определяют пространственную ориентацию атомов или атомных групп вокруг асимметричного С-атома, а знаки (+)- правое вращение, (-) – левое вращение.
Смесь (+) и (-) форм (а в большинстве случаев это смесь Д- и L – форм) в соотношении 1:1 называют рацемат или рацемическая смесь. Она оптически неактивна (±). Если в органическом соединении несколько асимметричных С-атомов, количество оптических изомеров определяют по формуле:
N = 2n
где N – количество оптических изомеров;
n – количество асимметрических С-атомов.
Изомерия молочной кислоты

D(-) – молочная кислота L(+) –молочная кислота
(Образуется в мышцах при интенсивной работе)(Образуется при скисании молока)
Изомерия винной кислоты
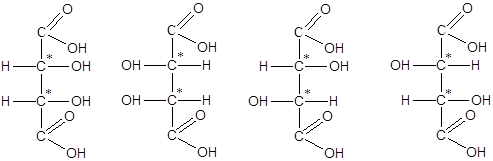
Мезовинная кислота L(-) - винная D(+) – винная кислота
У мезо-форм одна половина молекулы имеет (+) конфигурацию, другая (-) конфигурацию (например, у мезовинной кислоты). В результате «внутренней компенсации» знака вращения мезо-формы оптически неактивны и в отличие от рацематов их нельзя разделить на энантиомеры.
Значение оптической изомерии
Каждое оптически активное вещество при исследовании в определенных условиях вращает плоскость поляризации на определенный угол, величина которого является постоянной и характерной для данного вещества, т.е. такой же константой, как температура плавления, температура кипения вещества, плотность и т.д. Константа, характеризующая оптическую активность вещества, называется удельным вращением. Таким образом, определяя удельное вращение можно определить подлинность вещества.
Оптическая изомерия имеет очень большое биологическое значение. Ферменты, катализирующие биохимические реакции в живых организмах, обладают оптической специфичностью, т.е. они действуют только на определенные оптические изомеры (например на Д-моносахариды, на L-аминокислоты и т.д.). На оптические антиподы этих веществ ферменты не действуют, т.е. не вовлекают их в метаболизм. Накапливаясь в тканях, такие изомеры могут вызывать патологические процессы.
