Последовательность выполнения работы.
1. Рассчитать объем концентрированного раствора карбонат натрия с известной молярной его концентрацией, который понадобится для приготовления 100 см3 разбавленного раствора с заданной молярной концентрацией эквивалента карбоната натрия , используя для этого соответствующие правила расчета при разбавлении раствора водой (учтите, что в расчетной формуле концентрации вещества в исходном и конечном растворах должны быть выражены одинаковым способом). Точность расчета объема – до 0,1 см3.
Найденный объем концентрированного раствора соды с помощью градуированной пипетки вместимостью 10,0 см3 или бюретки перенести в мерную колбу вместимостью 100,0 см3, разбавить его дистиллированной водой до метки на колбе и тщательно перемешать.
2. Выбрать оптимальный объем аликвотной части Vал анализируемого раствора, обеспечивающий наиболее низкое значение относительной случайной ошибки определения объема титранта Vбюр, из расчета, что на ее титрование стандартным раствором серной кислоты с концентрацией с (½ H2SO4) = 0,1 моль/дм3 в присутствии метилоранжа будет израсходовано, например, 20 см3 стандартного раствора реагента. Расчет оптимального объема аликвотной части анализируемого раствора проводят на основании закона эквивалентов (уравнение (8)), откуда
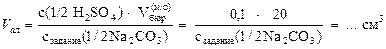
Полученный результат следует округлить до ближайшего целого числа, чтобы не допустить случайную ошибку при отборе аликвотной части раствора для титрования, и внести в заголовок таблицы 4.
3. Заполнить бюретку стандартным раствором серной кислоты, c (1/2 Н2SO4) = 0,1 моль/дм3, удаляя избыток рабочего раствора в колбу для сливов через носик бюретки. Процедура заполнения бюретки стандартным раствором реагента подробно описана в предыдущей работе.
4. Для проведения титрования аликвотную часть анализируемого раствора, рассчитанную в пункте 2, отбирают из мерной колбы с помощью градуированной пипетки и переносят в колбу для титрования (если пипетка не проходит в горлышко мерной колбы, то перед отбором аликвотных частей раствор полностью переливают в чистую сухую коническую колбу или стакан).
5. Титрование проводят согласно схеме; последовательность действий при его проведении – см. лабораторную работу № 2.1, пункт 3, второй и четвертый абзацы.
В коническую колбу для титрования добавляют с помощью мерного цилиндра около 50 см3 дистиллированной воды, затем несколько(3-4) капель фенолфталеина, - раствор окрасится в малиновый цвет (почему?). Титрование ведут до момента обесцвечивания раствора от одной добавленной избыточной капли титранта, что соответствует ТЭI , фиксируют по бюретке объем 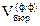 , заносят в таблицу, после чего в этот же растворвносят несколько капель метилоранжа – смесь окрасится в желтый цвет, и,не добавляя титрант в бюретку до нулевой отметки, продолжают титрование до изменения окраски реакционной смеси с желтой на розовую от одной избыточной капли стандартного раствора серной кислоты, что соответствует ТЭII ; по бюретке фиксируют объем
, заносят в таблицу, после чего в этот же растворвносят несколько капель метилоранжа – смесь окрасится в желтый цвет, и,не добавляя титрант в бюретку до нулевой отметки, продолжают титрование до изменения окраски реакционной смеси с желтой на розовую от одной избыточной капли стандартного раствора серной кислоты, что соответствует ТЭII ; по бюретке фиксируют объем 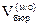 .заносят конечные показания на шкале бюретки в таблицу.
.заносят конечные показания на шкале бюретки в таблицу.
Первое титрование является ориентировочным и служит для грубой оценки объемов 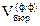 и
и 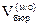 . Оттитрованный раствор выливают в раковину, колбу ополаскивают сначала водопроводной, а затем дистиллированной водой, после этого в нее отбирают новую аликвотную часть анализируемого раствора для выполнения контрольных титрований. Контрольные титрования проводят три – четыре раза, устанавливая перед титрованием каждой новой аликвотной части анализируемого раствора уровень стандартного раствора кислоты в бюретке на нулевое деление.
. Оттитрованный раствор выливают в раковину, колбу ополаскивают сначала водопроводной, а затем дистиллированной водой, после этого в нее отбирают новую аликвотную часть анализируемого раствора для выполнения контрольных титрований. Контрольные титрования проводят три – четыре раза, устанавливая перед титрованием каждой новой аликвотной части анализируемого раствора уровень стандартного раствора кислоты в бюретке на нулевое деление.
Допустимый разброс значений соответствующих объемов в параллельных титрованиях не должен превышать 0,1 см3 (одна капля титранта имеет объем около 0,05 см3). Результаты контрольных титрований заносят в таблицу 3, рассчитывают средний объем титранта для каждого индикатора и на их основе делают вычисления для заполнения последующих граф таблицы, используя для этого уравнения (4.7) и (4.8).
Из схемы титрования следует, что между объемами 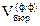 и
и 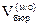 должна существовать связь:
должна существовать связь: 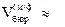
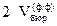 ; на практике обычно левая часть несколько больше, чем правая. Как этот факт можно связать с возможным изменением состава исследуемого раствора соды при его контакте с воздухом?
; на практике обычно левая часть несколько больше, чем правая. Как этот факт можно связать с возможным изменением состава исследуемого раствора соды при его контакте с воздухом?
По результатам проведенного анализа делают заключение о качестве приготовления раствора карбоната натрия и определяют относительную ошибку:
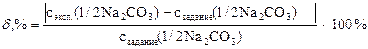
Таблица 3 – Результаты ацидиметрического анализа разбавленного раствора карбоната натрия
(титрант – с ( ½ H2SO4) = 0,1 моль/дм3; Vал = . . . см3; Vзадачи = 100 см3 )
| № | Объем титранта, см3 | с ( 1/1 Na2CO3), моль/дм3 по ф/ф | с (½ Na2CO3), моль/дм3 по м/о | m(Na2CO3) в задаче, г | |
| ТЭI по ф/ф | ТЭII по м/о | ||||
| . . . . . . . . . ср. знач. | . . . . . . . . . ср. знач. |
Все вычисления выполнить в рабочей тетради. Составить отчет по проделанной работе.
В выводах по работе указать роль каждого из индикаторов, используемых в данной работе и сравнить с их ролью при алкалиметрическом определении серной кислоты в растворе.
