Дослід 6. порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
Атоми галогенів, що перебувають у бензеновому кільці, мало рухливі. Вони переважно вступають у реакцію обміну на відміну від атомів галогену, які перебувають у боковому ланцюзі.
Стійкість галогену в бензеновому кільці. У пробірку набирають кілька крапель бромбензену або хлоробензену, добавляють 2–3 мл 1%-ного водного розчину нітриту аргентуму і нагрівають. Утворення осаду броміду або хлориду аргентуму не спостерігається, що свідчить про важку заміну атома галогену, безпосередньо з'єднаного з бензеновим ядром.
В умовах цього досліду реакція гідролізу бромбензену або хлоробензену не відбувається.
Рухливість галогену в боковому ланцюзі. У невеликий циліндр із притертою пробкою вміщують кілька крапель хлористого бензилу і добавляють 5–8 мл 2 %-ного водно-спиртового розчину нітрату аргентуму. Циліндр закривають пробкою. При енергійному збовтуванні спочатку спостерігається помутніння розчину, а потім з'являється осад хлориду аргентуму, кількість якого збільшується під час слабкого нагрівання. Це вказує на легкість заміни атома хлору, що перебуває в боковому ланцюзі. Реакція проходить за таким рівнянням:
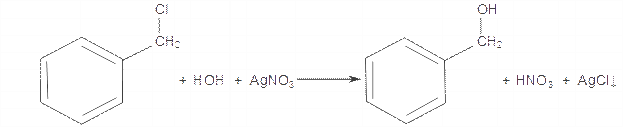
Примітка. Залишок хлористого бензилу і посуд, в якому він знаходився, треба обробити розчином гідроксиду натрію, оскільки хлористий бензил с лакриматором і подразнює слизову оболонку.
Контрольні запитання
- Запропонуйте схеми синтезу: хлористого метилу, фторпропану, йодбутану, ізопропілброміду.
- Зазначте основні напрямки використання галогенпохідних в будівництві, сільському господарстві, в медицині та ін. Наведіть приклади.
- Які сполуки використовуються як фреони. Напишіть їх формули.
ОКСИГЕНВМІСНІ СПОЛУКИ ТА ЇХ ПОХІДНІ.
ОДНОАТОМНІ СПИРТИ
Спирти розглядаються як похідні вуглеводнів, у яких один або кілька атомів Гідрогену заміщені на гідроксили. Кількість гідроксильних груп визначає атомність спирту. Розрізняють насичені, ненасичені й ароматичні спирти.
Одноатомні спирти (алканоли) — похідні алканів, у яких один атом Гідрогену заміщений на гідроксильну групу. Загальна формула — CnH2n+1OH. Ізомерія алканолів залежить від будови карбонового ланцюгу й положення гідроксильної групи. Розрізняють первинні, вторинні й третинні спирти.
Назва насичених одноатомних спиртів за тривіальною номенклатурою утворюється від назви залишків, із якими зв'язана гідроксильна група. За раціонального номенклатурою — як заміщені карбінолу (метилового спирту). За систематичною — назву утворюють від назв вуглеводнів із добавкою закінчення -ол і числовим позначенням атома Карбону, біля якого знаходиться гідроксильна група.
У вільному стані в природних умовах зустрічаються тільки деякі спирти. Зазвичай їх добувають синтетичними методами, із яких найбільше значення мають гідроліз галогенопохідних, гідратація алкенів, відновлення альдегідів і кетонів, окислення етерів, синтез за допомогою металоорганічних сполук і бродіння цукристих речовин.
Наявність гідроксильної групи в молекулі речовини зумовлюють її фізико-хімічні властивості. Підвищення температури кипіння пояснюється асоціацією молекули спирту, що відбувається завдяки появі водневих зв'язків.
З хімічного погляду спирти виявляють високу реакційну здатність. Вони легко вступають у різні хімічні перетворення: реакції заміщення, дегідратації, дегідрування, естерифікації, окислення.
Багатоатомні спирти розглядаються як похідні вуглеводнів, у яких два або кілька атомів Гідрогену заміщені на гідроксили. Двохатомні спирти називають гліколями, трьохатомні – гліцеринами, чотирьохатомні – еритритами, п'ятиатомні – пентитами, шестиатомні – гекситами і т.д. За номенклатурою IUPAC назви двохатомних спиртів мають закінчення -діол, трьохатомних – -тріол. Цифрами вказується положення гідроксильних груп у карбоновому ланцюзі.
Введення в молекулу другого й третього гідроксилу значно підвищує температуру кипіння, збільшує густину спирту і його розчинність у воді, приводить до збільшення рухомості атомів Гідрогену в гідроксилах. Завдяки цьому багатоатомні спирти здатні розчиняти гідрати оксидів важких металів.
Фенолами називають похідні ароматичних вуглеводнів, у яких один або кілька атомів Гідрогену бензенового кільця заміщені на гідроксильну групу. За кількістю гідроксильних груп розрізняють одно-, двох-, і багатоатомні феноли. У разі заміни атома Гідрогену в боковому ланцюзі на гідроксильну групу одержують ароматичні спирти.Більшість фенолів та їх похідних мають тривіальні назви.
У промисловості феноли добувають із кам'яновугільної смоли. Найбільше значення із синтетичних методів має отримання фенолів із галогенопохідних, солей сульфокислот (лужна плавка), первинних ароматичних аміносполук через діазосполуки.
Феноли — тверді кристалічні речовини з характерним запахом, добре розчинні в спирті, етері, бензені. Легко відганяються з водяною парою і є антисептиками.
Реакції, які характеризують хімічні властивості фенолів, поділяють на два типи: реакції за рахунок фенольного гідроксилу та реакції за рахунок бензенового кільця. До першого відносять реакції утворення фенолятів, алкілювання й ацилювання; до другого — реакції електрофільного заміщення атомів Гідрогену в бензеновому кільці: нітрування, сульфування, галогену-вання та ін. Крім того, феноли здатні до реакцій гідрування, поліконденсації й окислення.
Лабораторна робота № 5
