Поверхностное натяжение минерального раствора
Одним из показателей способности вытягивания минерального раствора в волокна является поверхностное натяжение (Н/м или дин/см). Оно определяется, как отношение вязкости (Па•с) к силам свободной энергии поверхности раствора.
Поверхностное натяжение - работа, которую необходимо затратить на образование единицы новой поверхности в плоскости раздела жидкой и твердой фаз при постоянной температуре.
Силы поверхностного натяжения существенно влияют на процесс получения волокон из минерального раствора. С их действием связано явление образования «корольков».При некоторых значениях вязкости и поверхностного натяжения наступает равновесие, а затем состояние, при котором силы внутреннего трения превышают силы свободной энергии поверхности. В результате силы свободной энергии не способны разорвать струйки расплава, деформировать частички расплава - образуется «королек».
Взаимосвязь между вязкостью расплава и силами свободной энергии доказывается опытом. Если подвесить волокно, закрепив его верхний конец, и нагревать до температуры, выше которой вещество волокна находится в вязком состоянии, а ниже — в пластичном, то, прилагая к волокну в течение 1—2 ч растягивающее усилие, можно наблюдать в зависимости от его значения то удлинение волокна, то отсутствие заметной деформации, то укорочение волокна.
На границе с воздухом раствор образует свободную поверхность, наличие которой приводит к возникновению поверхностных явлений. Они возникают в особых физических условиях, в которых находятся молекулы вблизи свободной поверхности.
На каждую молекулу раствора действуют силы притяжения со стороны окружающих ее молекул, расположенных на расстоянии радиуса молекулярного действия. На молекулу М1(рис. 9), расположенную внутри раствора, действуют силы со стороны таких же молекул, и равнодействующая сил близка к нулю.
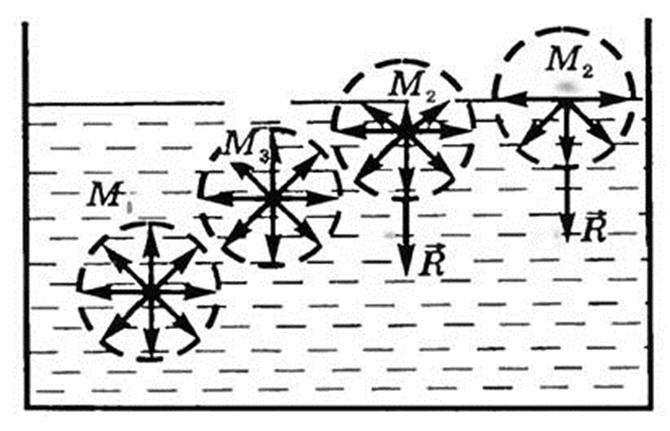 рис. 9. Поверхностные явления
рис. 9. Поверхностные явления
Для молекул M2 равнодействующие сил отличны от нуля и направлены внутрь раствора, перпендикулярно к поверхности. Все молекулы поверхностного слоя втягиваются внутрь. Но пространство внутри раствора занято другими молекулами, поэтому поверхностный слой создает давление на раствор (молекулярное давление), чтобы их протолкнуть.
Чтобы переместить молекулу M3, расположенную под поверхностным слоем, на поверхность, необходимо совершить работу против сил молекулярного давления. Т.е., молекулы поверхностного слоя раствора обладают дополнительной потенциальной энергией по сравнению с молекулами внутри расплава. Эту энергию называют поверхностной энергией.
Единицей коэффициента поверхностного натяжения в СИ является джоуль на квадратный метр (Дж/м2).
Коэффициент поверхностного натяжения — величина, численно равная работе, совершенной молекулярными силами при изменении площади свободной поверхности раствора на 1 м2 при постоянной температуре.
Любая система, предоставленная сама себе, стремится занять положение, в котором ее потенциальная энергия наименьшая, т.е., раствор стремится к сокращению свободной поверхности.Поверхностный слой раствора ведет себя подобно растянутой резиновой пленке, всегда стремясь сократить площадь своей поверхности до минимальных размеров, возможных при данном объеме.
Равнодействующая сил, действующих на все молекулы, находящиеся на границе свободной поверхности - сила поверхностного натяжения. Она действует так, что стремится сократить поверхность жидкости.
Коэффициент поверхностного натяжения σ численно равен силе поверхностного натяжения, действующей на единицу длины границы свободной поверхности расплава. Коэффициент поверхностного натяжения зависит от природы раствора, температуры и наличия примесей. При увеличении температуры коэффициент уменьшается.
Примеси в основном уменьшают коэффициент поверхностного натяжения.
Поверхностный слой раствора - эластичная растянутая пленка, охватывающая раствор и стремящаяся собрать его в одну «каплю». Если пленка под действием внешних сил растягивается, то сила поверхностного натяжения будет противодействовать растяжению в продольном направлении. При растяжении жидкой пленки расстояние между частицами не меняется, увеличение поверхности происходит в результате перехода молекул из толщи раствора в поверхностный слой. Поэтому при увеличении поверхности раствора сила поверхностного натяжения не изменяется (она не зависит от площади поверхности).
Смачивание
При соприкосновении с твердым телом силы сцепления молекул связующего с молекулами волокна играют существенную роль. Поведение связующего будет зависеть от того, что больше: сцепление между молекулами связующего или сцепление молекул связующего с молекулами волокна.
Смачивание — явление, возникающее вследствие взаимодействия молекул связующего с молекулами волокна. Если силы притяжения между молекулами связующего и волокна больше сил притяжения между молекулами связующего, то связующее будет смачиватьволокно; если силы притяжения молекул связующего и волокна меньше сил притяжения между молекулами связующего, то связующее не смочит волокно.
Из физики известно, что вода (в нашем случае раствор связующего) смачивает стекло, т.е., наше волокно.
Пример.
Смачивание или несмачивание жидкостью стенок сосуда, в котором она находится, влияет на форму свободной поверхности жидкости в сосуде. У самых стенок явление смачивания и несмачивания приводят к искривлению поверхности жидкости, возникают краевые эффекты.
Количественной характеристикой краевых эффектов служит краевой угол θ - угол между плоскостью касательной к поверхности жидкости и поверхностью твердого тела. Внутри краевого угла всегда находится жидкость (рис. 10, а,б). При смачивании он будет острым (рис. 10,а), а при несмачивании – тупым (рис. 10,б). В школьном курсе физики рассматривают только полное смачивание (θ = 0º) или полное несмачивание (θ = 180º).
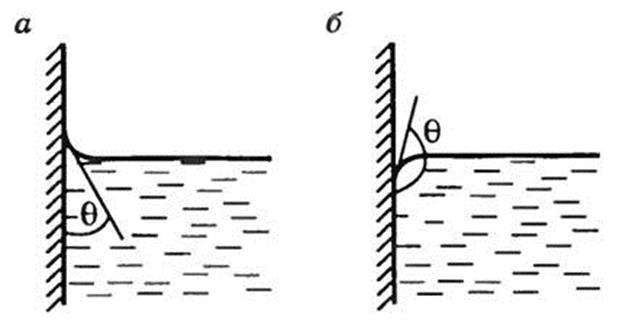 рис. 10. Явления смачивания в слое жидкости.
рис. 10. Явления смачивания в слое жидкости.
Если смачивающая жидкость находится на открытой поверхности твердого тела (рис. 11,а), то происходит ее растекание по этой поверхности. Если на открытой поверхности твердого тела находится несмачивающая жидкость, то она принимает форму, близкую к шаровой (рис. 11,б).
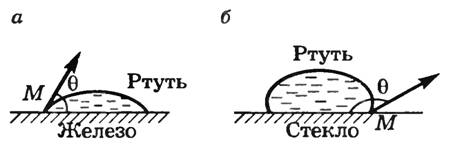
Рис. 11. Явления смачивания на поверхности.
Смачивание имеет важнейшее значение при нанесении связующего на волокна минеральной ваты. Хорошее смачивание необходимо при нанесении предварительного слоя силана, входящего в состав связующего и служащего подложкой для связующего. На местах пересечений волокон краевой угол связующего имеет острую форму, и место пересечения волокон как бы обволакивается связующим. После поликонденсации смолы происходит эффект «холодной» химической сварки волокон, придающий плите жесткость.
