Общий приход тепла на плавку
Физическое тепло подогретого лома
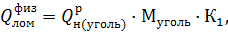
где К1 - коэффициент усвоения тепла угля.
Qнагр = 28680 · 0,6 · 0,35 = 6022,8 кДж
Тепло оставшейся части неокисленного углерода учитывается при расчете химического тепла реакций окисления элементов металлошихты.
Физическое тепло жидкого чугуна
Физическое тепло жидкого чугуна можно определить по формуле
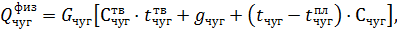
где Gчуг - количество жидкого чугуна в металлической шихте, Gчуг = 80 кг;
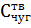 - теплоемкость твердого чугуна,
- теплоемкость твердого чугуна, 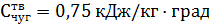 ;
;
tчуг - температура заливаемого в конвертер чугуна, tчуг = 1380 °С
gчуг - скрытая теплота плавления чугуна, gчуг = 217,9 кДж/кг;
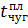 - температура плавления чугуна,
- температура плавления чугуна, 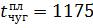 °С;
°С;
Cчуг - теплоемкость жидкого чугуна, Счуг = 0,92 кДж/кг · град;
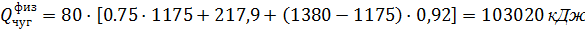
Химическое тепло металлошихты
Значения тепловых эффектов реакций окисления элементов при температурах их окисления приведены в таблице 18.
Таблица 18 - Значение тепловых эффектов реакций окисления
| Реакция | Тепловой эффект реакции окисления на 1 кг элемента, кДж |
| [C] + {O2} = {CO2} | |
| [C] + 0,5{O2} = {CO} | 10458,2 |
| [Si] + {O2} = (SiO2) | 30913,8 |
| [Mn] + 0,5{O2} = (MnO) | 7018,3 |
| 2P + 2,5{O2} = (P2O5) | 24327,1 |
| [Fe] + 0,5{O2} = (FeO) | 4826,9 |
| 2[Fe] + 1,5{O2} = (Fe2O3) | 7374,4 |
На основании данных таблицы 18 и результатов материального баланса можно определить химическое тепло реакций окисления элементов металлошихты Qхим, результаты представлены в таблице 19.
Таблица 19 - Химическое тепло реакций окисления
| Элемент-окисел | Выгорело элементов, кг | Расчет | Вносится тепла, кДж | |
| М.з. | [C] ® {CO2} | 0,545 | 0,545 · 34094 | 18581,230 |
| [C] ® {CO} | 3,593 | 3,593 · 10458,2 | 37576,313 | |
| [Si] ® (SiO2) | 0,576 | 0,576 · 30913,8 | 17806,349 | |
| [Mn] ® (MnO) | 0,315 | 0,315 · 7018,3 | 2210,765 | |
| [P] ® (P2O5) | 0,065 | 0,065 · 24327,1 | 1483,953 | |
| [Fe] ® (FeO) | 1,507 | 1,507 · 4826,9 | 7274,138 | |
| [Fe] ® (Fe2O3) | 0,45 | 0,45 · 7374,4 | 3318,48 | |
| [Fe] ® (Fe2O3)пыль | 0,6 | 0,6 · 7374 | 4424,640 | |
| Итого: | 7,651 | Итого: | 92675,868 |
2.1.4 Химическое тепло реакций шлакообразования 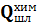
Считаем, что все количество SiO2, P2O5 и Fe2O3 в шлаке связано следующими реакциями:
SiO2 + 2CaO = (CaO)2 · SiO2 + 137432 кДж/кг·мольSiO2;
P2O5 + 4CaO = (CaO)4 · P2O5 + 691350 кДж/кг·мольP2O5;
Fe2O3 + CaO = (CaO) · Fe2O3 + 211176 кДж/кг·мольFe2O3;
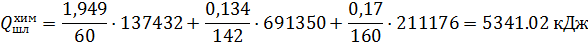
Физическое тепло миксерного шлака
Среднюю теплоемкость миксерного шлака определяем по формуле:
С0 = 0,73 + 0,003 · Тм.шл.,
где 0,73 - теплоемкость шлака при 0 К, кДж/кг·град;
0,0003 - приращение теплоемкости шлака на 1°, кДж/кг·град;
Тм.шл. - средняя температура миксерного шлака, К.
Среднюю температуру миксерного шлака, попадающего в конвертер из чугуновозного ковша, ориентировочно можно принимать на 15-20° ниже температуры заливаемого в конвертер чугуна, тогда:
Тм.шл. = (1380 - 20) + 273 = 1633К,
С0 = 0,73 + 0,0003 · 1633 = 1,22 кДж/кг·град.
Количество вносимого тепла миксерным шлаком определится из выражения:
Qм.шл. = Мм.шл. · (С0 · tм.шл. + qм.шл.),
где Мм.шл. - количество миксерного шлака на 100 кг металлошихты, кг;
tм.шл. - средняя температура миксерного шлака, °С;
С0 - средняя теплоемкость миксерного шлака, кДж/кг·град;
qм.шл. - средняя теплота плавления шлака, qм.шл. = 209,5 кДж/кг.
Qм.шл. = 0,5 · (1,22 · (1380 - 20) + 209,5) = 934,35 кДж
Общий приход тепла на плавку
Общий приход тепла на плавку рассчитывается следующим образом:
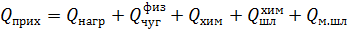
Qприх = 6022,8 + 103020 + 92675,868 + 5341,02 + 934,35 = 207994,038 кДж.
Расход тепла
Физическое тепло стали
Физическое тепло стали Q1 можно определить по уравнению
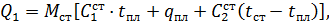
где Mст - вес жидкой стали перед раскислением, кг;
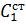 - теплоемкость твердой стали,
- теплоемкость твердой стали, 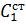 = 0,7 кДж/кг·град;
= 0,7 кДж/кг·град;
tпл - температура плавления стали, °С;
qпл - скрытая теплота плавления стали, qпл = 272,4 7 кДж/кг·град;
tст - температура стали перед выпуском, °С;
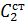 - теплоемкость жидкой стали,
- теплоемкость жидкой стали, 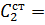 0,84 7 кДж/кг·град.
0,84 7 кДж/кг·град.
Температура плавления стали:
tпл=1539-65·(%C),
где 1539 - температура плавления чистого железа, °С;
65 - снижение температуры плавления стали на 1% углерода в металле, °С;
(%С) - содержание углерода в металле перед раскислением.
tпл = 1539 - 65 · 0,054 = 1535оС.
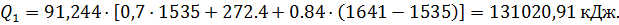
Физическое тепло шлака
Среднюю теплоемкость конечного шлака (как и миксерного) определяем по формуле:
C0 = 0,73 + 0,0003 × Tшл ,
где Тшл - температура конечного шлака, К.
Температуру конечною шлака принимаем выше температуры металла в конце продувки на 10°С, т.е. 1651°С, так как превышение температуры шлака над температурой металла составляет обычно 5-15°С.
С0 = 0,73 + 0,0003 · (1651 + 273) = 1,3 кДж/кг·град.
Потери тепла со шлаком определяются по формуле:
Q2 = (C0 · tшл + qшл) · Мшл,
где qшл - скрытая теплота плавления шлака, qшл = 209,5 кДж/кг·град;
Мшл - количество конечного шлака, кг.
Q2 = (1,3 · (1641 + 10) + 209,5) · 12,9 = 30389,82 кДж.
