Знак неравенства относится к необратимым процессам, а знак равенства - к обратимым процессам.
Чтобы энтропии веществ были сравнимы (для сопоставления и определения энтропии в различных процессах, в том числе и химических реакциях), их, как и тепловые эффекты принято относить к определенным условиям. Чаще всего значения S определяют при t =25°С и р=1 атм. (что соответствует стандартным условиям); при этом газы считают идеальными, а для растворов ( и ионов в растворах) принимают их состояние при концентрации, равной единице, предполагая, что раствор обладает свойствами бесконечно разбавленного раствора. Энтропия при этих условиях обозначается S°298 и называется стандартной энтропией S°298 (Дж/моль∙К) Часто пользуются и условным названием энтропийная единица ( э.е.): 1 э.е. = 1 кал/моль∙К (1кал =4.18 Дж). Значение энтропии для стандартных состояний веществ приведены в справочниках термодинамических величин и сравнимы по значению с S°298 (Н+(р.)), принятой равной нулю ( что объясняет отрицательные значения S°298 для некоторых ионов).
Наряду со значениями S°298 пользуются и величинами S°Т. Их тоже называют стандартными, однако высокотемпературные значения известны для сравнительно небольшого числа веществ.
Значение энтропии реакции может быть найдено с использованием следствия из закона Гесса, по формуле:
∆S°p.f=∑νjS°j - ∑νiS°i
гдеS°j, S°i – значения энтропии образования продуктов реакции и исходных веществ, νj ,νi - соответствующие стехиометрические коэффициенты в уравнении химической реакции.
Критерий самопроизвольности процесса устанавливается вторым законом термодинамики, который был сформулирован Клаузиусом в 1850 г. Второй закон (начало) термодинамики определяет направленность и пределы протекания самопроизвольных процессов, в том числе и биохимических:
В изолированных системах самопроизвольно могут совершаться процессы, при которых энтропия системы возрастает, т.е. ∆S>0.
Для неизолированных систем нужно учитывать не только изменение энтропии, но и изменение энергии. Поэтому необходимо рассматривать две тенденции, определяющие направление самопроизвольно протекающих процессов:
Стремление системы к достижению минимума энергии;
Стремление системы к максимуму энтропии, т.е. к неупорядоченности.
Таким образом, изменение энтропии является однозначным критерием самопроизвольности реакции, протекающей в изолированной системе:
∆S>0 – реакция протекает самопроизвольно;
∆S=0 - реакция находится в состоянии равновесия;
∆S<0 – реакция самопроизвольно не протекает.
Энергия Гиббса и направление химических реакций.
Биохимические реакции обычно происходят при изобарно –изотермических условиях. В этих условиях энергетическое состояние системы характеризуется энтальпией, а мерой неупорядоченности системы будет произведение температуры и энтропии. Функцией, учитывающей обе эти характеристики и противоположность в тенденции их изменения при самопроизвольных процессах, является свободная энергия Гиббса.
Энергия Гиббса (или изобарно – изотермический потенциал) является обобщенной функцией состояния системы, учитывающей энергетику и неупорядоченность системы при изобарно – изотермических условиях.
Изменение энергии Гиббса для биохимических процессов в условиях, отличных от стандартных, можно рассчитать на основе экспериментальных значений ∆Н и ∆S для этих процессов по уравнению:
∆G =∆Н - Т∆S,
где ∆Н - характеризует полное изменение энергии системы при p,T = const и отражает стремление системы к минимуму энергии (энтальпийный фактор);
Т∆S – характеризует ту часть энергии, которую нельзя превратить в работу, и отражает стремление системы к максимуму неупорядоченности (энтропийный фактор);
∆G – характеризует ту часть энергии, которую можно перевести в работу, и является термодинамическим критерием самопроизвольного протекания любых процессов при p,T = const.
Если в уравнение для расчета свободной энергии Гиббса ввести значение ∆Н°р. и ∆S°р., найденные с использованием следствия из закона Гесса, то мы получаем формулу для расчета ∆G реакции, протекающей в стандартных условиях:
∆G°p.f=∑νj∆G°j - ∑νi∆G°i
где∆G°j, ∆G°i – значения энергии Гиббса продуктов реакции и исходных веществ, νj ,νi - соответствующие стехиометрические коэффициенты в уравнении химической реакции.
В термодинамических расчетах используют значения энергии Гиббса, измеренные при стандартных условиях (∆G°, кДж/моль). Данные величины приведены в справочниках термодинамических величин. Для простых веществ в термодинамически устойчивой форме стандартная энергия Гиббса их образования принята равной нулю.
Рассчитав ∆G химической реакции, можно не производя экспериментов, дать ответ о принципиальной (термодинамической) возможности (или невозможности) ее протекания:
∆G<0 – реакция протекает самопроизвольно;
∆G=0 – реакция находится в состоянии равновесия;
∆G>0 – несамопроизвольная реакция (самопроизвольна обратная реакция).
Знак ∆G, а значит, и самопроизвольность реакции зависит от величины соотношения ∆Н и Т∆S. Самопроизвольное осуществление реакции (∆G<0) возможно в следующих случаях:
1) ∆Н<0 (экзотермический процесс) и в то же время |∆Н |>| Т∆S |, т.е. при экзотермических процессах знаки ∆Н и ∆G совпадают, что означает возможность протекания процесса независимо от знака ∆S;
2) ∆Н>0 (эндотермический процесс) и |∆Н |<| Т∆S |, тогда возрастание энтальпии компенсируется значительно большим ростом энтропийного фактора, что осуществимо при высоких температурах или при реакциях с участием газовой фазы, когда наблюдается значительное увеличение энтропии. Этим и объясняется возможность протекания эндотермических реакций, что не согласуется с принципом Бертло о самопроизвольности только экзотермических реакций. Судить о направлении процесса по знаку изменения энтальпии в соответствии с этим признаком можно лишь: а) при низких температурах (при Т→0, Т∆S→0, и Т∆S<< ∆Н), когда знаки изменения свободной энергии и энтальпии совпадают; б) в конденсированных системах, в которых в процессе взаимодействия энтропия меняется незначительно (беспорядок не может существенно возрасти, если, например, одно кристаллическое вещество превращается в другое кристаллическое вещество). Поэтому при низких температурах и в конденсированных системах возможно лишь протекание экзотермических реакций (∆G<0, когда ∆Н<0).
Химическое равновесие.
Химические реакции бывают обратимыми и необратимыми.
Необратимыминазываются реакции, которые протекают только в одном направлении до полного израсходования одного из реагирующих веществ.
2Ca + O2→2CaO (тв.)
Ca + H2SO4 (разб.)→ CaSO4+H2↑
4Ca +5 H2SO4 (конц.)→ 4CaSO4+H2S +4H2O
NH4NO3→ 2H2O +N2O↑
Критериями необратимости процесса можно считать выделение газа в процессе реакции, образование твердых и малодиссоциирующих соединений.
Однако в природе необратимых реакций меньше, чем обратимых.
Обратимыминазываются процессы, в которых одновременно протекают две взаимно противоположные реакции – прямая и обратная. Например,
H2 + I2 ↔2HI
CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O
Главная особенность протекания обратимых реакций заключается в стремлении достичь динамического равновесия, так как это состояние возникает и поддерживается вследствие протекания реакций в двух противоположных направлениях с одинаковыми скоростями.
Химическое равновесное состояние системы характеризуется:
1) равенством скоростей прямой и обратной реакции;
2) отсутствием изменений величин параметров и функций состояния системы : концентрации реагентов, энтальпии, энтропии и энергии Гиббса для прямой и обратной реакций.
Поскольку в состоянии химического равновесия система достигает минимально возможного значения энергии Гиббса, то реакция, которая приводит в данных условиях к состоянию равновесия, всегда самопроизвольна. Рассмотрим на графике изменение энергии Гиббса в закрытой системе в обратимой химической реакции (р, Т=const):
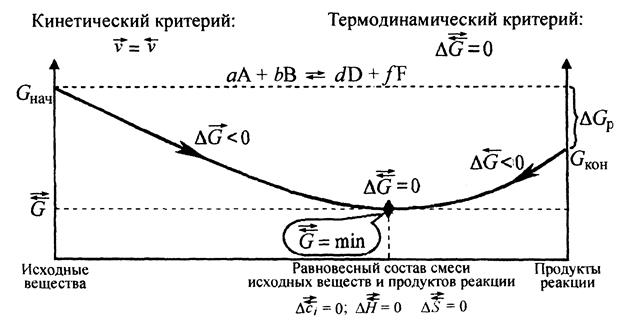
В этом случае изменение энергии Гиббса в системе характеризуется минимальным значением, к которому возможен подход, как со стороны исходных веществ, так и со стороны продуктов реакции.
Так как в состоянии равновесия скорости прямой и обратной реакции равны, то, используя закон действующих масс, выразим значение скоростей прямой (V1) и обратной реакций (V2) :
aА +bB ↔ cC + dD
Vпрям. р.=k∙[A]a∙[B]b, Vобрат. р.=k∙[C]c∙[D]d
Где [A],[B],[C],[D] – равновесные концентрации реагентов и продуктов обратимой реакции, a,b,c,d – стехиометрические коэффициенты в уравнении реакции.
Равновесными концентрацияминазываются концентрации всех веществ системы, которые устанавливаются в ней при наступлении состояния химического равновесия.
Соотнеся скорости обратной и прямой реакции, получаем:
V2 k∙[C]c∙[D]d
----- = -------------
V1 k∙[A]a∙[B]b
Так как рассматриваемые реакции являются противоположными друг другу, то и значение отношения констант их скоростей и равновесных концентраций реагентов и продуктов реакции есть величина постоянная.
[C]c∙[D]d
Кс= ------------
[A]a∙[B]b
(для реакции aA + bB↔ cC +dD)
Величина Кс, равная отношению произведений равновесных концентраций к произведению равновесных концентраций реагентов, взятых в степени их стехиометрических коэффициентов, называется константой равновесия обратимой реакции.
Константа химического равновесия (Кс) обратимого процесса равна отношению произведения равновесных концентраций конечных продуктов к произведению равновесных концентраций исходных веществ в степени, равной стехиометрическим коэффициентам соответствующих химических веществ в химической реакции.
Константа равновесия (Кр) для обратимых реакций, проходящих в газовой фазе, может быть также выражена отношением произведений парциального давления продуктов реакции к произведению парциального давления реагентов, взятых в степени их стехиометрических коэффициентов.
Например, для реакции:
N2 (г) + 3H2 (г)↔ 2NH3 (г)
Константы равновесия могут быть записаны следующим образом:
Р2 (NH3) [NH3]2
Kp= -------------- Кс = -------------
P(N2)∙P3(H2) [N2]∙[H2]3
Связь между константами равновесия, выраженными через величины парциального давления и равновесных концентраций реагентов и продуктов реакции, отражена в формуле:
Кр = Кс∙(RT) ∆ν
где ∆ν =Σ νпрод. - Σ νисх.
В случае гетерогенных реакций в выражение константы химического равновесия входят парциальные давления (или концентрации) только газообразных участников реакции. Парциальные давления и концентрации веществ в твердом и жидком состояниях принимаются за единицу, так как их химические потенциалы равны. Например, для реакции
С (тв.) + О2 (г.)↔ СО2 (г.)
V→ =k∙[O2] V← = k∙[CO2]
[CO2]
Kc = ---------
[O2]
Для выражения константы равновесия (Ка) обратимых реакций растворов электролитов, значения равновесных концентраций заменяют на равновесные активности:
aCc ∙ aDd
Ка= ------------
aAa ∙ aBb
где а = С(х)∙γ, γ – коэффициент активности
(для реакции aA + bB↔ cC +dD)
Значение константы равновесия определяет положение равновесия, т.е. относительное содержание исходных веществ и конечных продуктов реакции, находящейся в состоянии равновесия.
Если Кс> 1,то в системе выше содержание конечных продуктов реакции, т.е. положение равновесия смещено в сторону прямой реакции.
Если Кс< 1, то в системе выше содержание исходных веществ, т.е. положение равновесия смещено в сторону обратной реакции.
Величина изменения свободной энергии Гиббса (∆G°) связана с константой равновесия обратимой реакции уравнением, выведенным Вант Гоффом в 1885 г. Он доказал, что между константой равновесия и энергией Гиббса обратимой реакции существует логарифмическая зависимость:
∆Gр. = - R∙T∙ln Kc,
где R – универсальная газовая постоянная, Т – температура (К).
Для упрощения математических расчетов зависимость константы равновесия и энергии Гиббса записать следующим образом:
∆Gр. = - 2,303∙R∙T∙lg Kc
Это уравнение дает возможность, зная ∆G, вычислить константу равновесия, и, наоборот, по экспериментально найденному значению константы равновесия рассчитать ∆G реакции.
Пользуясь уравнением изотермы химической реакции:
[C]c∙[D]d
∆G = ∆G° + RTln ----------
[A]a∙[B]b
(для реакции aA + bB↔ cC +dD)
можно определить, в каком направлении и до какого предела может протекать реакция в конкретных условиях при заданном составе исходных реагентов и продуктов реакции. Это же уравнение позволяет определить, какими должны быть условия реакции и состав исходной смеси, чтобы реакция протекала в нужном направлении и до рассчитанного предела.
Константы равновесия обратимых реакций зависят от температуры и природы реагирующих веществ, но не зависят от концентрации (Кс), активности (Ка), давления (Кр) реагирующих веществ.
Таким образом, в случае протекания обратимых реакций система самопроизвольно приходит к состоянию химического равновесия, из которого она без внешнего воздействия не может выйти, поскольку это требует увеличения энергии Гиббса.
Влияние изменения условий на химическое равновесие определяется принципом Ле Шателье:
Если на систему, находящуюся в состоянии химического равновесия, оказывать воздействие путем изменения концентрации реагентов, давления и температуры в системе, то равновесие всегда смещается в направлении той реакции, протекание которой ослабляет это воздействие.
Влияние изменения концентрации реагентов. В соответствии с принципом Ле Шателье введение в равновесную систему дополнительных количеств какого-либо реагента вызывает сдвиг равновесия в том направлении, при котором его концентрация уменьшается. Поэтому избыток исходного вещества (исходных веществ) вызывает смещение равновесия вправо, увеличивая степень превращения других реагентов; добавление продукта (продуктов) реакции вызывает смещение равновесия влево, т.е. уменьшение степени полноты ее протекания. Так, избыток кислорода увеличивает степень превращения SO2 в SO3 при контактном получении триоксида серы – возрастание концентрации молекул веществ ускоряет ту реакцию, которая их израсходует. В целях повышения выхода продуктов реакции, во многих случаях смещение равновесия в сторону продуктов взаимодействия можно осуществить и их удалением из реакционной зоны, связывая их в малодиссоциирующие, труднорастворимые или нелетучие вещества. Так, введение в равновесную систему:
СН3СООН + СН3ОН ↔ СН3СООСН3 + Н2О
водоотнимающих веществ (например, Н2SO4) позволяет сместить равновесие этой реакции вправо, т.е. в сторону образования продуктов реакции.
Таким образом, при изменении в равновесной системе концентрации любого из реагентов, исходное соотношение концентраций реагентов и величина константы равновесия в состоянии последующего равновесия не изменятся, хотя положение равновесия сместится в ту или иную сторону.
Влияние изменения давления в системе.Давление не изменяет величины константы равновесия обратимой реакции, так как она зависит только от температуры и природы реагирующих веществ, следовательно, с давлением меняется ∆G реакции.
Повышение давления в системе смещает химическое равновесие в направлении реакции, идущей с образованием меньшего числа молей газообразных веществ, т.е. в сторону уменьшения объема, а понижение давления в системе вызывает сдвиг равновесия в противоположную сторону. При равном числе молей газообразных исходных веществ и продуктов реакции изменение давления не смещает химическое равновесие. Влияние давления на химическое равновесие при Т = const показано схемой, где в первом случае рассмотрена реакция, сопровождающаяся уменьшением объема; а во втором – реакция, сопровождающаяся увеличением объема.
Чем меньше абсолютное значение изменения объема в системе, тем меньше влияние давления на равновесие. Поэтому при небольших значениях давления оно не влияет на равновесие системы. В гетерогенных процессах объемом конденсированной фазы можно пренебречь, однако, при сверхвысоких давлениях объем газов становится соизмеримым с объемом твердых тел и жидкостей. Если рассматривать реакции, в которых среди реагентов нет газообразных продуктов, например, процесс модификационного превращения С(графит)→С(алмаз), так как в данном случае изменение объема ничтожно мало, то даже для незначительного сдвига равновесия вправо требуется весьма значительное изменение (повышение) давления.
Для точного учета влияния давления на равновесие реакций, особенно при высоких давлениях, следует принимать во внимание изменение величины объема с давлением; так, если по мере повышения давления абсолютное значение изменения объема уменьшается, то будет уменьшаться и эффект действия давления в системе.
Влияние изменения температуры в системе.В соответствии с принципом Ле Шателье нагревание вызывает смещение равновесия в сторону того из двух встречных процессов, протекание которого сопровождается поглощением теплоты, т.е. в сторону эндотермической реакции. Понижение температуры приводит к противоположному эффекту: равновесие смещается в сторону того процесса, протекание которого сопровождается выделением тепла, в сторону экзотермической реакции .Из этого следует, что для суждения о влиянии температуры необходимо знать тепловой эффект изучаемого процесса. Как уже говорилось ранее, тепловой эффект реакции может быть определен опытным путем или по закону Гесса. Направление смещения и его степень определяются знаком и величиной теплового эффекта; чем больше ∆Н, тем значительнее влияние температуры; наоборот, если ∆Н близко к нулю, то и температура практически не влияет на равновесие. На схеме отражено влияние температуры на химическое равновесие при р = const, где первая зависимость приведена для эндотермической реакции, вторая – для экзотермической реакции. Законы наступления, сохранения и смещения динамического равновесия справедливы не только для химических и физико-химических процессов, но и имеют аналоги в живой природе. Соблюдение этого принципа в живых системах позволяет им поддерживать состояние гомеостаза. Основу гомеостаза составляет стационарное состояние системы, причем далекое от равновесия, из-за чего живые системы способны к эволюции.
Основы биоэнергетики.
Протекание жизненных процессов требует затрат энергии. Источником энергии для живых организмов служит пища. Главными компонентами пищи являются жиры, белки и углеводы, окисление которых сопровождается выделением энергии. В медицине энергетическую характеристику продуктов питания принято считать в калориях. Поскольку пища – разнородная смесь, ее калорийность, как правило, приводят в виде средних значений на 100 г.
Калорийностью питательных веществ – называется энергия, выделяемая при полном окислении (сгорании)1 г. питательных веществ.
Взаимосвязь между единицами энергии выражается соответствием:
1 калория = 4.18 Дж
Хорошо известная всем калорийность пищевых продуктов – не что иное, как теплота их сгорания, которую можно измерить экспериментально.
Начало таким измерениям положили Антуан Лавуазье и Пьер Симон в 1780 г. Определяя при помощи калориметра количество теплоты, выделенное морской свинкой, они установили, что окисление пищи в организме и вне его, дает близкие тепловые эффекты. На основании этих опытов был сделан важный вывод: живой организм выделяет теплоту за счет окисления в нем пищи кислородом воздуха. Это позволило объяснить различие в цвете артериальной и венозной крови, а в дальнейшем послужило исходным пунктом к открытию первого закона термодинамики.
Конечно, окисление питательных веществ в организме протекает совсем не так, как в калориметре. Это сложные многостадийные процессы с участием биологических катализаторов (ферментов). Однако, согласно закону Гесса, теплота, выделяемая при окислении питательных веществ, не зависит от того, окисляется она в организме или в калориметре, если продукты ее окисления одинаковы. Наибольшую энергетическую ценность имеют жиры, при окислении которых выделяется 37.7 –39.8 кДж/г (9.3 ккал/г). В процессе усвоения углеводов в организме человека выделяется 16.5 –17.2 кДж/г (4.1 ккал/г). На этом же уровне находится и калорийность белков.
Информация о выделении теплоты очень важна для понимания путей преобразования различных веществ в энергию в живых организмах.
В основе научной диетологии лежит соответствие калорийности пищевого рациона энергозатратам человека. Биоэнергетику организма можно регулировать не только с помощью выбора отдельных продуктов, но, главным образом, их сочетанием.
Зная основные термодинамические закономерности, химический состав продуктов питания и энергетические характеристики питательных веществ, врач должен уметь с учетом суточной потребности человека в энергии и на основе энергетического баланса его жизнедеятельности составить оптимальный рацион питания (энергоменю).
